Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Свечи куплены и доставлены в лабораторию. О том, что такое «октановое число» и как его
измеряют, мы рассказывали не раз. Напомним, что из существующих технологий производства
бензинов лишь одна - каталитический риформинг - позволяет сразу получить нужное октановое число,
вплоть до 98. Таких бензинов сравнительно немного, при этом они весьма дороги! А можно ли из
низкооктановых бензинов, сравнительно дешевых, получить высокооктановое топливо? Да, конечно -
для этого существует так называемая «химизация» топлива, когда нужное октановое число достигается
добавкой различного рода присадок (подробности - в нашей врезке). Здесь-то и нашел свою нишу
ферроцен - находка для нефтяников: он столь же дешев (особенно китайский!), сколь и эффективен.
Если следовать разрешенным нормам, то одного килограмма этого оранжево-коричневого порошка
стоимостью в десяток условных единиц хватает для изготовления 50 тонн (!) высокооктанового
бензина. Сказка, а не порошок… Но вот беда: он порождает множество отложений в камере сгорания и
выпускной системе. Железо, которое является основой этого металлоорганического соединения,
гореть почему-то не хочет - оно осаждается и на клапаны, и на свечи, и на стенки выпускной системы,
причем не просто так, а в виде токопроводящих оксидных пленок цвета качественной ржавчины. Как с
этим бороться? Да как в бородатом анекдоте - «летай, сынок, но так низенько-низенько…». С
ферроценом нечто подобное - лей, но маленько-маленько. Раньше, во времена преимущественно
простеньких карбюраторных двигателей разрешали использовать эту бяку в концентрации не больше
37 мг/л топлива. Для «башковитых» впрысковых моторов и этого оказалось много - токопроводящие
отложения стали весело убивать лямбда-зонды и катализаторы. Наши подумали-подумали и решили…
не запрещать ферроцен совсем, как это сделано в большинстве цивилизованных стран, а уменьшить
его предельно допустимую концентрацию - до 17 мг/л. Но уж коли хоть что-то разрешено, а на
горизонте маячит суперприбыль от реализации копеечного прямогонного бензина под видом
супертоплива, то предсказать последствия нетрудно! Вдали от крупных городов и контролирующих
органов удержаться от соблазна ох как трудно... А теперь - к практике! Что реально происходит со
свечами, работающими на отравленном ферроценом бензине?
Свечи зажигания - это макушка айсберга, который может пострадать от ферроцена. Еще есть
лямбда-зонды и катализаторы - но ими займемся позднее: и без того ферроценовый тест очень
длинный. И дорогой... Для испытаний решили взять самые известные свечи с «надежной»
родословной, дабы на корню пресечь разговоры о том, что пациент помер сам по себе. Компания
подобралась разноликая и достойная. Классические одноэлектродные свечи представили французские
Beru Ultra 14R-7DO, из «трехэлектродок» взяли Brisk DR15-TC1 Extra, а из современных свечей с
«драгоценными» электродами пригласили Bosch Platin WR7DP. И это еще не все. От очень редкого, но
столь же эффективного класса иридиевых свечей взяли японские Denso Iridium IK20 с диаметром
электрода 0,4 мм, а обойтись без Beru Ultra Platin UX79P было просто невозможно: этот комплект -
внимание! - и четырехэлектродный, и платиновый, и самоочищающийся! Для разнообразия в тест
включили плазменно-форкамерные свечи Plazmofor Super ПФА 17 ДРМ украинского производства.
Для начала на моторных стендах были сняты базовые характеристики двигателей с каждым из комплектов. Заодно оценили процесс искрообразования у всех свечей. Ничего нового по сравнению с тем, что получали ранее, не увидели - и это хорошо: стабильность - признак качества! А затем началось… Для каждого комплекта свечей на отдельном двигателе, заранее определенном на заклание, выжгли по сорок литров бензина с запредельным по нашим нормам содержанием ферроцена - 100 мг/л. Бензин изготовили - точнее, набодяжили - сами... Если соответствовать нашим старым нормам, то это - две с половиной полных заправки, если новым - то более пяти. Впрочем, такую дозу легко можно хватануть и при одной-единственной заправке - если уж совсем не повезет. Зачем брали отдельный двигатель - понятно. Ведь ферроцен дает отложения не только на свечах, и все это влияет на показатели мотора. Поэтому контрольные замеры делали на «чистых» моторах, ставя туда полуживые свечи.
Начнем с хорошего известия -все свечи остались живы, а потому разговоры о возможной остановке
в чистом поле даже после такой экстремальной заправки ушли с повестки дня. Но свечам стало очень
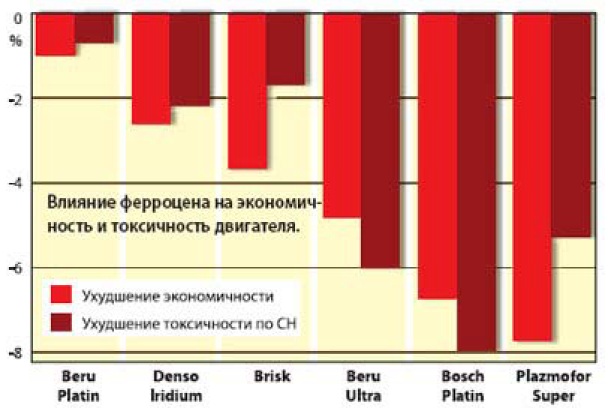
плохо, причем в разной степени: это видно по увеличению расхода топлива и росту токсичности.
Больше всего пострадали украинские Plazmofor. Чуть лучше чувствовали себя немецкие Bosch Platin.
Классические Beru Ultra отработали поспокойнее, но и на них влияние ферроцена более чем заметно.
Зато окислы азота снизились и там, и там - на те же 18-20%. Хорошо? Напротив - это говорит о
нарушениях в искрообразовании, при которых часть топлива летит несгоревшей прямо в трубу! Отсюда
и рост расхода топлива, и выход несгоревших углеводородов -а окислы азота падают потому, что
температуры сгорания уменьшаются. А вот иридиевые свечи Denso и «многоэлектродки» Brisk
оказались значительно более лояльными к ферроцену. Для них снижение расхода топлива составило
примерно 2-3%, а рост токсичности по СН - 7-9%. Скорее всего, Denso спасло то, что тонкий
центральный электрод диаметром всего 0,4 мм создает напряженность электрического поля,
сконцентрированную в очень малом объеме, в результате разряд «сносит» с электродов все - и
органические отложения, и нагары, и оксиды железа. А для Brisk отработали три боковых электрода -
искра начинает бить по наиболее простому пути, поскольку есть альтернатива. Вот пропусков вспышек
и меньше. Если следовать такой логике, то свечи Beru Ultra Platin вообще должны были не
почувствовать ферроцена! Там и самоочистка, и платиновый центральный электрод, и четыре боковых
электрода! Так оно и получилось - изменение параметров двигателя с этими свечами уложилось в
пределы погрешности измерения. Кстати, по утверждениям некоторых специалистов, при загрязнении
ферроценом падает сопротивление изолятора и свеча начинает «шить»… Вот этого наш эксперимент
не выявил - как для новых, так и для загрязненных свечей мегаомметр показал одно и то же
сопротивление - бесконечность!
Известны три основных принципа в производстве высокооктановых топлив путем их химизации.
Первый - использование добавок на базе ароматических углеводородов. Пример - монометиланилин
(ММА), имеющий октановое число 280. Один процент добавки такого состава повышает октановое
число базового бензина на 1-2 единицы. Основной недостаток - повышение токсичности отработавших
газов и уровня органических отложений в камере сгорания. Второй - использование высокооктановых
компонентов на базе спиртов или эфиров. Наиболее распространенное - метилтретбутило-вый эфир
(МТБЭ). Это кислородсодержащие вещества, и добавка их к базовому топливу повышает полноту
сгорания, снижает токсичность отработавших газов. Основные недостатки - сравнительно низкое
октановое число (110-120), поэтому требуется большой процент добавки - до 15%, а это существенно
снижает общую теплотворную способность товарного топлива. Кроме того, у таких топлив повышенная
агрессивность к резинам и пластикам. Третий - использование металлсодержащих антидетонаторов на
базе свинца, железа, никеля, марганца и других металлов. Основное преимущество этих присадок -
очень высокая «работоспособность»: тетраэтилсвинец имеет эффективность в 600 раз большую, чем
бензол, а ферроцен - в 450-500 раз. Основные недостатки - плохая выносимость из камеры сгорания, а
также резкий рост канцерогенной опасности отработавших газов.
Тем, кто сразу полез в конец статьи за информацией на тему «Что купить?», попробуем дать
несколько советов - они могут пригодиться перед дальней и нецивилизованной дорогой. Во-первых,
прихватить с собой канистру с качественным и проверенным бензином, заправившись перед выездом
«под завязку». Во-вторых, избегать неизвестных, особенно контейнерных заправок на трассе, сколь бы
привлекательной ни казалась цена. А уж если ферроценовое насилие над мотором представляется
неизбежным, то поставьте либо самоочищающиеся «многоэлектродки», либо что-то с тонким
центральным электродом. И - СЧАСТЛИВОГО ПУТИ!
Для справки (Википедия):
Ферроцен — бис-η5-циклопентадиенилжелезо (II) (η5-С5Н5)2Fe.
Свойства. Оранжевые кристаллы; температура плавления 173°C, температура кипения 249°C; плотность 1,49 г/см3 (25°C); устойчив до 470°C; возгоняется при атмосферном давлении; растворим в органических растворителях, нерастворим в воде; устойчив к действию воздуха, горячей конц. соляной кислоте и растворам щелочей.
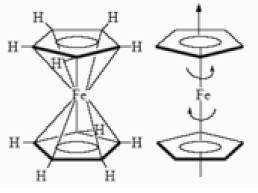
Открытие. В 1951 году Т. Кили и П. Посон, пытаясь синтезировать новый углеводород — дициклопентадиенил, неожиданно для себя выделили совершенно новое, исключительно устойчивое жёлто-оранжевое кристаллическое соединение, содержащее железо. Потребовалось около года, чтобы понять, как построено это соединение. Выяснилось, что атом железа «запечатан» между двумя симметричными пятичленными кольцами, причём так, что все расстояния Fe—C оказались одинаковыми. Кроме того, оказалось, что кольца в молекуле свободно вращаются вокруг оси, соединяющей центры колец (в твёрдом состоянии более устойчива заторможенная конформация).
Соединение было названо ферроценом, а подобный структурный тип — сэндвичевым. Сандвичевая структура ферроцена была установлена Р. Вудвордом и независимо от него Э. Фишером в 1952 году на основании магнитных, спектральных и рентгеноструктурных данных.
Свойства. Многими исследователями было показано, что по общему характеру реакционной способности ферроцен напоминает бензол; это привело к тому, что очень скоро после открытия ферроцен был назван небензоидной ароматической системой. Для него характерны три типа химических превращений: замещение водорода в С5Н5-кольцах без разрыва связей Fe—С, окисление по атому Fe и разрыв связи Fe—C.
Реакции электрофильного замещения для ферроцена протекают легче, чем для бензола; при этом образуются как моно- так и гетероаннулярные (содержащие заместители в разных циклах) дизамещённые производные.
Ферроцен легко и обратимо окисляется до катион-радикала ферроцения (кислородом воздуха в кислой среде, перекисью водорода, иодом, хлоридом железа (III) и т.п.). При окислении не происходит заметных изменений в геометрии молекулы ферроцена. Разбавленные растворы солей ферроцения окрашены в синий цвет, концентрированные — в красный.
Связь Fe—С в ферроцене мало реакционноспособна и разрывается только при действии очень сильных восстановителей: водорода в присутствии катализатора (Никель Ренея) (300°C, 2,5 МПа) либо растворов щелочных металлов в жидком аммиаке или аминах. При взаимодействии ферроцена с аренами в присутствии AlCl3/Al одно кольцо замещается на арен и образуется катион [Fе(С5Н5)(арен)]+.
Применение. Ферроцен используется в нефтяной промышленности в качестве антидетонатора. Применяется как термостабилизатор полиэтилена и диеновых каучуков (например, бутадиеновых); используется в синтезе некоторых медицинских препаратов.
СМЕРТЕЛЬНЫЙ НОМЕР
БОДЯГА ТРЕТЬЕЙ СТЕПЕНИ

Для начала на моторных стендах были сняты базовые характеристики двигателей с каждым из комплектов. Заодно оценили процесс искрообразования у всех свечей. Ничего нового по сравнению с тем, что получали ранее, не увидели - и это хорошо: стабильность - признак качества! А затем началось… Для каждого комплекта свечей на отдельном двигателе, заранее определенном на заклание, выжгли по сорок литров бензина с запредельным по нашим нормам содержанием ферроцена - 100 мг/л. Бензин изготовили - точнее, набодяжили - сами... Если соответствовать нашим старым нормам, то это - две с половиной полных заправки, если новым - то более пяти. Впрочем, такую дозу легко можно хватануть и при одной-единственной заправке - если уж совсем не повезет. Зачем брали отдельный двигатель - понятно. Ведь ферроцен дает отложения не только на свечах, и все это влияет на показатели мотора. Поэтому контрольные замеры делали на «чистых» моторах, ставя туда полуживые свечи.
КРАСНАЯ СМЕРТЬ, КАК ОНА ЕСТЬ
ОТКУДА БЕРЕТСЯ ОКТАН?
СОВЕТЫ ПЕРЕД ДАЛЬНЕЙ ДОРОГОЙ
(журнал За рулем)
Для справки (Википедия):
Ферроцен — бис-η5-циклопентадиенилжелезо (II) (η5-С5Н5)2Fe.
Свойства. Оранжевые кристаллы; температура плавления 173°C, температура кипения 249°C; плотность 1,49 г/см3 (25°C); устойчив до 470°C; возгоняется при атмосферном давлении; растворим в органических растворителях, нерастворим в воде; устойчив к действию воздуха, горячей конц. соляной кислоте и растворам щелочей.

Открытие. В 1951 году Т. Кили и П. Посон, пытаясь синтезировать новый углеводород — дициклопентадиенил, неожиданно для себя выделили совершенно новое, исключительно устойчивое жёлто-оранжевое кристаллическое соединение, содержащее железо. Потребовалось около года, чтобы понять, как построено это соединение. Выяснилось, что атом железа «запечатан» между двумя симметричными пятичленными кольцами, причём так, что все расстояния Fe—C оказались одинаковыми. Кроме того, оказалось, что кольца в молекуле свободно вращаются вокруг оси, соединяющей центры колец (в твёрдом состоянии более устойчива заторможенная конформация).
Соединение было названо ферроценом, а подобный структурный тип — сэндвичевым. Сандвичевая структура ферроцена была установлена Р. Вудвордом и независимо от него Э. Фишером в 1952 году на основании магнитных, спектральных и рентгеноструктурных данных.
Свойства. Многими исследователями было показано, что по общему характеру реакционной способности ферроцен напоминает бензол; это привело к тому, что очень скоро после открытия ферроцен был назван небензоидной ароматической системой. Для него характерны три типа химических превращений: замещение водорода в С5Н5-кольцах без разрыва связей Fe—С, окисление по атому Fe и разрыв связи Fe—C.
Реакции электрофильного замещения для ферроцена протекают легче, чем для бензола; при этом образуются как моно- так и гетероаннулярные (содержащие заместители в разных циклах) дизамещённые производные.
Ферроцен легко и обратимо окисляется до катион-радикала ферроцения (кислородом воздуха в кислой среде, перекисью водорода, иодом, хлоридом железа (III) и т.п.). При окислении не происходит заметных изменений в геометрии молекулы ферроцена. Разбавленные растворы солей ферроцения окрашены в синий цвет, концентрированные — в красный.
Связь Fe—С в ферроцене мало реакционноспособна и разрывается только при действии очень сильных восстановителей: водорода в присутствии катализатора (Никель Ренея) (300°C, 2,5 МПа) либо растворов щелочных металлов в жидком аммиаке или аминах. При взаимодействии ферроцена с аренами в присутствии AlCl3/Al одно кольцо замещается на арен и образуется катион [Fе(С5Н5)(арен)]+.
Применение. Ферроцен используется в нефтяной промышленности в качестве антидетонатора. Применяется как термостабилизатор полиэтилена и диеновых каучуков (например, бутадиеновых); используется в синтезе некоторых медицинских препаратов.