Химия и Химики № 1 2017
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 1 2017 Журнал Химиков-Энтузиастов |
Эксперименты с бором ч.1, 2, 3 Experiments with boron Добрый Химик |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Получение бора
Аморфный бор получил восстановлением оксида бора натрием. Рецепт есть в Энциклопедическом словаре Брокгауза и Ефрона:
Preparation of elemental boron Для получения аморфного бора (по Вёлеру и Девиллю) в раскаленный чугунный тигель всыпают смесь 100 ч. борного ангидрида с 60 ч. металлического натрия и покрывают все слоем прокаленной поваренной соли (от 40 до 50 ч.); наступает бурная реакция, причем часть борного ангидрида отдает свой кислород натрию; бор выделяется в свободном состоянии, и вместе с тем образуется бура; сплав перемешивают железным прутом, выливают в воду, подкисленную соляной кислотой, и собирают остающийся нерастворенным бор на фильтре; в виде аморфного порошка он легко проходит через поры бумаги, висит в воде и сообщает ей бурую окраску, <...> сушить порошок следует на пористых фарфоровых пластинках при обыкновенной температуре, так как при более сильном подогревании бор легко загорается. Для реакции в качестве стального тигля удобен 100 мл китайский стаканчик из нержавейки. Крышка - из кружка жести. Вначале борная кислота обезвоживается в том же стаканчике в муфельной печи при 700-800 С. Затем стакан (наружные стенки) охлаждается водой, растрескавшийся стекловидный оксид бора удобно извлечь ударом молотка, подстелив под стакан бумагу. Потом борный ангидрид быстро измельчается ударами молотка или в ступке острожными ударами пестика. Ступка помещается в пакет. У меня кусочки оксида бора получились довольно крупные, тщательно дробить было лень - вещество очень твердое. Масса оксида бора - примерно 20 г. Натрий (12 г), порезанный ножом на мелкие кусочки, поместил в тигель, и засыпал его оксидом бора с добавлением 8 г хлорида натрия. Закрыл крышкой, (для надежности придавленной дополнительным грузом железа) и поместил в разогретую до 800°С печь. Тигель нагревался около 15 минут при температуре 800-900°С. После остывания внутри был плав грязно-коричнево-черного цвета. От удара молотка он отделился от стакана. Полученный плав раздробил на несколько кусков, поместил в стакан с водой, подкисленной соляной кислотой, воду нагрел до кипения. После охлаждения осадок и взвесь отфильтровал на воронке Бюхнера, залил 10 % раствором едкого калия, довел до кипения, потом нейтрализовал щелочь, прилив соляной кислоты. Отфильтровал под вакуумом. Бор образует тончайшую взвесь черного цвета, фильтруется довольно медленно, на фильтре промыл осадок водой и ацетоном (для ускорения сушки). Получилось примерно 1.2 г бора в виде тончайшей пыли. Выход небольшой (скорее всего из-за крупных кусков натрия и оксида бора), но для нескольких экспериментов с бором этого хватит. Вот часть полученного бора, цвет серо-черный: |

Бор Elemental boron |
|
Бор и азотная кислота
Реакция с концентрированной серной и азотной кислотой - наиболее доступными кислотами-окислителями - является важной для характеристики свойств неметаллов со средним значением электроотрицательности. Среди таких неметаллов следует назвать: серу, фосфор, кремний, йод, селен, теллур, мышьяк. Например, фосфор реагирует с азотной кислотой с образованием фосфорной кислоты. Elemental boron and nitric acid P + 5HNO3 = H3PO4 + 5NO2 + H2O Сера реагирует с азотной кислотой с образованием серной кислоты, а с серной кислотой - с образованием диоксида серы и воды. S + 2HNO3 = H2SO4 + 2NO S + 2H2SO4 = 3SO2 + 2H2O Кремний не реагирует с концентрированной серной и азотной кислотами. Чтобы растворить кремний, используют смесь азотной и плавиковой (фтористоводородной) кислоты. Азотная кислота играет роль окислителя, фтористоводородная - комплексообразователя. 3Si + 4HNO3 + 18HF = 3H2[SiF6] + 4NO + 8H2O Бор - типичный неметалл с невысокой электроотрицательностью. Как должна протекать его реакция с азотной кислотой? В практикуме Рипан Р. Четяну И. Руководство к практическим работам по неорганической химии (1965), С. 555 [ссылка] сказано: С концентрированной азотной или серной кислотой бор реагирует следующим образом: B + 3HNO3 = H3BO3 + 3NO2 2B + 3H2SO4 = 2H3BO3 + 3SO2 Опыт проводят в пробирке при нагревании. - И все: больше никаких подробностей. Значит - проверим опытным путем. Налил в стаканчик концентрированную азотную кислоту (60-70%) и всыпал туда небольшой шпателек аморфного бора. Произошла вспышка, которая сопровождалась шипением и образованием желтых искр. Появились бурые пары. Но пламя исчезло и после этого бурной реакции не последовало. Добавил еще один шпатель бора: снова вспышка, а потом - отсутствие всякой активности. Греть стакан до растворения бора не стал (ввиду тривиальности процедуры). Повторил эксперимент: снова при добавлении бора в азотную кислоту дважды произошла вспышка. Про такой эффект при взаимодействии аморфного бора с азотной кислотой в практикуме не было ни слова. Возможно, бор содержал примесь борида натрия, который и дал вспышку с кислотой? Но это практически исключено, т.к. полученный аморфный бор я кипятил с раствором соляной кислоты: бориды натрия в этих условиях разложились бы. Приведу еще раз фрагмент цитаты из Энциклопедического словаря Брокгауза и Ефрона: ...сушить порошок [аморфного бора] следует на пористых фарфоровых пластинках при обыкновенной температуре, так как при более сильном подогревании бор легко загорается. Другими словами, аморфный бор, полученный реакцией борного ангидрида с натрием (с последующей промывкой соляной кислотой), содержит активные частицы, способные воспламеняться на воздухе, если бор сушить при нагревании. Например, это могут быть очень мелкодисперсные частицы (вспомните, что железо и свинец - металлы средней активности - в мелкодисперсном виде вспыхивают на воздухе, т.е. обладают пирофорностью). Не удивительно, что реакция бора с азотной кислотой происходит со вспышкой. Такой "активной формы" бора в полученном образце, по-видимому, содержится мало, поэтому после вспышки дальнейшей бурной реакции не наблюдается. |

Бор и азотная кислота Elemental boron and nitric acid |

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
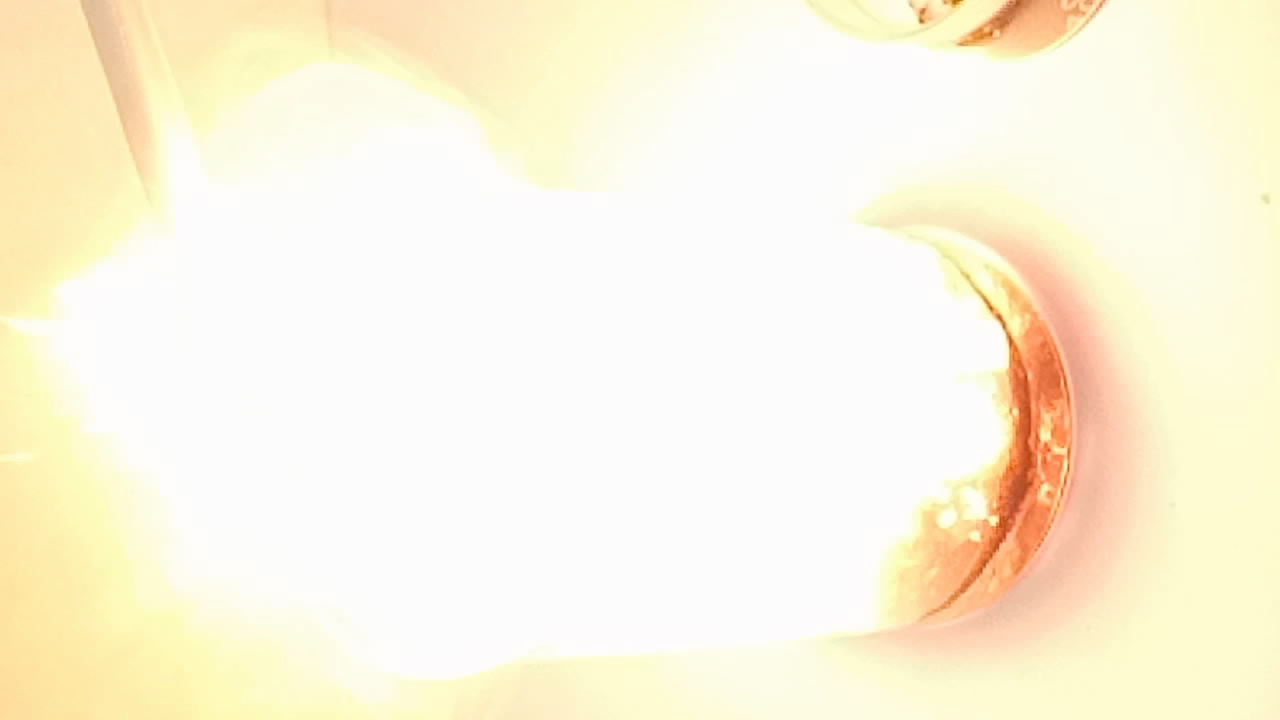
|

|

|

|

|
|
Горение бора в кислороде
Согласно практикуму Рипан Р. Четяну И. Руководство к практическим работам по неорганической химии (1965), С. 555 [ссылка] при нагревании в кислороде или на воздухе бор воспламеняется и сгорает красным пламенем с образованием борного ангидрида и выделением большого количества тепла.
Burning of elemental boron in oxygen Поместил бор в ложечку для сжигания, нагрел его в пламени зажигалки и внес в колбу с кислородом. Сначала бор горел красивым ослепительным бело-зеленым пламенем, затем - красным и белым. Образовался белый дым. На воздухе бор невзрачно "тлеет". |

Горение бора в кислороде Burning of elemental boron in oxygen |
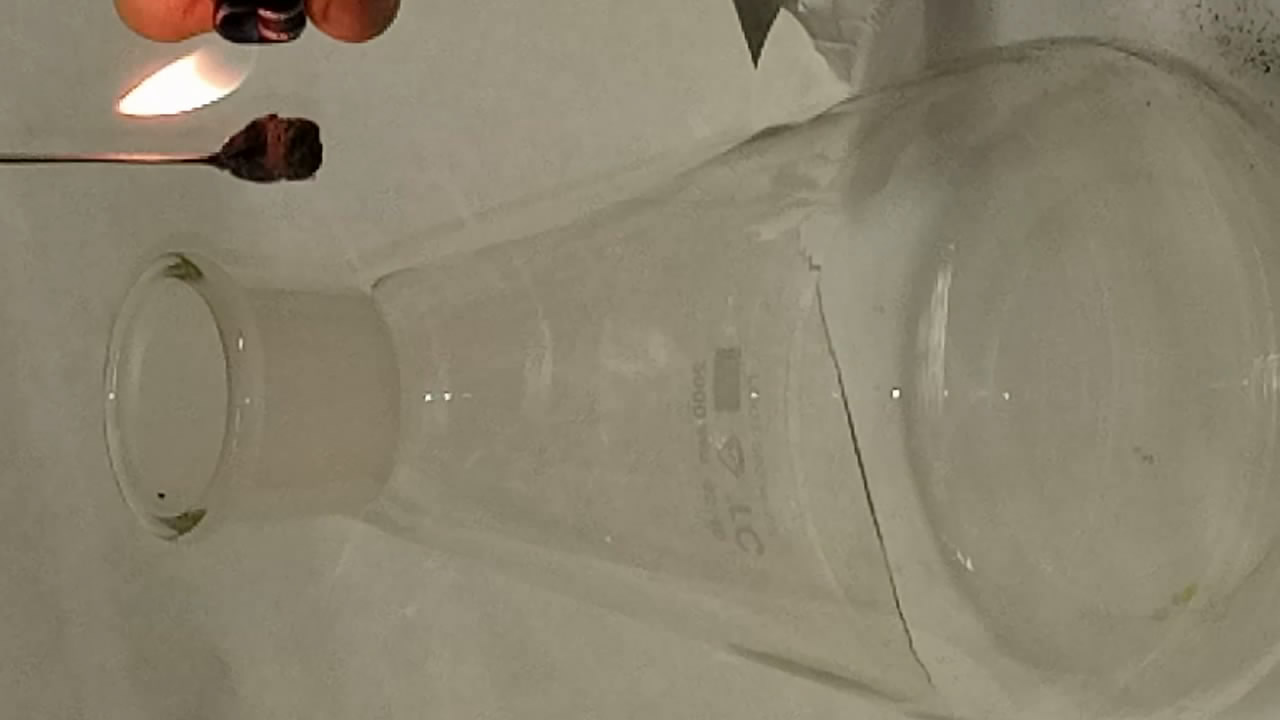
|

|

|
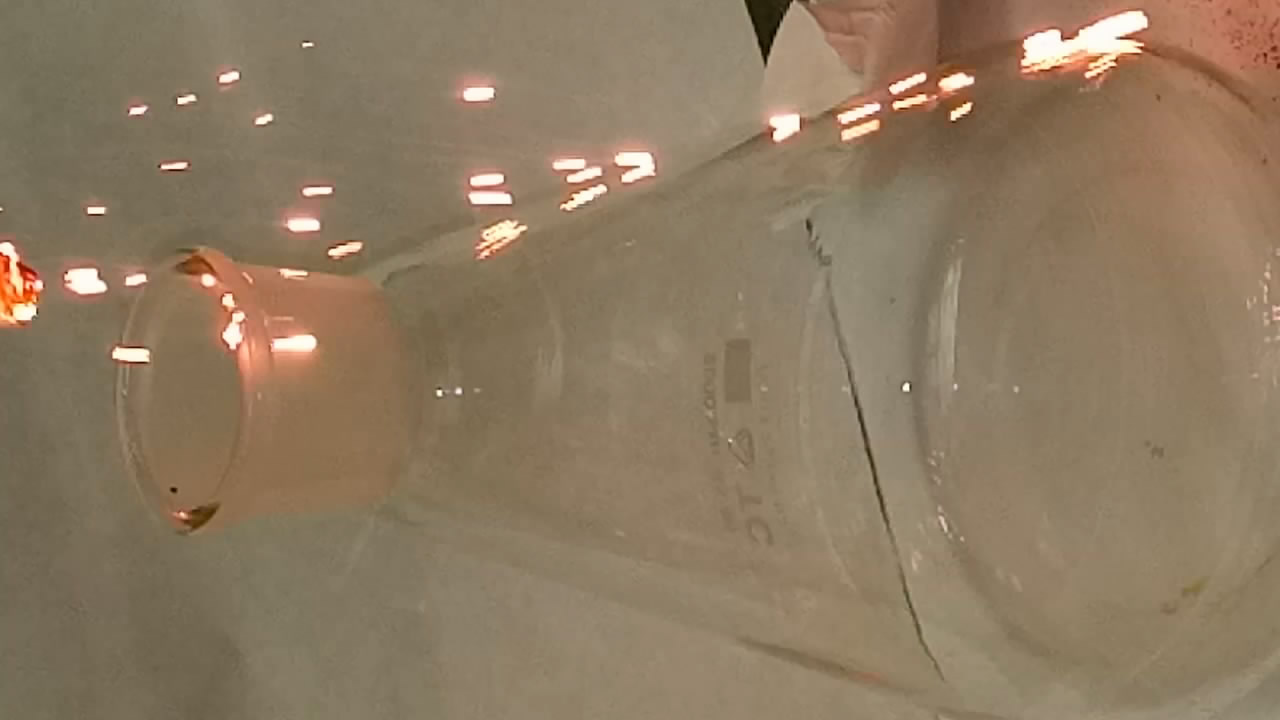
|
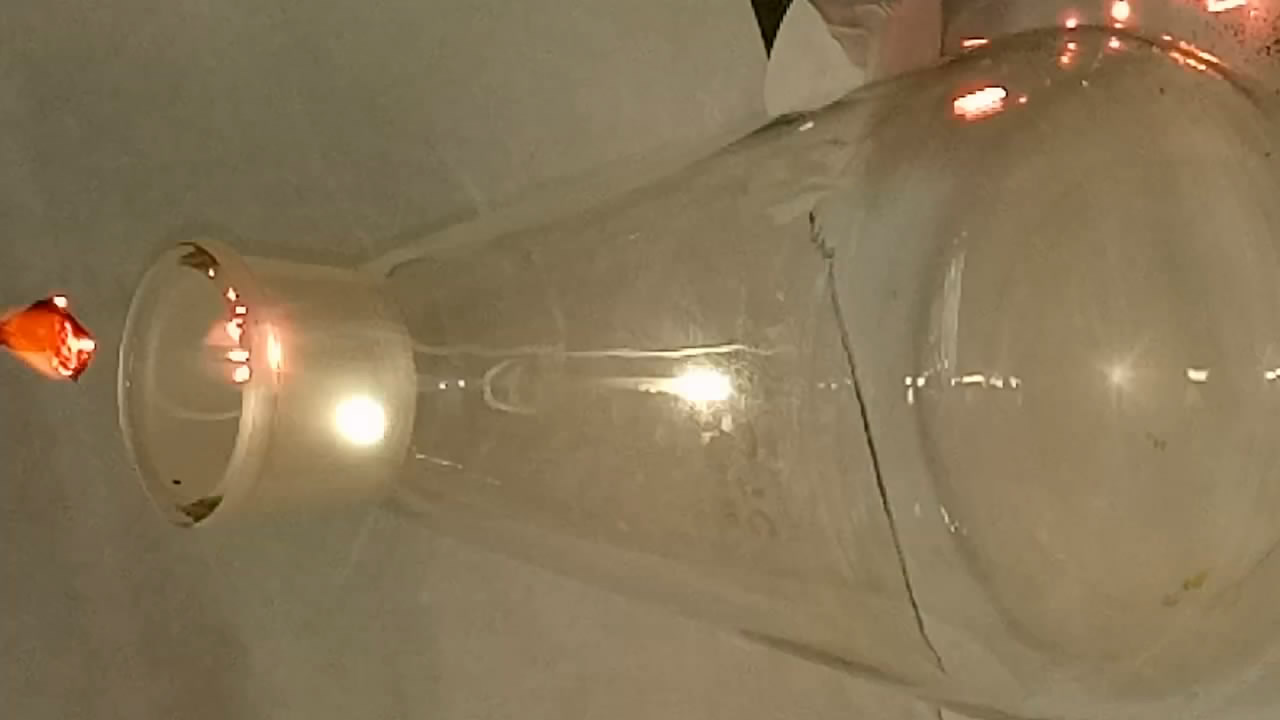
|

|

|

|

|

|

|

|

|

|

|

|

|