Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Задание 1 (15 баллов)
Твёрдое при комнатной температуре вещество А
содержит 50% (мол.) водорода. Оно не реагирует с водным раствором перманганата
калия, а при действии бихромата калия в 30% растворе серной кислоты
превращается только в кислоту Б, содержащую 58.5% углерода и 3.7% водорода.
Выделения газа при этом не наблюдается. При нагревании кислота Б плавится,
после чего теряет воду и образует вещество В. Если А обработать нитрующей
смесью при слабом нагревании, то среди многочисленных продуктов нитрования
преобладают 3 соединения (Г, Д и Е) в соотношении по массе 1:1:1, с трудом
поддающиеся разделению. Все эти соединения содержат 49,5% углерода, 3,1%
водорода и 14,4% азота. При окислении любого из этих трёх соединений кислым
раствором бихромата калия образуется только одно вещество - кислота Ж. Укажите
вещества А - Ж и напишите соответствующие превращения.Задание 2 (12 баллов)
При полной нейтрализации 200 мл соляной кислоты с
массовой долей 0,0352 (p=1036 кг/м3) раствором КОН выделилось 11,18 кДж
теплоты (условия стандартные). В реакции нейтрализации 500 мл 0,1 М уксусной
кислоты при тех же условиях выделилось 2,38 кДж.1) Определите молярную теплоту диссоциации воды. Ответ обоснуйте.
2) Предложите способ (теоретический или экспериментальный) определения молярной теплоты диссоциации воды.
3) Как меняется величина ионного произведения воды с ростом температуры.
Ответ обоснуйте.
Задание 3 (10 баллов)
Элемент Х образует множество кислородсодержащих кислот. Содержание (в
процентах по массе) калия, элемента Х и кислорода в калиевых солях некоторых из
них приведено в таблице:1) определите Х.
2)запишите молекулярные и графические формулы кислот, дайте их названия и названия солей, указанных в условии.
| Соль | К | Х | О |
| I | 44,8 | 17,8 | 36,8 |
| II | 49,4 | 19,6 | 30,4 |
| III | 30,7 | 24,4 | 44,1 |
| IV | 37,5 | 29,8 | 30,8 |
Задание 4 (8 баллов)
При взаимодействии 1,0000 г сложного эфира некоторой органической кислоты
с избытком раствора гидроксида натрия было получено 1,1356 г натриевой соли этой
кислоты.1) Установите формулу сложного эфира.
2) Составьте кинетическое уравнение и рассчитайте, во сколько раз увеличится скорость гидролиза эфира, если концентрацию эфира увеличить в 3 раза, а концентрацию щёлочи в 4 раза. Медленной и равновесной считать 1-ю стадию присоединения ОН к эфиру.
Задание 5 (5 баллов)
Неизвестный металл массой 4,8 г обработали избытком очень разбавленного
раствора азотной кислоты. К полученному раствору прибавили избыток раствора
щёлочи и нагрели, при этом выделилось 1,12 л газа (н.у.). Определите металл,
напишите уравнения реакций.Задание 6 (4 балла)
Осуществите следующие превращения: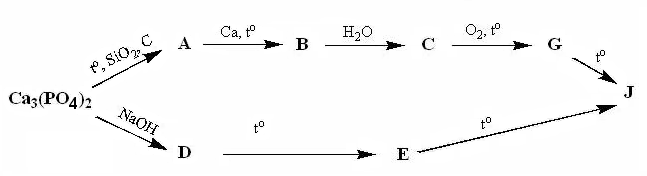
Химиков-Энтузиастов в разделе Олимпиада по Химии