Химия и Химики № 2 2017
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 2 2017 Журнал Химиков-Энтузиастов |
Воспламенение метанола под действием платинового катализатора - ч.4 Catalytic ignition of methanol on platinum catalyst Добрый Химик |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Воспламенение метанола под действием платинового катализатора (катализатор для анализа органического углерода)
Во второй и третьей части статьи мы приготовили самодельный платиновый катализатор и испытали, как он воспламеняет метиловый спирт. Для сравнения мы провели аналогичный опыт по каталитическому воспламенению метанола с использованием японского катализатора для анализатора органического углерода (т.е. катализатора промышленного изготовления). Согласно описанию производителя [ссылка] данный катализатор приготовлен на кварцевой вате и содержит 1% платины - т.е. он является аналогом приготовленного нами катализатора.
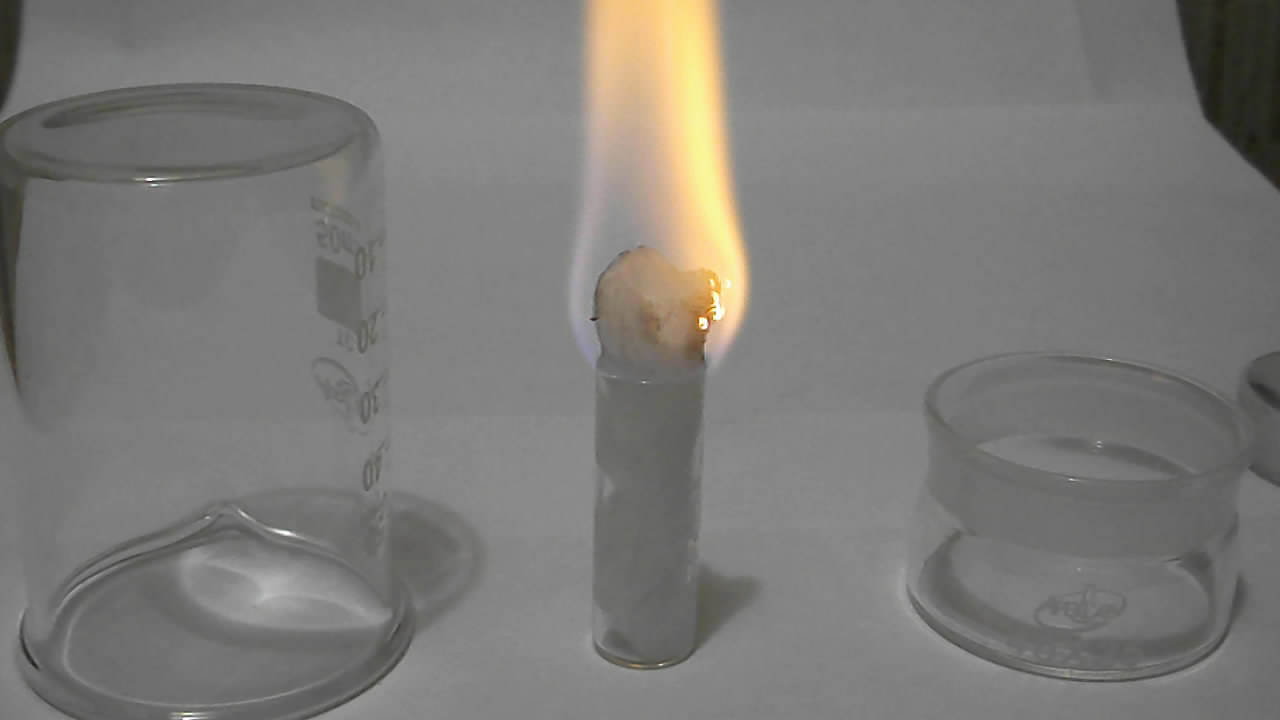
Catalytic ignition of methanol on platinum catalyst (catalyst for total organic carbon analysis) Техника эксперимента была аналогична предыдущей (см. ч.3). Ватка, пропитанная метиловым спиртом, находилась в стеклянном цилиндре. К ней приближали платиновый катализатор. От контакта с парами метилового спирта катализатор раскаялся, вата вскоре загоралась. Для успеха опыта желательно, чтобы в помещении было тепло (23-25°С и выше). Ватку со спиртом гасят, накрывая ее стеклянным стаканом. После чего стакан можно снять и повторить опыт. |

Воспламенение метанола под действием платинового катализатора (катализатор для анализа органического углерода) Catalytic ignition of methanol on platinum catalyst (catalyst for total organic carbon analysis) |

|

|

|

|

|

|

|

|

|

|
|

|

|

|

|

|

|

|

|
|
В наших экспериментах катализатор, приготовленный в промышленных условиях (1% платины), и самодельный катализатор (1.4% платины) показали себя одинаково хорошо. В обоих случаях носителем для платины была кварцевая вата.
Также мы приготовили катализатор, носителем в котором служил асбест. Содержание платины - 1-2%. При контакте с ватой, пропитанной метиловым спиртом, такой катализатор раскалялся, как уголь (по цвету), но спирт от него не загорелся. Зато водород воспламеняет. Обратите внимание, что успех опытов по самопроизвольному воспламенению зависит не только от активности катализатора, но и от ряда других факторов. Прежде всего - от температуры и от интенсивности потерь тепла из зоны реакции. Чем выше температура в лаборатории - тем больше шанс на успех. Но и это не все. Бумага, опавшие листья, угольная пыль и другие горючие материалы медленно окисляются кислородом воздуха даже при комнатной температуре (имеет место, как прямое окисление, так и окисление при участии микроорганизмов). В этой реакции выделяется тепло. Но, поскольку скорость реакции при комнатной температуре небольшая, тепло выделяется медленно и успевает рассеяться в окружающую среду. Зато, если бумага, листья или уголь лежат большой кучей, то тепло, которое вылепляется в ее недрах, не успевает рассеяться и идет на нагрев самой кучи. Выше температура - выше скорость окисления - быстрее выделяется тепло - выше температура - и т.д. В результате температура может подняться настолько, что горючий материал воспламениться. Особенно склонны к самовоспламенению кучи промасленных тряпок, а также - огромные кучи породы с угольной пылью возле шахт - терриконы. Другой пример. Небольшие кусочки металлического калия на воздухе обычно не загораются (могут, но не часто). Зато, если завернуть кусочек калия в хлопковую вату, он вскоре загорится. Вата - катализатор окисления металлического калия? - Конечно - нет. Дело в том, что слой ваты играет роль теплоизолятора. Вата мешает теплу, которое выделяется при самопроизвольном окислении калия, рассеиваться в окружающую среду [1]. Аналогично и с нашими опытами по самовоспламенению метанола с платиновым катализатором. Кроме активности самого катализатора, тут имеет значение: форма и размер катализатора, форма и размер ватки с метанолом, и то, насколько хороший контакт катализатора с парами спирта. - Т.е. важно все, что влияет на скорость выделения тепла реакции (чем эта скорость выше - тем лучше) и на скорость отвода тепла из зоны реакции (чем потери тепла меньше - тем лучше). Ниже на фотографии показаны (слева направо): асбест с платиной (катализатор), кварцевая вата с платиной (катализатор) и платинохлористоводородная кислота (50 мг, из которых потом приготовили катализатор - см. ч.2). __________________________________________________ 1 Подробнее - см: Плавление и горение калия. Самовоспламенение калия [ссылка] |

|