Бихромат калия, нитрат хрома (III) и яичный белок. Potassium dichromate, chromium (III) nitrate and egg white protein - Химия и Химики № 2 2017
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Бихромат калия, нитрат хрома (III) и яичный белок. Potassium dichromate, chromium (III) nitrate and egg white protein - Химия и Химики № 2 2017 Журнал Химиков-Энтузиастов |
Бихромат калия, нитрат хрома (III) и яичный белок ч.1, 2 Potassium dichromate, chromium (III) nitrate and egg white protein В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Бихромат калия и яичный белок. Potassium dichromate and egg white protein
Белок - основа жизни. Можно долго спорить о возможности небелковых форм жизни, но вся известная нам жизнь существует благодаря белкам. Основа жизни очень хрупкая. Белок неустойчив ко многим воздействиям. Например, к химическому воздействию. Растворенные белки денатурируют (коагулируют) при добавлении кислот, щелочей, спирта, солей тяжелых металлов и т.д. Это можно наглядно наблюдать, используя яичный белок или молоко. Такие эксперименты просты в исполнении и могут быть выполнены в самых неприспособленных условиях. В журнале уже были опыты с серной кислотой, азотной кислотой, сульфатом меди и спиртом, результат на лицо: белок сразу же сворачивался - образовывалась масса, похожая на жвачку (см. подборку статей Полимеры, Мономеры, Природные полимеры, Пластмассы, Природные вещества. Polymers, Monomers, Natural Polymers, Plastics, Natural products [ссылка]).
В этот раз решил проверить, как действуют на яичный белок соли хрома. Казалось бы, какая разница: сульфат меди или соли хрома - зачем проводить однотипные эксперименты? Дело в том, что соли хрома много лет использовали для дубления кож. Вспомните фразу "хромовые сапоги". Означала она не "сапоги, изготовленные из металлического хрома", а сапоги, сделанные из кожи, которую дубили с помощью солей хрома. Кстати, такие сапоги очень ценились - в стране кирзовых сапог. Для дубления кож использовали соли именно трехвалентного хрома, но я решил начать эксперимнеты с соли шестивалентного хрома - бихромата калия. Почему? Кроме всего прочего, бихроматы - хорошие окислители и канцерогены, так что факт их действия на биологические молекулы не вызывает сомнения. В стакан с яичным белком добавил насыщенный раствор бихромата калия, перемешал, и... Ничего не произошло. Жидкости просто смешались, а денатурации белка не наблюдалось! Подождал несколько минут - ничего. Для сравнения добавил в этот же стакан азотную кислоту. В результате белок моментально свернулся. Образовалась масса, которая напоминала оконную замазку. Таким образом, азотная кислота моментально коагулировала яичный белок, а насыщенный раствор бихромата калия - нет! Вспомните, что бихроматами пугают детей, что они - канцерогены. Бояться не стоит, но работать с соединениями шестивалентного хрома нужно осторожно: не допускайте попадания на кожу, а тем более - внутрь организма. Как мы только что убедились, не все яды моментально сворачивают белки, но это не уменьшает их опасность (точнее - увеличивает). Для дубления кож использовали соли трехвалентного хрома, не шестивалентного (чаще всего - хромокалиевые квасцы), может быть дело в этом? |

Бихромат калия Potassium dichromate |

Бихромат калия и яичный белок Potassium dichromate and egg white protein |

|

|

|

|

|

Денатурация белка отсутствует There is no denaturation of the protein |

Добавляем азотную кислоту Nitric acid is added |

Наблюдается быстрая денатурация белка There is fast denaturation of the protein |

|

|

|

|

|
|
Нитрат хрома (III) и яичный белок. Chromium (III) nitrate and egg white protein
Хромокалиевых квасцов под рукой не оказалось, можно было попросить у коллег, но нашел банку с нитратом хрома (III) - решил, что такая замена вполне эквивалентна. Кстати, банка оказалась старой: дата выпуска затерлась, но таких этикеток уже давным-давно не делают. Внутри банки были крупные фиолетовые кристаллы.
Приготовил в стаканчике насыщенный раствор нитрата хрома (III) [с осадком нерастворившейся соли], хорошо перемешал. Отделил яичный белок от желтка, поместил в другой стакан. Вылил раствор нитрата хрома в яичный белок, перемешал. Результат: жидкости просто смешались. И только через несколько минут я заметил, что в стакане образовались светлые волокна - белок начал частично коагулировать. Вскоре волокна стали похожи на скомканные пленки, их количество увеличилось, но основная часть белка так и не денатурировала. Подождал минут 10 - ничего не изменилось. Добавил для сравнения этанола - сразу же произошла денатурация белка, единственное, образовалась не "масса, похожая на жвачку" (как в прошлых опытах с кислотами), а серый гелеобразный осадок (который напоминал гидроксид алюминия). |

Нитрат хрома (III) и яичный белок Chromium (III) nitrate and egg white protein |

|

|

|

|

|

|

|

|

|
|

|

|

|

|

|

|

|

|

Добавляем спирт Ethanol is added |

Наблюдается быстрая денатурация белка There is fast denaturation of the protein |

|

|
|
Коллега провел аналогичный эксперимент с хромокалиевыми квасцами. При добавлении крепкого раствора хромокалиевых квасцов к белку сразу появляются "нити": белок частично сворачивается. Но при последующем добавлении, картина та же. Плотной массы не получается.
Прошло несколько минут (см. третье и четвертое фото ниже), и этот свернувшийся белок начал всплывать, но плотная масса все равно не образовалась. |

Хромокалиевые квасцы и яичный белок Chromium(III) potassium sulfate and egg white protein |

|

|

|
|
Другой коллега пояснил причину неудач. Согласно книге Аронина Ю.Н. - Технология выделки и крашения (1981) [ссылка] дубящим свойством обладают не сами по себе ионы хрома (III), а только их основные соли. Ни нитрат трехвалентного хрома, ни хромокалиевые квасцы (а тем более - бихромат) непосредственно для дубления не применяются.
Нужен или гидроксид хрома (его дубящая способность, в технологии - "основность", принята за 100%) или гидроксид-сульфат хрома (III) CrOHSO4 ("основность" - 33%). Для получения дубящего раствора из бихромата, его смешивают с концентрированной серной кислотой и каким-нибудь восстановителем (глюкоза). Приведем цитату: "В производстве все расчеты ведутся на содержание в растворе оксида хрома, т. е. в технологических картах указано, что для проведения дубления раствор должен содержать, например, 0.9 г/л оксида хрома Cr2О3 и иметь основность 40%. Растворы основных солей трехвалентного хрома обычно называют хромовыми солями, а их концентрированные растворы - хромовыми экстрактами. Для приготовления хромового экстракта в качестве исходных материалов берут калиевый или натриевый хромпик. Приготовление экстракта заключается в восстановлении шестивалентного хрома в трехвалентный. Реакция восстановления шестивалентного хрома может быть представлена так: Реакция восстановления проводится в кислой среде. Хромпик мелко раздробляют и растворяют в горячей воде. К полученному раствору медленно добавляют серную кислоту. Требуемое количество серной кислоты рассчитывают по формуле n = 133.3 - а, где n - количество 100%-ной серной кислоты на 100 мае. ч. хромпика; а - требуемая основность экстракта. Если, например, надо подсчитать, сколько требуется серной кислоты для приготовления хромового экстракта с основностью 30%, то n = 133.3-30=103.3 кг на 100 кг хромпика. После добавления серной кислоты к кислому раствору хромпика постепенно приливают при непрерывном перемешивании восстановитель (патоку, глюкозу и др.). Раствор сильно разогревается и вспенивается, при этом выделяется большое количество газов. В процессе восстановления хромпика окраска раствора меняется от красновато-оранжевой до зеленой, характерной для основных солей трехвалентного хрома. Готовность экстракта устанавливают по таким признакам: капля экстракта на белой фильтровальной бумаге имеет зеленый цвет; экстракт не должен окрашиваться в синий цвет при добавлении нескольких капель 10%-ного раствора крахмала; если образуется синяя окраска, реакция не закончена и восстановление надо продолжить. " Сейчас наравне с хромом при дублении используют соли циркония, алюминия и титана. Схема взаимодействия между хромом и белком при дублении кож показана ниже. |
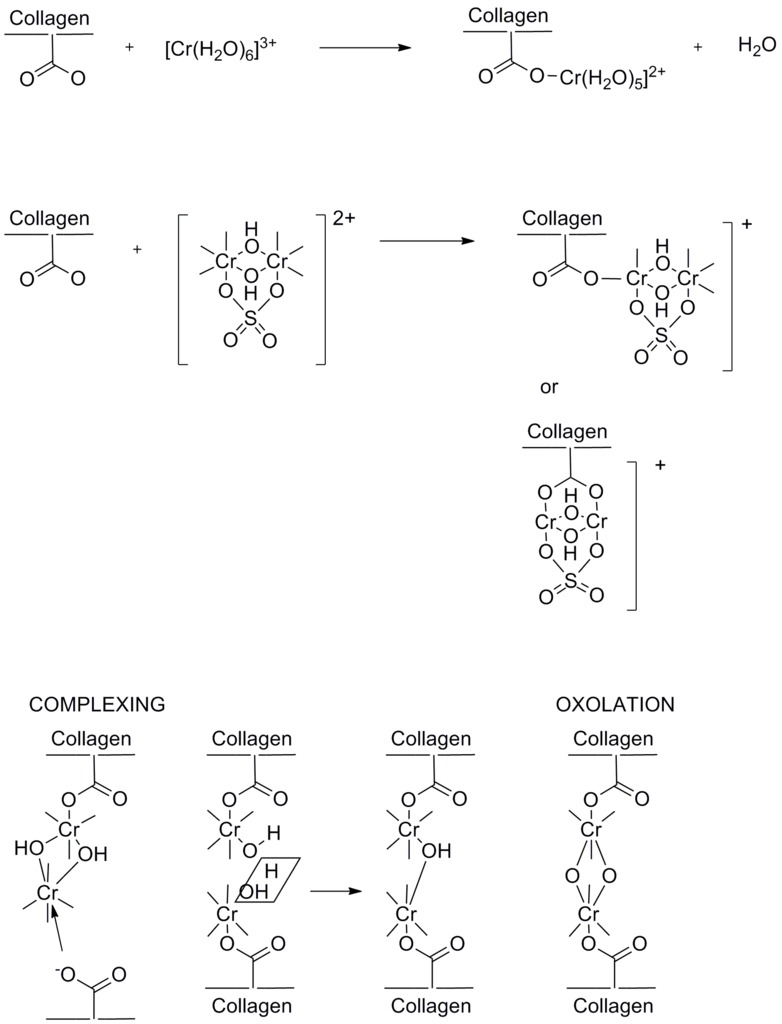
Механизм дубления кожи (белков) солями хрома Chemistry of chrome tanning |