Химия и Химики № 2 2022
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 2 2022 Журнал Химиков-Энтузиастов |
Танины (эксперименты) ч.8, 9 Tannins (experiments) В.М. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Галловая кислота и хлорид железа (III) / Gallic acid and iron(III) chloride
В прошлых частях статьи для проведения характерной реакции с хлоридом трехвалентного железа использовал настой кожуры граната и продажные танины (химический реактив). В этот раз решил провести данную реакцию с галловой кислотой (3,4,5-тригидроксибензойная кислота). Разумеется, ничего принципиально нового, но эксперимент простой (можно сказать - примитивный): почему бы не попробовать? Заодно можно проверить саму технику проведения демонстрационных химических опытов (с акцентом на первом слове), когда характерная окраска развивается постепенно - за счет того, что в сосуд с водой добавляют растворы обеих реагентов без перемешивания. Галловая кислота - представитель класса фенолокислот (т.е., карбоновых кислот, которые одновременно содержат карбоксильные -СООН и гидроксильные -ОН группы, связанные с бензольным кольцом). Пожалуй, наиболее известный представитель этого класса - салициловая кислота. 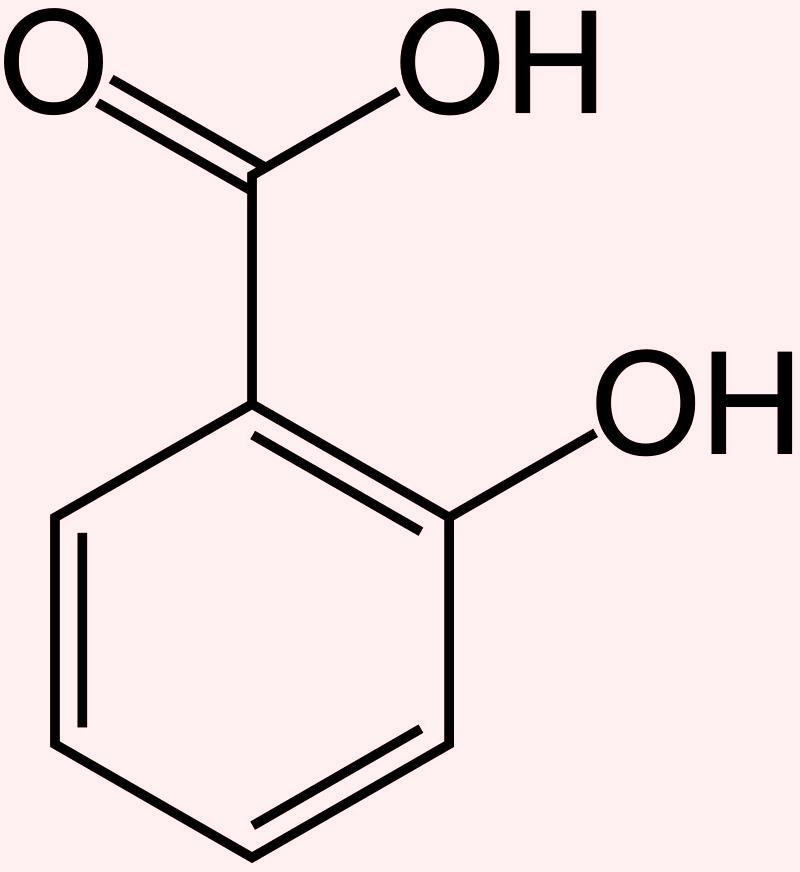
Салициловая кислота 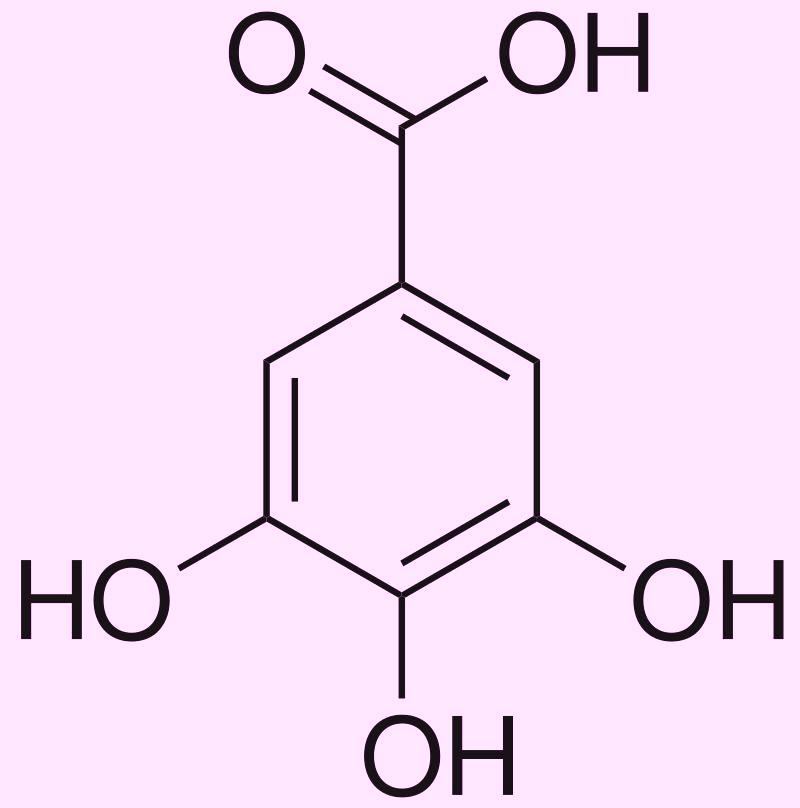
Галловая кислота Чернильные орешки (галлы) образуются на листьях дуба как результат жизнедеятельности насекомых-паразитов семейства орехотворок, внутри галлов развиваются их личинки. Английский вариант названия: oak apples - "дубовые яблоки". Галлы образуются не только на листьях дуба, но именно чернильные орешки - галлы на листьях дуба - наиболее известная разновидность галлов. Ниже показаны фотографии чернильных орешков, сделанные в одном из парков Киева. Часто такие орешки распределены не равномерно, а встречаются скоплениями (там - нет, а здесь - полно). |

Чернильные орешки |

|

|

|

|

|

|

|

|

|
|
В моем случае галловая кислота представляла собой легкий белый порошок. Взял 0.5 г галловой кислоты, попытался растворить в 20 мл дистиллированной воды. Полностью не растворилась. Посмотрел - галловая кислота слабо растворима в воде при комнатной температуре. Ничего - подойдет и суспензия.
Итак, в стакан с 300 мл воды (водопроводная) капнул 4 капли раствора хлорида железа (III), близкого к насыщенному. Потом капнул несколько капель суспензии галловой кислоты. На дне стакана постепенно стало формироваться темно-фиолетовое облако, которое состояло из множества нитей. Добавил больше галловой кислоты. Облако стало расти и расширяться. Перемешал - раствор моментально стал черным и непрозрачным. Дальше. Одна капля хлорида железа (III). Потом добавил примерно полмиллилитра галловой кислоты. Снова с задержкой возникло облако из темно-фиолетовых нитей. Добавил еще железа, перемешал. Результат - черный раствор. Следующий опыт. Капля хлорида железа, потом - капля суспензии галловой кислоты. Сперва - почти ничего (визуально). Потом твердые частички галловой кислоты опустились на дно стакана и дали там черную окраску. Перемешал - появилась темно-фиолетовая окраска. С экспериментами - все. Уже во время монтажа видео заметил интересную деталь. Второй опыт. Стакан с водой. Капаю хлорид трехвалентного железа. Когда капля опустилась на дно и рассеялась в воде, на дне стакана появилось несколько черных точек. Не заметил бы, если бы не знал куда смотреть. По-видимому, во время первого опыта к дну стакана пристало несколько частичек галловой кислоты, которые остались там после мытья стакана. Мелкие белые частички были незаметны - стакан казался чистым, но хлорид железа (III) их проявил. |

Галловая кислота и хлорид железа (III) |

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

Свертывание яичного белка суспензией галловой кислоты |

|

|

|

|

|

|

|

|

|

|

|

|

|
|
Теперь - небольшое дополнение к предыдущим разделам статьи по танинам. Оставил суспензию танинов над осадком. При стоянии на воздухе в растворе развивалась все более интенсивная коричневая окраска. Неудивительно, ведь танины - природные полифенолы, а полифенолы легко окисляются до хинонов, которые имеют коричневую окраску (даже под действием кислорода воздуха). Подобным образом, например, ведет себя гидрохинон.
Раствор галловой кислоты после 1 суток стояния над осадком приобрел желто-серый цвет. Тоже начал окисляться. Что будет дальше - не проверял (использовал его для эксперимента). Зато в растворе танинов при стоянии завелась плесень. Серо-зеленый грибок покрыл раствор толстым слоем. Это ведь не карамелька, а танины, которые обладают антисептическими свойствами! Вспомнил интересный факт: грибки съели високоактивный графит, выброшенный из реактора при аварии на Чернобыльской АЭС! Причем обычный графит "кушать" они не желали (слишком стойкий): для питания грибкам был нужен именно графит с радиационными дефектами, которые увеличивают его химическую активность. Позже вспомнил, что танины - не просто полифенолы: среди них есть гликозиды, т.е. - производные углеводов. А есть сахара - не такой и подвиг. На работе завариваю черный чай на дистиллированной воде. Уже привык к "стандартной окраске" чая, когда на одно и то же количество воды я добавляю примерно одинаковое количество заварки. Пару раз заварил чай на воде из-под крана: при прочих равных условиях окраска чая получилась заметно более интенсивной, чем на дистилляте. Для этого хватило щелочности солей, которые содержатся в водопроводной воде. Т.е., добавка щелочей усиливает окраску чая. Об этом я уже писал в пятой части статьи (Настой кожуры граната, аммиак и соляная кислота / Infusion of pomegranate peel, ammonia and hydrochloric acid [ссылка]). |

В растворе танинов (продажный реактив) выросла плесень |
Гумус и агрономы: взаимодействие гумата натрия с хлоридом железа (III) и протеином яйца Interaction of sodium humate with iron (III) chloride and egg protein В.М. Витер |
|
Когда я занимался экспериментами с танинами, коллега дал пакетик гумата натрия. Конечно, это не танины, более того, данный продукт - не химический реактив, а технический препарат - "стимулятор роста", т.е. содержать он мог что угодно. Тем не менее - решил поэкспериментировать, а именно - провести с гуматом натрия те же реакции, которые я провел с танинами: реакция с хлоридом трехвалентного железа (качественная реакция на фенольный гидроксил) и реакция сворачивания белка.
Дело в том, что гуминовые вещества можно рассматривать как более конденсированные аналоги танинов: они образуются при разложении отмерших растений, содержат бензольные ядра и целый ряд функциональных групп, в частности - гидрокисльных. Напомню, что сами танины можно рассматривать как продукты конденсации полифенолов, иногда - с добавлением других фрагментов, в частности - сахаров. Как и некоторые танины, гуминовые вещества содержат в молекуле фрагменты углеводов, а также - пептидов. Гуминовые вещества (подобно техническим препаратам танинов) имеют нерегулярный состав - представляют собой трудноразделимую или практически неразделимую смесь многих веществ, строение и содержание в смеси которых могут в широких пределах меняться. Технические препараты, которые продаются под названием "гумат" (натрия, калия, аммония), получают обработкой торфа или бурого угля щелочью. Тот препарат, который дал мне товарищ, был получен именно из бурого угля. Также сырьем для получения гуматов могут служить отходы целлюлозно-бумажных комбинатов. Гуматы рекламируют как чудо-удобрения и стимуляторы роста. А также гуматы можно использовать для детоксикации грунта. Позитивный эффект от их применения, по-видимому, имеет место, но есть и обратная сторона медали. Дело в том, что гуматы способны связывать и переводить в труднодоступную форму не только "страшные-токсичные тяжелые металлы", но и "микроэлементы", необходимые для роста и развития растений (часто это - одни и те же элементы: все дело в количестве). Аналогично ведут себя и танины. Поэтому важно не переборщить с количеством такого удобрения, а также вносить его только на определенных фазах развития растений. Коллега наблюдал действие гуматов на комнатные растения собственными глазами. Декану агрохимического факультета знакомые подарили мешок гумата натрия. Он сказал методистам, чтобы они полили ним растения, которые стояли в деканате. Залили гумат водой, полученной вытяжкой полили вазоны. Результат - растения начали погибать. Декан сказал: - Вы слишком много поливаете, уменьшить количество гумата на половину! Методисты для виду согласились, но пошли к моему коллеге: он был в числе немногих здесь химиков. - Чем, чем вы их полили?! Гуматом натрия?! Так он же из бурого угля: растениям от него может стать "нехорошо". Выкопайте растения, хорошо отмойте водой корни и пересадите в свежую землю. Так и сделали. Растения отошли и поправились. Через время декан строил: - Сколько вы даете гумата натрия? - Все, как вы сказали! - Так и продолжайте. "Агрохимики" - пусть название не вводит читателей в заблуждение. Между ними и химиками общего не больше, чем между гумусом и гуманизмом (или гумусом и гуманитариями). Теоретически агрохимия - наука, а на практике уровень факультета агрохимии был ниже детского сада. Если результаты экспериментов не вписывались в теорию начальства - их подделывали: здесь это было железным правилом. А часто - вообще не делали экспериментов, а просто "рисовали" результаты - даже не удосуживаясь это скрывать. Если у нас - химиков, не сделав анализ, ты не можешь знать, получилось ли у тебя целевое соединение (а, если да, то достаточно ли оно чистое)? То у агрохимиков - проще. Одна аспирантка заявила мне прямым текстом: - Ты наперед должен знать, что у тебя получится! [В будущем эксперименте]. Одно хорошо, агрохимикам выдают диплом по специальности "агроном", а не химик. Зато настоящие агрономы (кафедра генетики и физиологии растений) их даже агрономами не считают. Итак, эксперименты. Реакция на фенольный гидроксил [с хлоридом железа (III)]. В частности, в эту реакцию вступают: фенол, салициловая кислота, сульфосалициловая кислота, танины и... аспирин. Казалось бы, ацетилсалициловая кислота - аспирин давать окраску с хлоридом железа (III) не должна (в молекуле нет фенольного гидроксила), но в моем случае давала, т.к. она содержала примесь салициловой кислоты. По фармакопее подобное не допускается, но контроль сейчас практически нулевой. Для экспериментов взял 4.44 г гуматанатрия и залил 15 мл воды.Оставил стоять на сутки, периодически перемешивая. Получился темно-коричневый (почти черный) раствор с осадком. В стакан с 300 мл воды капнул 1 каплю раствора гумата натрия. Получился красивый каскад вихревых колец. Разумеется, целью эксперимента были не вихревые кольца - содержимое перемешал, добавил 1 каплю раствора хлорида железа (III) (близкого к насыщенному). Перемешал, ожидал появления темной окраски (черной или фиолетовой), но раствор так и остался бесцветным (сильное разведение). Добавлял новые порции хлорида железа и гумата натрия - все больше, перемешивал. В результате раствор стал, сначала желтым, потом - коричневым: цвет исходных веществ. Т.е., если и образовался комплекс (а должен), то его цвет визуально не отличался от окраски исходных реагентов. При увеличении количества реагентов в растворе появились бурые хлопья, которые напоминали гидроксид трехвалентного железа. Может, гумат натрия имеет слишком щелочную реакцию? Напрямую попробовать индикаторной бумажкой раствор гумата натрия было проблематично - он почти черный [1], фильтровать - не стал, а проверил индикаторной бумагой реакцию раствора в стакане (куда я добавил гумат и хлорид трехвалентного железа). Реакция оказалась кислой. Т.е., цветной реакции между гуматом натрия и хлоридом железа (III) не получилось. __________________________________________________ 1 Можно было слегка вмочить бумажку в темный раствор, вынуть и подождать, пока фронт жидкости на полоске бумаги разделится: прозрачная жидкость опередит темную суспензию. |

|

Гумат натрия |

Вода, гумат натрия и хлорид железа (III) |

В сильно разбавленных растворах образование окрашенного комплекса замечено не было |

|

|

В более крепких растворах наблюдалась коричневая окраска, неотличимая от окраски исходных веществ (а также - от окраски гидроксида трехвалентного железа) |

|

|

|
|
Остаток раствора гумата натрия использовал для эксперимента по сворачиванию яичного белка. Белок яйца поместил в стакан и добавил раствор гумата натрия - свертывания белка не произошло. В растворе, правда, обнаружилось какое-то полужидкое прозрачное образование, но оно было и в исходном яичном белке. Если добавляемое вещество сворачивало яичный белок (серная кислота, например), то в растворе появлялись хлопья, а данное образование становилось, словно резиновым, но в данном эксперименте этого не наблюдалось.
|

Действие гумата натрия на яичный белок: коагуляция не отмечена |

|

|

|

|

|
|
Вот такой он гумус: и воспоминания неприятные, и эксперимент не получился. Пусть агрономы ним и занимаются.
|

|
Взаимодействие с хлоридом железа (III) - качественная реакция на фенолы: флуоресцеин, эозин, фенолфталеин, ионол Interaction with iron (III) chloride - qualitative reaction for determination of phenols: fluorescein, eosin, phenolphthalein, butylated hydroxytoluene В.М. Витер |
|
Качественная реакция с хлоридом железа (III) - известный метод обнаружения веществ, которые содержат в своем составе фенольный гидроксил, например, фенола, салициловой кислоты, сульфосалициловой кислоты, танинов. Основана на образовании фенолами окрашенных комплексов с катионом трехвалентного железа. В нашем журнале подобные эксперименты были описаны неоднократно.
Решил провести реакцию на фенольный гидроксил с немного "нетипичными" веществами - которые содержат в своей молекуле фенольный гидроксил, но описание их реакции с хлоридом железа (III) я не встречал. Подобрал такой перечень: флуоресцеин, эозин, фенолфталеин и ионол (бутилгидрокситолуол). |
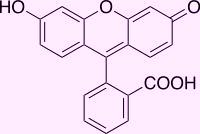
Флуоресцеин |
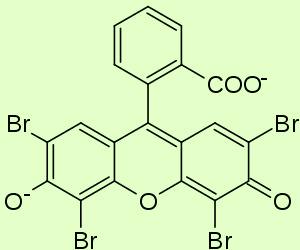
Эозин Y |
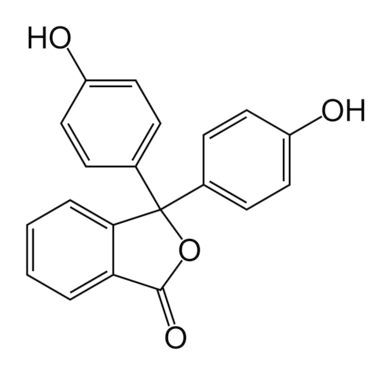
Фенолфталеин |
-4-methylphenol.jpg)
Ионол (бутилгидрокситолуол) |
|
Флуоресцеин и эозин - известные флуоресцентные красители: дают яркую окраску, заметную при мизерной концентрации красителя. Фенолфталеин - один из самых распространенных кислотно-основных индикаторов, раньше использовался в качестве слабительного средства, но потом был изгнан из аптек. Ионол (бутилгидрокситолуол) - известный антиоксидант (антиокислитель), используется, как в промышленности, так и в лабораторной практике. Как можно видеть из структурных формул, все данные вещества содержат фенольный гидроксил в молекуле. Почему же в практикумах по аналитической (или органической) химии не описаны их реакции с хлоридом железа (III)? Ведь вещества доступные, а эксперименты исключительно простые. Возможных причин две:
1. Вещества не взаимодействуют с хлоридом железа (III); 2. Вещества реагируют с хлоридом железа (III), но без образования яркоокрашенного комплекса (как вариант - окраска этого комплекса неотличима от окраски исходных веществ). Дополнительный фактор: флуоресцеин (натриевая соль) и эозин растворимы в воде, а для фенолфталеина и особенно - ионола реакцию нужно проводить в среде спирта (в воде они растворимы плохо). Начал с флуоресцеина. Стакан с 300 мл воды (водопроводной). Вмочил спичку в раствор флуоресцеина (натриевая соль), потом - в воду. Пленки жидкости на поверхности дерева хватило, чтобы с двух раз предать содержимому стакана четкий зеленый оттенок. Стоило бы посмотреть, как раствор светиться в ультрафиолетовых лучах, но не в этот раз - сейчас стоит другая задача. Добавил в стакан несколько капель раствора флуоресцеина - жидкость приобрела яркую желто-зеленую окраску с отчетливой флуоресценцией. Теперь добавил несколько капель раствора хлорида железа (III) (близкого к насыщенному) - флуоресценция сильно ослабла, но новая окраска (которую нельзя объяснить смешением цветов) не появилась. Повторил эксперимент, в этот раз добавил в воду флуоресцеина гораздо больше. Флуоресценция сосредоточилась в основном в верхнем слое раствора (лампа расположена сверху, в более глубокие слои раствора возбуждающий свет проникал слабо). Добавил хлорид трехвалентного железа, перемешал. Результат: коричневый раствор (цвет хлорида железа (III)), верхний слой флуоресцирует. Т.е. по цвету раствора нельзя утверждать, что образовался комплекс. |

Добавим в воду флуоресцеин |

|

Теперь добавим хлорид железа (III) |

|
|
Эозин. Несколько капель в тот же стакан воды на 300 мл - интенсивно-зеленый цвет, яркая флуоресценция. Добавил хлорид железа (III), перемешал. Флуоресценция исчезла, цвет раствора - как у хлорида железа (III). Опять окрашенный комплекс не зафиксирован.
|

Добавим в воду эозин |

|

Теперь добавим хлорид железа (III) |

|
|
Фенолфталеин. Хорошо растворим в спирте и плохо в воде, если добавить к воде спиртовый раствор фенолфталеина - растворенное вещество выделится в твердую фазу, образуя белую суспензию. Чтобы этого не произошло - решил провести реакцию в спирте. Налил в небольшой стаканчик спирт, добавил каплю водного раствора хлорида железа (III) и перемешал - появилась коричневая окраска, потом - добавил спиртовый раствор фенолфталеина: окраска практически не изменилась (если не считать эффекта разбавления).
Аналогично произошло и с ионолом. Зато, когда вылил содержимое стакана в раковину, - получил фиолетовую окраску. Дело в том, что перед этим я вылил в раковину недопитый чай (содержит танины). Таким образом, со всем исследуемыми веществами фенольной природы: флуоресцеин, эозин, фенолфталеин и ионол (бутилгидрокситолуол) не удалось зафиксировать образование окрашенных комплексов с хлоридом трехвалентного железа. Остается констатировать, что отрицательный результат - тоже результат. |

К спирту добавим 1-2 капли раствора хлорида железа (III) |

|

Теперь добавим спиртовый раствор фенолфталеина (или ионола) |