Chemistry and Chemists № 2 2025
Journal of Chemists-Enthusiasts
| Content | Chemistry experiments - video | Physics experiments - video | Home Page - Chemistry and Chemists |
|
Chemistry and Chemists № 2 2025 Journal of Chemists-Enthusiasts |
Experiments with Nitrocellulose - pt.10, 11 Chemist |
|
Having noticed a mistake in the text, allocate it and press Ctrl-Enter
Fire on Hand (Combustion of Nitrocellulose Film) - Part 10
During previous experiments, I needed an organic dye to color an artificial "amoeba." Instead of a dye, a colleague suggested using a varnish designed to protect against corrosion. Later, he realized this idea was inappropriate - we didn't even know the approximate composition of the varnish. In an effort to help, he brought a commercial nitrocellulose varnish, hoping it might be useful for experiments involving nitrocellulose.
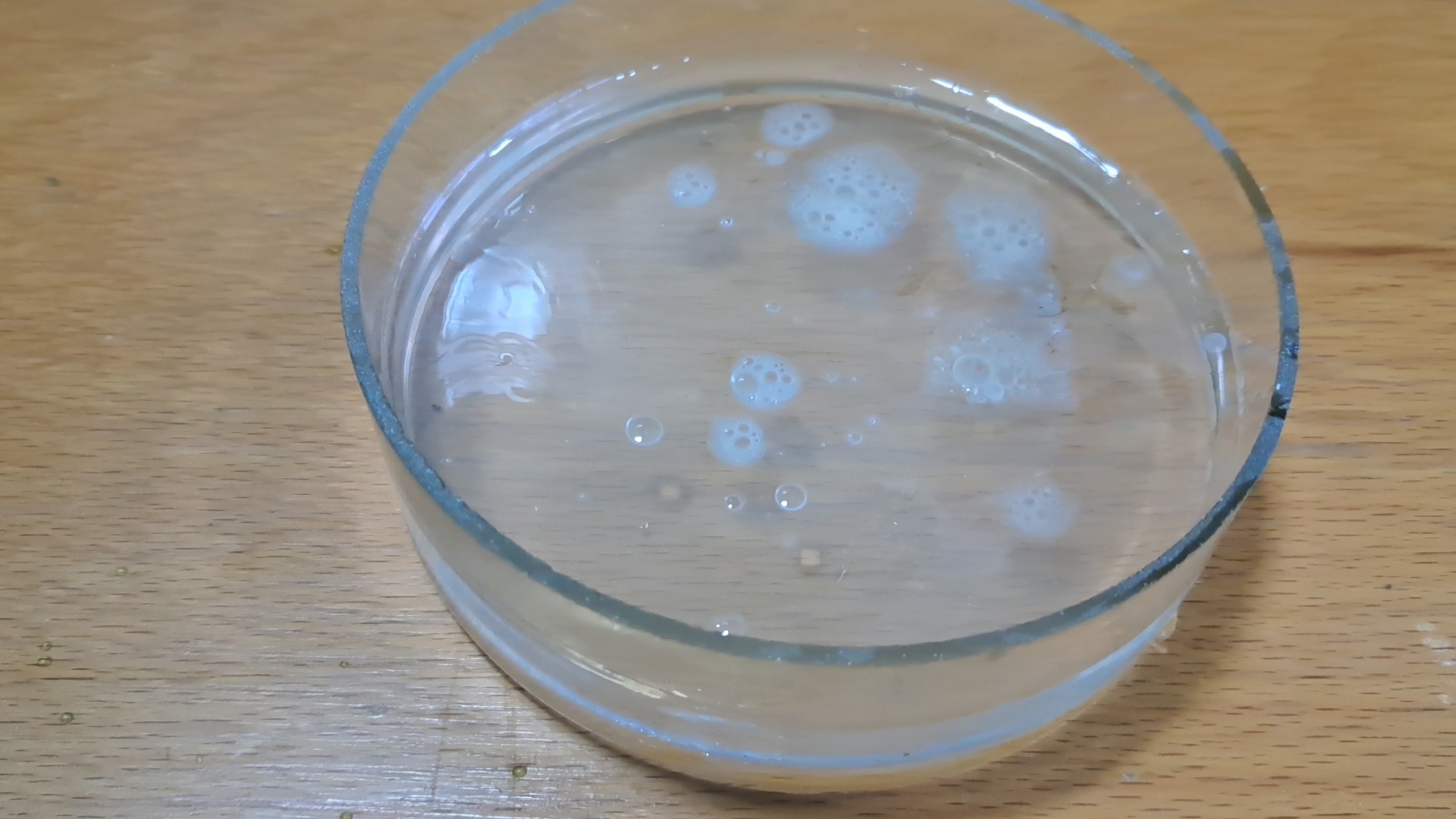
Огонь на ладони (горение нитроцеллюлозной пленки) - часть 10 The exact composition of this varnish was also unknown, but it could reasonably be assumed to contain nitrocellulose, a solvent, a plasticizer, and various additives. It was primarily intended for coating wooden furniture. I decided to use this varnish to attempt imitating the "amoeba." I poured water into a Petri dish and dropped varnish onto it. Upon hitting the water's surface, some drops retained their compact structure for several seconds before spreading out, while others immediately spread, forming a thin film. Eventually, a varnish film developed on the surface of the water. However, no moving objects resembling an ''amoeba'' were observed. The solvent contained in the varnish clearly did not mix with the water, so it did not pass from the varnish into the water and, consequently, did not form jets. This solvent might have been composed of hydrocarbons. I waited until the solvent evaporated, leaving a nitrocellulose film on the surface of the water. I then carefully removed the solid film from the Petri dish and placed it in a thermostat to dry. Why did I need a nitrocellulose film? To set it on fire on my palm. Experiments where substances or mixtures are burned on the hand without causing burns are some of the most visually striking chemical demonstrations. There are many variations of such experiments. For instance, soap foam filled with methane or hydrogen can be burned on the palm, creating a dramatic yet harmless flame. Small quantities of certain organic peroxides, such as HMTD or acetone peroxide, are also used for this purpose. However, handling organic peroxides is risky, as they can explode and cause serious injuries. This danger doesn't deter some chemists. Occasionally, liquid mixtures like trichloromethane with hexane are used for similar demonstrations, though these are not entirely harmless. A safer alternative for demonstrating flames on the palm is nitrated cotton wool. Ordinary cotton wool is treated with a mixture of concentrated sulfuric and nitric acids (a nitrating mixture) to convert the cellulose into nitrocellulose while retaining its fibrous structure. This modified cotton burns with a brief yellow flash that causes little to no harm. Of course, sulfuric and nitric acids are not always readily available. Even if they are on hand, the nitration process is far from pleasant. That's why I decided to replace fibrous nitrocellulose (made from cotton wool) with a nitrocellulose film. The first attempt was only partially successful: I didn't sustain a burn, but the experience was painful. The problem was that the film was too thick. The nitrocellulose film that formed when the varnish evaporated on the water's surface was even thicker than the one I had used in the earlier experiment. If set on fire on the palm, such a thick film would inevitably cause burns. To demonstrate this, I burned the film on a sheet of paper. After the nitrocellulose burned away, it was evident that the paper had burned through in several places and continued to smolder. For combustion on the palm of the hand, the nitrocellulose film must be thin enough to burn quickly without causing harm. To create such a film, I decided to use a solution of smokeless powder in low-quality acetone. I prepared a solution with a viscosity low enough to spread evenly over the surface of the water without collecting into drops. After pouring water into a Petri dish, I added the nitrocellulose solution onto its surface. The solution formed a film that spread across the water. As the solvent gradually evaporated, a thin, solid nitrocellulose film formed. When I tried to separate the nitrocellulose film from the water, it stuck together and tore. However, this did not interfere with the experiment. I dried the film at room temperature and then burned it on my palm. There was a brief yellow flash, and I felt neither heat nor pain. At the time, the laboratory temperature was only 5°C. During the flame experiment, my hands were shaking from the cold, so I had to carefully choose the moment to avoid capturing the trembling on video. Otherwise, viewers might mistakenly think the experimenter was scared, implying the experiment was dangerous. To produce a larger amount of nitrocellulose film, I poured water into a plate with a much larger surface area than the Petri dish. I added the nitrocellulose solution to the water, forming a thin film on the surface. I left it for a day to allow the solvent to evaporate, then carefully poured off the water, leaving the solid film on the plate. I placed the plate in a thermostat set at 80°C to dry. After three hours, I discovered that the film had adhered to the surface of the plate — a behavior I had never observed before. Normally, a wet nitrocellulose film, once dried, easily separates from solid surfaces. Using a spatula to remove pieces of the film, I realized the nature of the force binding it to the plate: electrostatic attraction. The pieces of nitrocellulose film clung not only to the plate but also to the spatula, my hands, the table, my clothes, and other objects. This strong electrostatic attraction was reminiscent of how small particles of fluoroplastic-4 (Teflon) behave. The intense electrification of the nitrocellulose particles was particularly unusual given the conditions. For surfaces to become highly electrified, both the air and the surfaces themselves must be dry. However, the laboratory was cold and humid; visible vapor escaped with every breath. Normally, electrostatic charges do not accumulate on damp surfaces because moisture increases electrical conductivity, allowing charges to dissipate. How could this contradiction be explained? The answer lay in the thermostat. The nitrocellulose film was removed while it was still hot and completely dry, so it had not yet absorbed moisture from the air. This unexpected behavior of nitrocellulose provided an excellent opportunity to experiment with electrostatic charges [1]. However, my primary focus remained on the combustion experiments. With some effort, I collected the pieces of nitrocellulose film on my palm and ignited them. A yellow flash occurred, and again, I felt no heat or pain. In a third attempt, I used a larger volume of a more viscous nitrocellulose solution. This resulted in a thicker film. Anticipating difficulties, I separated the solid film from the plate while it was still wet. After it dried, I hesitated: was the film too thick to burn safely on my palm? Despite my doubts, I decided to take the risk. As before, the nitrocellulose burned quickly without causing harm or discomfort. __________________________________________________ 1 After 24 hours in the humid laboratory, the remaining pieces of nitrocellulose film were no longer attracted to nearby surfaces. После 24 часов пребывания во влажной лаборатории, оставшиеся кусочки нитроцеллюлозной пленки перестали притягиваться к окружающим поверхностям. |
|
Огонь на ладони (горение нитроцеллюлозной пленки) - часть 10
Во время прошлых экспериментов понадобился органический краситель, чтобы окрасить искусственную "амебу". Вместо органического красителя коллега предложил лак, предназначенный для защиты от коррозии. Позже коллега осознал, что его идея была неуместной - даже ориентировочный состав лака мы не знаем. Пытаясь помочь, коллега принес продажный нитроцеллюлозный лак - в надежде, что он пригодиться для экспериментов с нитроцеллюлозой.
Состав данного лака также был неизвестен, но можно было предположить, что он содержит нитроцеллюлозу, растворитель, пластификатор и другие добавки. Лак предназначался для покрытия деревянной мебели. Я решил использовать данный лак для имитации "амебы". В чашку Петри налил воды и капнул в нее лак. Попав на поверхность воды, некоторые капли сохраняли компактную структуру на протяжении нескольких секунд, потом растекались. Другие капли сразу же растеклись по поверхности, образуя тонкую пленку. В результате поверх воды образовалась пленка лака. Никакого подобия движущихся "амеб" не наблюдалось. Растворитель, входящий в состав лака, явно не смешивался с водой и не переходил из лака в воду. Следовательно, "реактивных джетов" не образовывалось. Например, это могли быть углеводороды. Подождал, пока растворитель испарится и на поверхности воды останется нитроцеллюлозная пленка. Извлек твердую пленку из чашки Петри, поместил в термостат сушиться. Зачем мне была нужна пленка из нитроцеллюлозы? Чтобы поджечь ее на ладони. Эксперименты, в которых вы сжигаете на руке вещество или смесь веществ, но не обжигаетесь, являются одними из самых эффектных химических демонстраций. Вариантов таких экспериментов много. Например, на ладони сжигают мыльную пену, наполненную не воздухом, но метаном или водородом. Также для этой цели используют небольшие количества некоторых органических перекисей - ГМТД или перекиси ацетона. Органические перекиси опасны в обращении, их взрыв может причинить серьезные травмы, но некоторых химиков это не останавливает. Иногда для этой цели используют смеси жидкостей, которые не всегда безвредны (например, смесь трихлорметана с гексаном). Более безопасным вариантом продемонстрировать пламя на ладони является нитрованная вата. Хлопковую вату помещают в смесь концентрированной серной кислоты с концентрированной азотной кислотой (нитрующая смесь). В результате целлюлоза переходит в нитроцеллюлозу, а ее волокнистая структура сохраняется. Такая модифицированная вата может сгорать на ладони, давая желтую вспышку, которая не причиняет существенного вреда. Разумеется, серная и азотная кислоты доступны не всегда. Даже, если они есть под рукой, процесс нитрования не принадлежит к числу приятных операций. Поэтому я и пытался заменить волокнистую нитроцеллюлозу (вату) нитроцеллюлозной пленкой. Первый эксперимент прошел не совсем удачно: ожога я не получил, но было больно. Причина состояла в том, что пленка была слишком толстой. Нитроцеллюлозная пленка, которая образовалась при испарении лака на поверхности воды, была еще толще, чем в упомянутом эксперименте. При попытке ее поджечь на ладони, ожоги будут неизбежны. Чтобы продемонстрировать это, сжег данную пленку на листе бумаги. После прекращения горения нитроцеллюлозы стало видно, что бумага прогорела в нескольких местах и продолжила тлеть. Для сжигания на ладони нитроцеллюлозная пленка должна быть достаточно тонкой, чтобы она сгорала быстро, не успев причинить вред. Для получения такой пленки решил использовать раствор бездымного пороха в некачественном ацетоне. Приготовил раствор с вязкостью достаточно низкой, чтобы он растекался по поверхности воды, не собираясь в капли. Налил в чашку Петри воды и вылил на ее поверхность раствор нитроцеллюлозы. Пленка раствора растеклась по поверхности воды. Растворитель постепенно испарился, образовалась тонкая твердая пленка. При попытке отделить пленку нитроцеллюлозы от поверхности воды она слипалась и рвалась. Впрочем, это не помешало эксперименту. Высушил пленку при комнатной температуре и сжег ее на ладони. Произошла желтая вспышка, я не почувствовал ни тепла, ни боли. Более того, в лаборатории было 5°С, поэтому во время эксперимента с пламенем руки дрожали от холода - пришлось выбрать момент, чтобы дрожь не попала на видео. В противном случае зритель мог решить, что экспериментатору страшно, следовательно, эксперимент представляет опасность. Чтобы увеличить количество нитроцеллюлозной пленки, налил воду в тарелку, которая имела гораздо большую поверхность, чем чашка Петри. Добавил в воду раствор нитроцеллюлозы в некачественном ацетоне. Поверх воды образовалась тонкая пленка раствора. Оставил на сутки, чтобы испарился растворитель. Затем аккуратно слил воду, чтобы твердая пленка осталась в тарелке. Поставил тарелку сушиться в термостат при 80°С. Через три часа оказалось, что пленка пристала к поверхности тарелки. Раньше я такого не наблюдал. Мокрая пленка нитроцеллюлозы после высыхания хорошо отделялась от твердых поверхностей. Отделив несколько кусочков пленки при помощи шпателя, я понял природу силы, которая притягивала пленку к поверхности тарелки. Более того, кусочки пленки также приставали к шпателю, рукам, столу, одежде и различным предметам. Причиной было электростатическое притяжение! Кусочки нитроцеллюлозы были сильно наэлектризованы, поэтому притягивались к окружающим поверхностям. Подобным образом ведут себя мелкие частицы фторопласта-4 (тефлон). Такая сильная электризация частиц нитроцеллюлозы выглядела крайне необычно. Дело в том, что для электризации поверхностей необходимо, чтобы воздух и сами поверхности были сухими. Однако, в помещении было холодно, а потому очень влажно. При дыхании изо рта шел пар. На влажной поверхности электростатические заряды обычно не накапливаются, поскольку вода увеличивает электропроводность, и заряды рассеиваются. Как объяснить это противоречие? Дело в том, что я вынул нитроцеллюлозу из горячего термостата: она была сухой и еще не успела поглотить влагу. Появилась хорошая возможность провести эксперименты с электростатическими зарядами, однако сейчас цель была другой - эксперименты с горением [1]. С большими трудностями собрал кусочки нитроцеллюлозной пленки на ладони и поднес к ним пламя. Произошла желтая вспышка. Ни тепла, ни боли я не почувствовал. В третий раз я поступил аналогично второму разу, только использовал больший объем более вязкого раствора нитроцеллюлозы. В результате пленка получилась толще. Помня проблемы, я отделил твердую пленку от тарелки, пока она была еще мокрой. После сушки я сомневался: стоит ли сжигать такую пленку на ладони? Не слишком ли много нитроцеллюлозы? Все-таки рискнул. Как и в прошлый раз нитроцеллюлоза сгорела, не причинив вреда и не вызвав неприятных ощущений. |

Fire on Hand (Combustion of Nitrocellulose Film) |

|

|

|
|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|