Chemistry and Chemists № 2 2025
Journal of Chemists-Enthusiasts
| Content | Chemistry experiments - video | Physics experiments - video | Home Page - Chemistry and Chemists |
|
Chemistry and Chemists № 2 2025 Journal of Chemists-Enthusiasts |
Working with Tritium - p.1, 2 Chemist |
|
Having noticed a mistake in the text, allocate it and press Ctrl-Enter
Distillation of Tritiated Water (HTO) and Other Lab Adventures - Part 1
In our chemical laboratory, we study compounds that exhibit interesting properties… Well, I'll tell you more about that some other time. For now, I'll just note that the main focus of our lab is applied research, so it's unlikely that we'll produce any groundbreaking scientific papers based on our primary work. Nevertheless, we are required to publish articles for reporting purposes. As a result, in addition to our main tasks, we carry out various side experiments that allow us to generate publishable results.
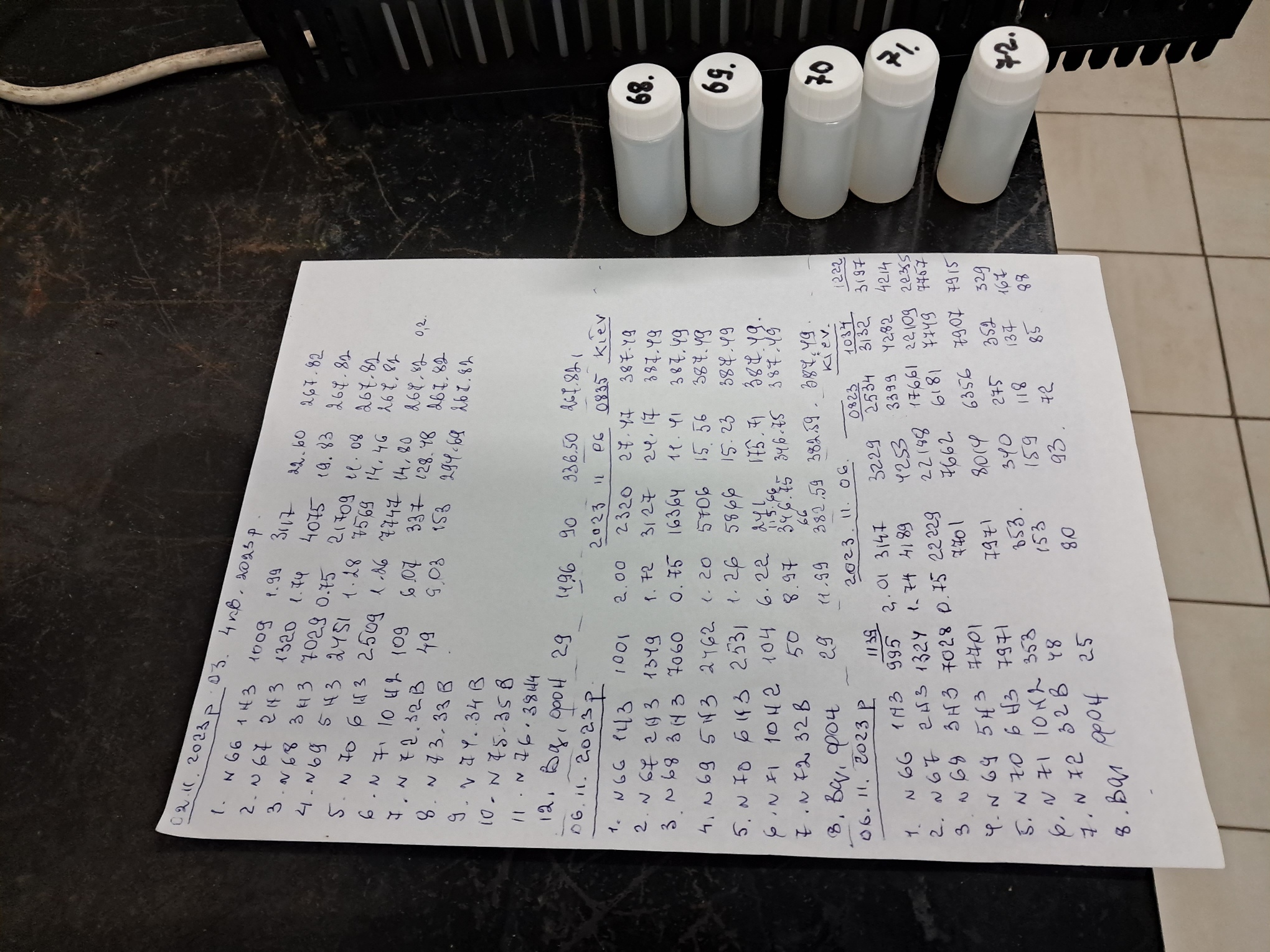
Работа с тритием Перегонка тритиевой воды (HTO) и другие лабораторные приключения - часть 1 One such side topic is the study of hydrogen isotope exchange: protium, deuterium, and tritium. Unlike deuterium and protium, tritium is weakly radioactive, which makes it easier to detect and track its movement in both natural and artificial systems. Instead of a mass spectrometer, you can use liquid scintillation analyzers, such as the Tri-Carb or Quantulus. From the very beginning, tritiated water (T2O) samples must be distilled. I write "T2O", although in reality the tritium content in our water samples is extremely low. In fact, these are just regular water samples - H2O - with added deuterium oxide (D2O) and only trace amounts of tritiated water (T2O). Pure tritium water is so radioactive that it would instantly evaporate, heated by the energy released from its own radioactive decay. Thus, the samples consist mainly of protium water (H2O), a few percent deuterium water in the form of HDO [1], and trace amounts of HTO. For example, the activity of the samples shown in the photographs was about 10000 Bq/L, whereas the tritium limit in drinking water is 30000 Bq/L - three times higher. In other countries, the allowable limits are much stricter, but our national standard is relatively high, apparently due to the Chornobyl nuclear power plant accident. Before determining the tritium content, the water samples had to be distilled with a small amount of potassium permanganate added. Potassium permanganate oxidizes organic substances in the sample, converting all hydrogen (protium, deuterium, and tritium) contained in those substances into water. We also added a few zeolite granules to the distillation flask to ensure even boiling. Samples of tritium water used to be distilled in another room, but that room is currently under renovation, so a colleague asked me to carry out the distillation in the room where I work. He brought over a condenser, adapters, distillation flasks, and flexible water hoses. He also brought two adjustable stands - one for a heating device and the other for the receiving flask. Instead of using an electric hotplate, my colleague brought a soldering pot filled with sand to heat the distillation flask. When I asked, "Wouldn't it be better to use a hotplate?" he replied: "No! The hotplate overheats the flask! The distilled samples get contaminated." Why is overheating the distillation flask undesirable? When too much heat is applied, the liquid boils violently and unevenly. This leads to "bumping" - portions of the liquid are thrown up into the condenser without vaporization and re-condensation. At best, small splashes of the original liquid can contaminate the distillate; at worst, large quantities of undistilled liquid may reach the receiving flask. As a result, the distillate becomes impure. My colleague claimed that the soldering pot provided gentler, more even heating, allowing for moderate boiling. However, to distill just two small flasks, he usually spent an entire day. Since we had nine samples to process, it looked like distillation would take five days at that rate. I assembled the apparatus in the center of the fume hood, connected the hoses to the condenser, and turned on the water. Then I switched on the soldering bath. After inspecting the setup, I realized: I only had one fume hood, and there were many other tasks to perform. Distillation was just one of them. So, I moved the distillation setup to the right side of the hood to free up space. As a result, access to the screw that adjusts the height of the stand holding the soldering pot was blocked. To fix this, I rotated the stand - while the soldering pot was still turned on. The wall of the soldering pot accidentally touched a nearby gas tap. Suddenly, a large blue spark flashed, there was a sharp crackling sound, and the soldering pot shut off. This tap was once connected to a natural gas supply via an iron pipe, but the gas had been turned off years ago. A rubber hose with a Teclu burner had still been attached to the pipe. Since the lab no longer used natural gas and there were no plans to restore it, I had removed the hose earlier that day, exposing the iron gas tap. I did this just before assembling the distillation setup, thinking it would save space. If I hadn't cut the hose, the incident wouldn't have occurred. The cause of the accident was clear: the gas pipe had acted as a ground loop. Apparently, the electrical insulation in the soldering pot had been damaged - there was a "live-to-housing short circuit," and the pot burned out when it touched the metal tap. But how serious was the breakdown? I removed the fuse - the central wire had vanished; it had melted and splashed along the inner walls. The fuse had blown. In the best case, only the fuse had burned out. In the worst case, something more critical had failed. Unfortunately, I didn't have a spare fuse. I told my colleague. He suggested: "Try shorting the fuse contacts, insert the fuse, and measure the resistance of the device." So, I wrapped the fuse in aluminum foil, reinserted it, and measured the resistance of the soldering pot - there was no continuity. That meant the fuse wasn't the only casualty. I had no choice but to use the electric hotplate - the very one my colleague had insisted was "absolutely unsuitable for distillation." I poured the first sample into the flask, added potassium permanganate (until an intense purple color appeared), and dropped in several zeolite granules. I connected the flask to the distillation apparatus and began heating. To my surprise, the water boiled gently and evenly. The heating was easily adjustable. Despite my colleague's warning, the hotplate worked well. In addition to oxidizing organic substances, the potassium permanganate also served another purpose: it acted as a visual indicator. Permanganate solutions are deeply colored. If even a small portion of the liquid from the distillation flask splashes into the receiver, the distillate turns pink - a clear sign that the distillation must be repeated. In our case, the distillate remained colorless. Still, the first portion must always be discarded to rinse the system. For this run, my colleague and I agreed that discarding 1 mL would suffice. After that, the receiving vessel was replaced and the purified sample was collected. When only a small volume of liquid remained in the distillation flask, I stopped the heating. You should never distill to dryness - this risks contaminating the distillate. I left 1-3 mL of liquid in each flask. It would have been better to leave more, but the sample volumes were limited. In the end, I managed to distill all nine samples in just half a working day. I disassembled the apparatus, turned off the condenser water, and washed the flasks. Then I moved on to other tasks... … and three days later, I discovered that the neighboring table was flooded. Where did the water come from? There were no visible hoses or water lines nearby. It turned out the leak was from the water-jet pump - more specifically, from the hose used to draw air into the pump. There are only two water taps in our laboratory. One is permanently connected to the water-jet pump, which is firmly attached to the pipe. That left just one tap for all other needs. To save space, I had connected the water supply to the condenser through the outlet pipe of the water-jet pump - the hose that drains water from the pump into the sink. When I finished the distillation, I closed the tap supplying water to the pump - and thus, also to the condenser. The outlet hose from the condenser stopped flowing, and I assumed the system was fully shut off. But I overlooked one thing: a small amount of water still continued to flow from the tap. This water didn’t pass through the pump and the condenser, but instead seeped through the pump’s side branch — the one used for drawing in air. The water followed the path of least resistance. First, it filled the trap - a 3-liter flask - and then overflowed onto the table. I didn't notice until three days later. The leak was slow, but by that time, a fair amount of water had accumulated and some had reached the floor. I was afraid the water might have seeped into the labs below. But luckily - this time - nothing happened. __________________________________________________ 1 Let me clarify to avoid confusion with the formulas. We added pure deuterium water (D2O) to the system, but due to the large excess of H2O, the D2O almost completely converts to HDO: D2O + H2O = 2HDO Tritium was initially present in the form of HTO, since protium is in large excess. I used the formula "T2O" for simplicity. Уточню, чтобы не было путаницы с формулами. Мы добавляли в систему чистую дейтериевую воду D2O, но в избытке H2O дейтериевая вода почти полностью переходит в HDO. D2O + H2O = 2HDO Тритиевая вода изначально была в форме HTO, поскольку протий находится в огромном избытке. Формулу "T2O" я употребил для упрощения. |
|
Работа с тритием
В нашей химической лаборатории мы исследуем вещества, которые проявляют интересные свойства... Впрочем, об этом я расскажу вам как-нибудь в другой раз. Отмечу только, что основное направление работы лаборатории - прикладное, поэтому по ее итогам вряд ли удастся написать стоящие внимания научные статьи. А публиковать статьи требуют от нас для отчетности. Следовательно, кроме основной работы приходится ставить разные побочные эксперименты, чтобы по их результатам можно было писать научные статьи.
Перегонка тритиевой воды (HTO) и другие лабораторные приключения - часть 1 Одна из таких побочных тем - исследование обмена изотопов водорода: протия, дейтерия и трития. В отличие от дейтерия и протия, тритий обладает слабой радиоактивностью, что упрощает его определение и позволяет легко отслеживать миграцию трития в природных и искусственных системах. Вместо масс-спектрометра можно использовать жидкостные сцинтилляционные анализаторы, например, TriCarb, Quantulus и другие. С самого начала пробы тритиевой воды T2O необходимо перегнать. Я пишу "T2O", хотя на самом деле содержание трития в наших пробах воды мизерное. Реально, пробы представляют собой "обычную" воду - H2O, которая содержит добавку дейтериевой воды D2O и лишь следовые количества тритиевой воды T2O. Чистая тритиевая вода T2O насколько радиоактивна, что такая вода моментально бы испарилась, нагретая теплом собственного радиоактивного распада. Таким образом, пробы содержат преимущественно протиевую воду H2O, несколько процентов дейтериевой воды в форме HDO [1] и мизерные количества HTO. Например, активность образцов, показанных на фотографиях, составляла примерно 10000Bq/l, в то время как норма содержания трития в питьевой воде составляет 30000Bq/l - в три раза выше. В других странах ограничения содержания трития в питьевой воде гораздо строже, но у нас норма высокая, по-видимому, это связано с аварией на Чернобыльской АЭС. Перед проведением определения трития образцы воды необходимо было перегнать с добавкой небольшого количества перманганата калия. Перманганат калия окисляет органические вещества, содержащиеся в пробе, переводя в воду весь водород (протий, дейтерий, тритий), который содержится в этих веществах. Также в перегонную колбу мы добавляем несколько гранул цеолита для обеспечения равномерного кипения. Образцы тритиевой воды раньше перегонялись в другой комнате, но сейчас там ремонт, поэтому коллега попросил меня провести перегонку в комнате, где я работаю. Он принес холодильник, насадки, перегонные колбы и гибкие трубки для подачи воды в холодильник. Также принес два подставки с регулируемой высотой - под электрическую плитку и колбу-приемник, соответственно. Вместо электрической плиты для нагрева перегонной колбы товарищ принес паяльную ванну (solder pot), заполненную песком. На мой вопрос: "Не лучше ли использовать электрическую плитку?" товарищ ответил: - Нет! Плитка греет слишком сильно! Перегнанные образцы загрязняются. Почему слишком сильный нагрев перегонной колбы нежелателен? Если подвод тепла слишком интенсивный, перегоняемая жидкость кипит бурно и неравномерно. Бурное кипение приводит к "забрасыванию" части жидкости из перегонной колбы в холодильник, откуда она стекает в приемник, минуя процесс испарения - конденсации ("проброс"). В лучшем случае в перегнанный образец могут попасть брызги исходной жидкости, в худшем случае в приемнике могут оказаться большие порции не перегнанной жидкости. В результате такой перегонки дистиллят получается загрязненным. Коллега утверждал, что паяльная ванна нагревает колбы слабее, обеспечивая умеренное и равномерное кипение. Правда, чтобы перегнать две крохотные колбочки, коллега тратил целый день. Образцов было девять, поэтому такими темпами перегонка образцов должна была занять пять дней. Я собрал перегонную установку по центру вытяжного шкафа, подсоединил к холодильнику шланги, включил воду. Включил паяльную ванну. Затем посмотрел на установку и решил - вытяжной шкаф у меня один, а разных работ предстоит много. Перегонка была только одной из них. Поэтому сместил перегонную установку в правый край вытяжки. В результате исчез доступ к винту, который регулировал высоту подставки для паяльной ванны (нагреватель для перегонной колбы). Чтобы устранить проблему, развернул подставку. Напомню, ванна была включена. Стенка ванны коснулась газового крана - неожиданно появилась большая синяя искра, послышался резкий звук электрического разряда, и паяльная ванна перестала работать. Раньше по железной трубе с краном подавался природный газ, но газ много лет назад отключили. К трубе был присоединен резиновый шланг с подключенной к нему горелкой Теклю. Поскольку природного газа в лаборатории не было и не предвиделось, я срезал шланг, оголив железный кран. Сделал я это как раз перед сбором установки с целью экономии места. Не срежь я шланг, описанной неприятности не произошло бы. Причина аварии была понятна: газовая труба выступила в качестве контура заземления. Очевидно, в паяльной ванне была нарушена электрическая изоляция - произошел "пробой фазы на корпус" и при контакте с краном ванна перегорела. Но насколько серьезной была поломка? Вынимаю плавкий предохранитель - центральная проволочка исчезла: она расплавилась и разбрызгалась по стенкам. Предохранитель перегорел. В лучшем случае перегорел только предохранитель, в худшем случае могло перегореть также что-то более важное. Запасного предохранителя у меня не было. Рассказываю коллеге. Он отвечает: - Попробуй замкнуть контакты предохранителя, вставить предохранитель и измерить сопротивление прибора. Обмотал предохранитель алюминиевой фольгой, вставил. Проверяю сопротивление паяльной ванны - контакт отсутствует. Значит, кроме предохранителя перегорело что-то еще. Пришлось использовать электрическую плитку, которая, по словам коллеги, "абсолютно не походит для перегонки". Налил в колбочку первую пробу, добавил перманганат (до появления интенсивной фиолетовой окраски) и несколько гранул цеолита. Присоединил колбу к перегонной установке, начал нагрев. Я был приятно удивлен, убедившись, что вода кипела равномерно и с умеренной скоростью, а интенсивность нагрева легко регулировалась. Кроме окисления органических веществ, перманганат калия играет еще одну роль. Растворы перманганата интенсивно окрашены. Перманганат служит визуальным индикатором. Если хоть небольшая порция жидкости из перегонной колбы попадет (забрасывается) в приемник, то перегнанная жидкость окрашивается в розовый цвет. Это означает, что дистиллят необходимо перегнать повторно. В нашем случае дистиллят получился бесцветным. Все равно первые порции дистиллята необходимо отбросить (промывка установки). В конкретном случае мы с коллегой решили, что для промывки хватит 1 мл дистиллята. После этого приемник меняют и ведут сбор перегнанной пробы. Когда в перегонной колбе остается определенное количество жидкости, перегонку прекращают. Перегонять пробу до полного испарения жидкости ("досуха") не следует, поскольку это может привести к загрязнению дистиллята. Я оставлял в перегонных колбочках по 1-3 мл жидкости. Следовало бы оставлять больше жидкости, но объем проб был ограничен. В результате я перегнал девять проб всего за половину рабочего дня. Разобрал установку, перекрыл воду, которая подавалась на холодильник. Вымыл колбы. Потом занялся другими работами... ... а через три дня обнаружил, что соседний стол был залит водой. Откуда взялась вода? Поблизости не было труб или шлангов с водой. Оказалось, что вода натекла... из водоструйного насоса, точнее - из шланга, по которому в водоструйный насос засасывается воздух. Водопроводных кранов в лаборатории всего два, один из кранов занят водоструйным насосом, который прочно прикреплен к трубе. Для всех остальных потребностей составился только один водопроводный кран. Поэтому я решил подключить подачу воды в холодильник сквозь выходной патрубок водоструйного насоса (через него вода из насоса стекает в раковину). Закончив перегонку, я закрыл кран, который подвал воду в насос, а через него - в холодильник. Вода из выходного шланга холодильника перестала течь - я решил, что поток воды был полностью перекрыт. Однако, небольшое количество воды все-таки продолжало вытекать из крана. Только текла вода не через насос и холодильник, а через боковой патрубок насоса, предназначенный для засасывания воздуха. Вода медленно потекла по пути наименьшего сопротивления. Сначала она заполнила ловушку - трехлитровую колбу, - затем потекла на стол. Заметил я это только через три дня. Поток был очень слабый, но воды накопилось изрядное количество, и часть ее уже успела стечь на пол. Я боялся, что вода протечет сквозь пол в расположенные ниже лаборатории. К счастью, на этот раз обошлось. |

Distillation of Tritiated Water (HTO) |

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

Tritium Determination |

|

|

|

The scintillator |

|

The scintillator |

|

|

|

|

|

|

The error message |
The error message |
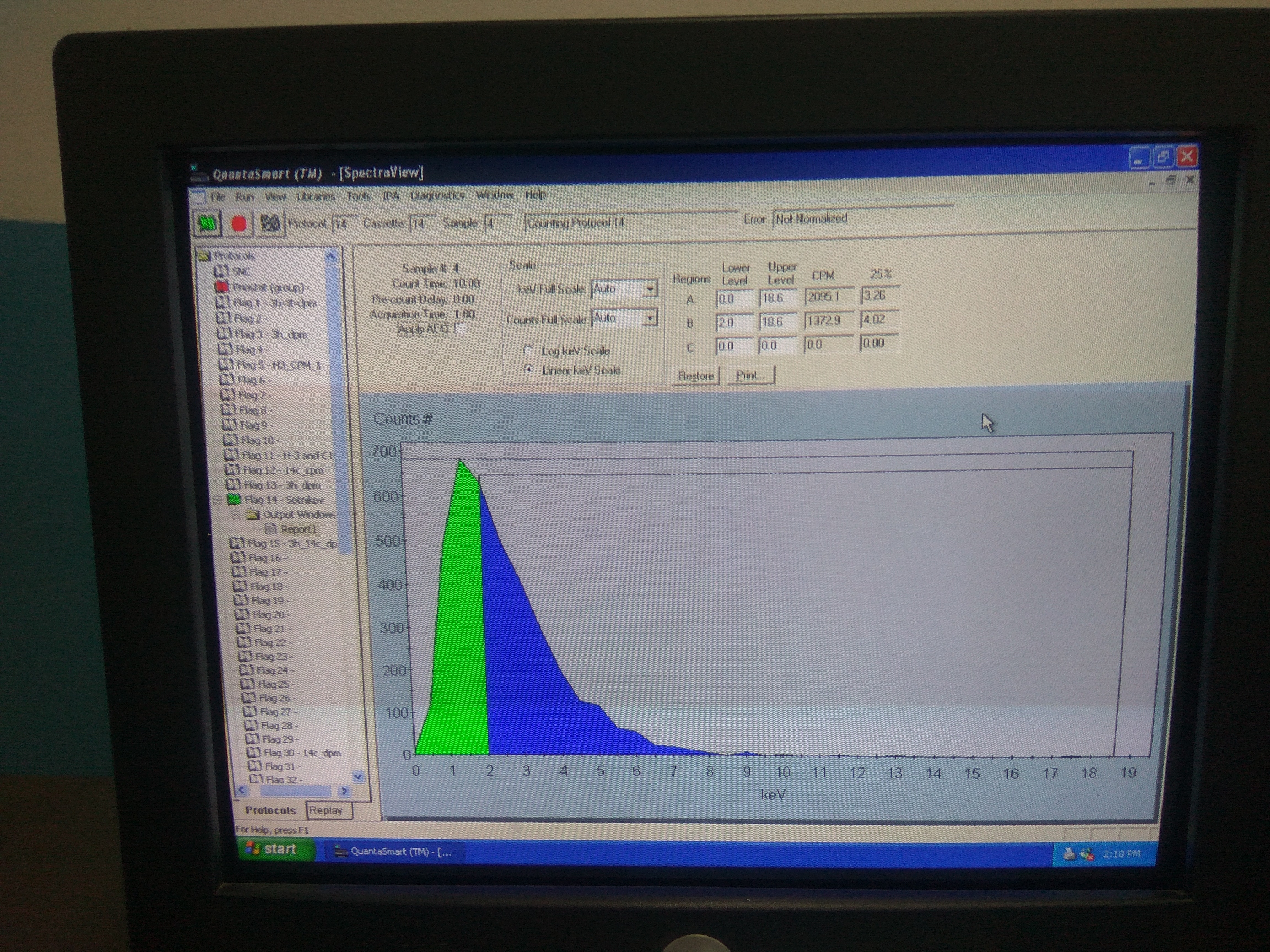
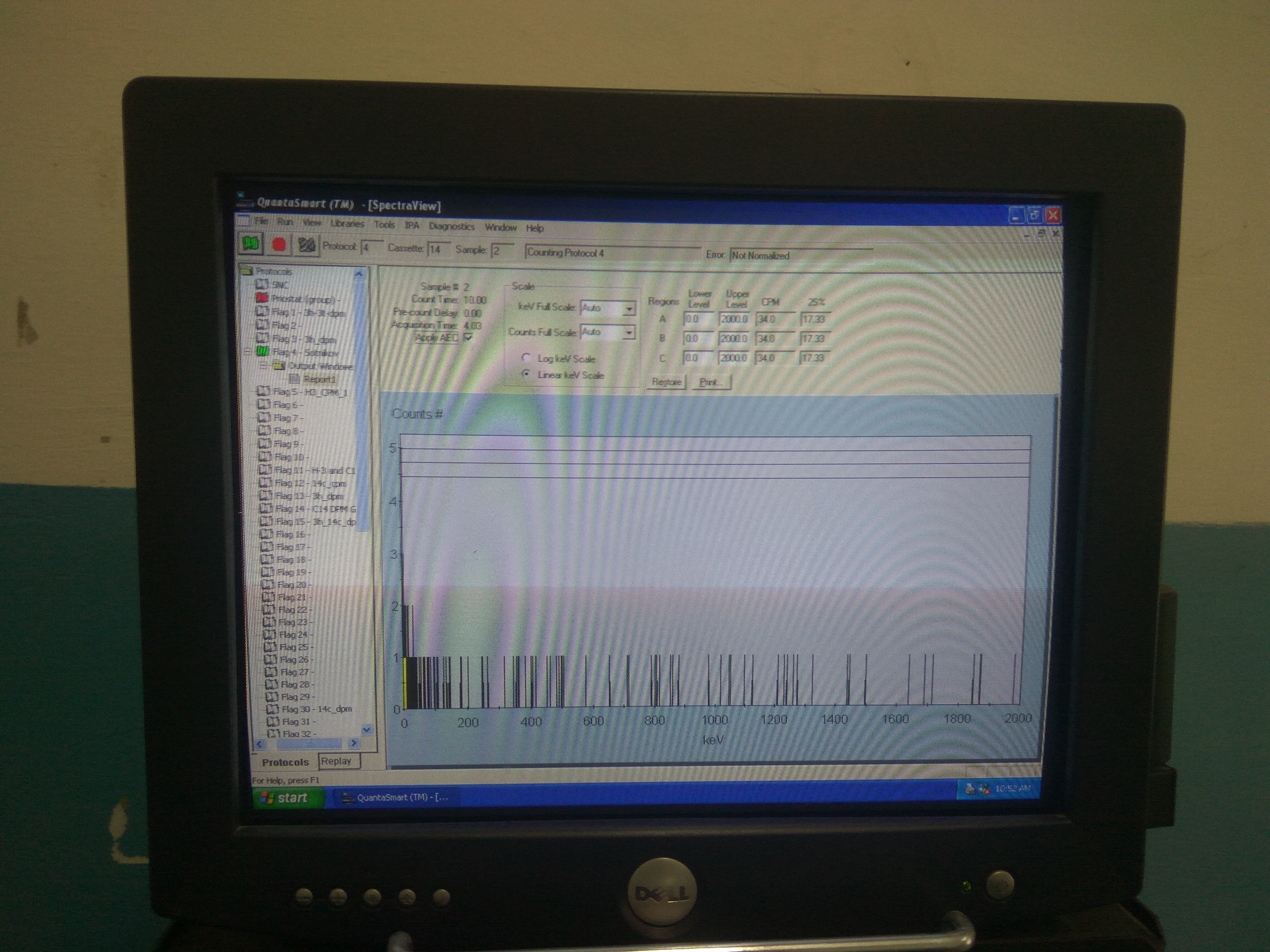
Let's start the measurement |

|

|

|

|
|

|

|

|

|

|
|
|
|

|

|

|

|

|

|

|

Potassium permanganate |

|

|

|

These mushrooms were picked up in a so-called "contaminated area" where radioactive waste was stored. Nevertheless, the employees were going to eat them |

|

|

|

|

|

|

|

|

|

|