Нетрудно догадаться, что, металлический аммоний, как и его окись - только вымысел автора (сюжет рассказа весьма оригинален), однако амальгама аммония может быть получена, правда существует она лишь в течение очень короткого времени.
Вот как описывает этот опыт талантливый популяризатор науки Гастон Тисандье в своей книге Научные развлечения (1885 г) ссылка
" Начнем, например, с описания одного интересного опыта, который обыкновенно демонстрируют на лекциях по химии.
Газ аммиак при соединении с элементами воды становится по свойствам похожим на металлическую окись, с металлическим радикалом аммоний. Заключить о существовании этого сложного гипотетического металла можно из того, что он в соединении с ртутью дает амальгаму.
Берут фарфоровую ступку и, налив туда небольшое количество ртути, кладут в эту последнюю маленькую свежеотрезанную пластинку натрия, причем растирают все это пестиком до тех пор, пока не послышится треск, сопровождаемый пламенем, - признак того, что ртуть и натрий вступили между собой в соединение и составили натриевую амальгаму. Положим теперь полученное соединение в стеклянную трубку, заключающую концентрированный раствор хлорида аммония или нашатыря в воде. Тогда ртуть начинает сильно пучиться и, в виде обильной массы металлического теста, выбрасывается из конца трубки (рис. 157). По сделанному нами предположению, аммоний, радикал аммиачных солей, в данном случае составляет со ртутью амальгаму, заняв место натрия.
Но соединение аммония со ртутью непрочно, и оно не замедлит разложиться на составные газообразные части - аммиак и водород, ртуть же снова примет свой обыкновенный вид. "
Использованная в книге терминология значительно отличается от современной (например, амальгамы теперь называют не соединениями, а сплавами - растворами металлов или аммония в ртути). Однако это ни в коей мере не свидетельствует о недостоверности описания.


Приведем цитату из более поздней книги В.Н. Верховский Техника и методика химического эксперимента в школе ссылка:
В ступку наливают около 7 мл ртути, затем от куска натрия, очищенного от корки, отрезают кубик со сторонами около 1-1.5 см (правила обращения с натрием!)
От приготовленного кубика натрия отрезаются кусочки величиной с горошину или немного больше и погружаются один за другим в налитую в ступку ртуть (при помощи щипцов, со всеми предосторожностями, указанными в т.1).
Полученная амальгама переливается в склянку, которая хорошо закрывается пробкой.
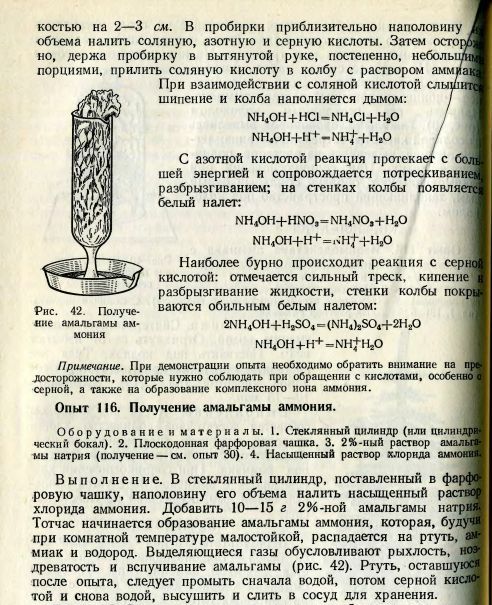
Опыт. Поместить приготовленную амальгаму в бокал или стакан (слоем в 2-3 см) и налить насыщенный раствор нашатыря NH4Cl, для чего растворить при нагревании около 40 г NH4Cl в 100 мл воды и дать остыть. Амальгама начинает пузыриться и подниматься до краев сосуда и выше (поэтому лучше поставить сосуд в чашку); затем постепенно снова опадает.
По окончанию урока оставшуюся после опыта ртуть промыть водой, разбавленным раствором азотной или серной кислоты и снова водой.
При лабораторном опыте можно выдать учащимся пробирки с уже готовой амальгамой натрия. "

Вот как описывает этот опыт талантливый популяризатор науки Гастон Тисандье в своей книге Научные развлечения (1885 г) ссылка
" Начнем, например, с описания одного интересного опыта, который обыкновенно демонстрируют на лекциях по химии.
Газ аммиак при соединении с элементами воды становится по свойствам похожим на металлическую окись, с металлическим радикалом аммоний. Заключить о существовании этого сложного гипотетического металла можно из того, что он в соединении с ртутью дает амальгаму.
Берут фарфоровую ступку и, налив туда небольшое количество ртути, кладут в эту последнюю маленькую свежеотрезанную пластинку натрия, причем растирают все это пестиком до тех пор, пока не послышится треск, сопровождаемый пламенем, - признак того, что ртуть и натрий вступили между собой в соединение и составили натриевую амальгаму. Положим теперь полученное соединение в стеклянную трубку, заключающую концентрированный раствор хлорида аммония или нашатыря в воде. Тогда ртуть начинает сильно пучиться и, в виде обильной массы металлического теста, выбрасывается из конца трубки (рис. 157). По сделанному нами предположению, аммоний, радикал аммиачных солей, в данном случае составляет со ртутью амальгаму, заняв место натрия.
Но соединение аммония со ртутью непрочно, и оно не замедлит разложиться на составные газообразные части - аммиак и водород, ртуть же снова примет свой обыкновенный вид. "
Использованная в книге терминология значительно отличается от современной (например, амальгамы теперь называют не соединениями, а сплавами - растворами металлов или аммония в ртути). Однако это ни в коей мере не свидетельствует о недостоверности описания.


Приведем цитату из более поздней книги В.Н. Верховский Техника и методика химического эксперимента в школе ссылка:
" Амальгама аммония
Для опыта нужна амальгама натрия, содержащая на 100 г (около 7.5 мл) ртути 1-2 г натрия. Приготовляется амальгама (до урока или на уроке) в фарфоровой ступке.
В ступку наливают около 7 мл ртути, затем от куска натрия, очищенного от корки, отрезают кубик со сторонами около 1-1.5 см (правила обращения с натрием!)
От приготовленного кубика натрия отрезаются кусочки величиной с горошину или немного больше и погружаются один за другим в налитую в ступку ртуть (при помощи щипцов, со всеми предосторожностями, указанными в т.1).
Полученная амальгама переливается в склянку, которая хорошо закрывается пробкой.
Опыт. Поместить приготовленную амальгаму в бокал или стакан (слоем в 2-3 см) и налить насыщенный раствор нашатыря NH4Cl, для чего растворить при нагревании около 40 г NH4Cl в 100 мл воды и дать остыть. Амальгама начинает пузыриться и подниматься до краев сосуда и выше (поэтому лучше поставить сосуд в чашку); затем постепенно снова опадает.
По окончанию урока оставшуюся после опыта ртуть промыть водой, разбавленным раствором азотной или серной кислоты и снова водой.
При лабораторном опыте можно выдать учащимся пробирки с уже готовой амальгамой натрия. "

Аналогичное описание приведено также в книге Ф.П. Платонов Лекционные опыты и демонстрации по общей и неорганической химии
ссылка:

После анализа литературы решил повторить этот опыт, но в небольших масштабах. Пропорции уменьшил в 10 раз: не из-за недостатка в ртути и натрии, а по причине некоторых сложностей приготовления амальгамы натрия. Растворение натрия в ртути - бурный процесс, сопровождаемый вспышкой, натрий бросают маленькими кусочками, придавливая его пестиком. Амальгаму натрия я никогда не готовил, поэтому использовал минимальный объем. Для получения 10 г однопроцентной амальгамы нужно всего 0.1 г натрия (кусочек размером с горошину).
Эффектность опыта от этого не пострадала, уменьшились лишь масштабы. Взял 4.0 г хлорида аммония и растворил его в 10 мл теплой воды. Для опыта решил использовать мерный цилиндр на 50 мл. Затем отвесил 10.0 г ртути, налил ее в тигель и стеклянной палочкой придавил кусочек натрия (предварительно обрезанный от корочек и обсушенный бумагой). Через некоторое время произошла вспышка с легким звуком и натрий растворился. Опыт делал на открытом воздухе. Лучше, наверное, было взять ступку, как это рекомендуется в руководствах, но из-за небольших масштабов я использовал высокий фарфоровый тигель. Полученную 1 % амальгаму натрия перелил в бюкс с пришлифованной пробкой. По виду она похожа на ртуть, но в отличие от ртути амальгама натрия немного смачивает стекло и поверхность ее постепенно тускнеет.

Амальгама натрия фото И.Н. Григорьев
Затем в теплый раствор хлорида аммония вылил амальгаму натрия.

Амальгама аммония
Очень быстро образовалась губчатая масса большого объема. Рост ее сопровождался легким шипением. Масса увеличивалась, и возникло опасение, что она вылезет из цилиндра. На случай этого я заранее подготовил стакан.

Амальгама аммония
Однако масса осталась в цилиндре. Когда я вытряхнул амальгаму аммония в стакан, ее размер уменьшался на глазах.
Через 5 минут после начала опыта объем амальгамы был всего в 4-5 раз больше первоначального объема ртути. Залитая горячей водой амальгама медленно выделяла пузырьки газа. Скоро реакция прекратилась, я промыл ртуть водой и поместил ее в исходную склянку.

Ртуть, оставшаяся после разложения амальгамы аммония
Эффектность опыта от этого не пострадала, уменьшились лишь масштабы. Взял 4.0 г хлорида аммония и растворил его в 10 мл теплой воды. Для опыта решил использовать мерный цилиндр на 50 мл. Затем отвесил 10.0 г ртути, налил ее в тигель и стеклянной палочкой придавил кусочек натрия (предварительно обрезанный от корочек и обсушенный бумагой). Через некоторое время произошла вспышка с легким звуком и натрий растворился. Опыт делал на открытом воздухе. Лучше, наверное, было взять ступку, как это рекомендуется в руководствах, но из-за небольших масштабов я использовал высокий фарфоровый тигель. Полученную 1 % амальгаму натрия перелил в бюкс с пришлифованной пробкой. По виду она похожа на ртуть, но в отличие от ртути амальгама натрия немного смачивает стекло и поверхность ее постепенно тускнеет.
Амальгама натрия фото И.Н. Григорьев
Затем в теплый раствор хлорида аммония вылил амальгаму натрия.
Амальгама аммония
Очень быстро образовалась губчатая масса большого объема. Рост ее сопровождался легким шипением. Масса увеличивалась, и возникло опасение, что она вылезет из цилиндра. На случай этого я заранее подготовил стакан.
Амальгама аммония
Однако масса осталась в цилиндре. Когда я вытряхнул амальгаму аммония в стакан, ее размер уменьшался на глазах.
Через 5 минут после начала опыта объем амальгамы был всего в 4-5 раз больше первоначального объема ртути. Залитая горячей водой амальгама медленно выделяла пузырьки газа. Скоро реакция прекратилась, я промыл ртуть водой и поместил ее в исходную склянку.
Ртуть, оставшаяся после разложения амальгамы аммония