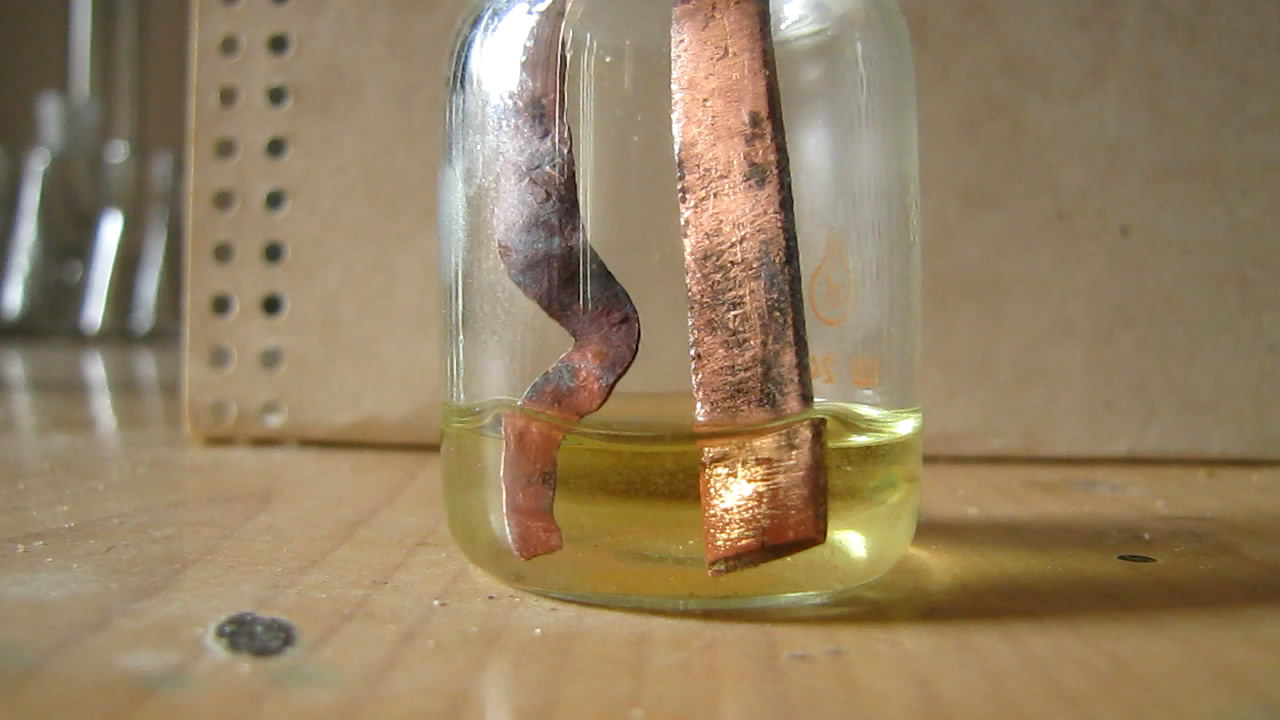
Электролиз с переменным током (соляная кислота, медные электроды)
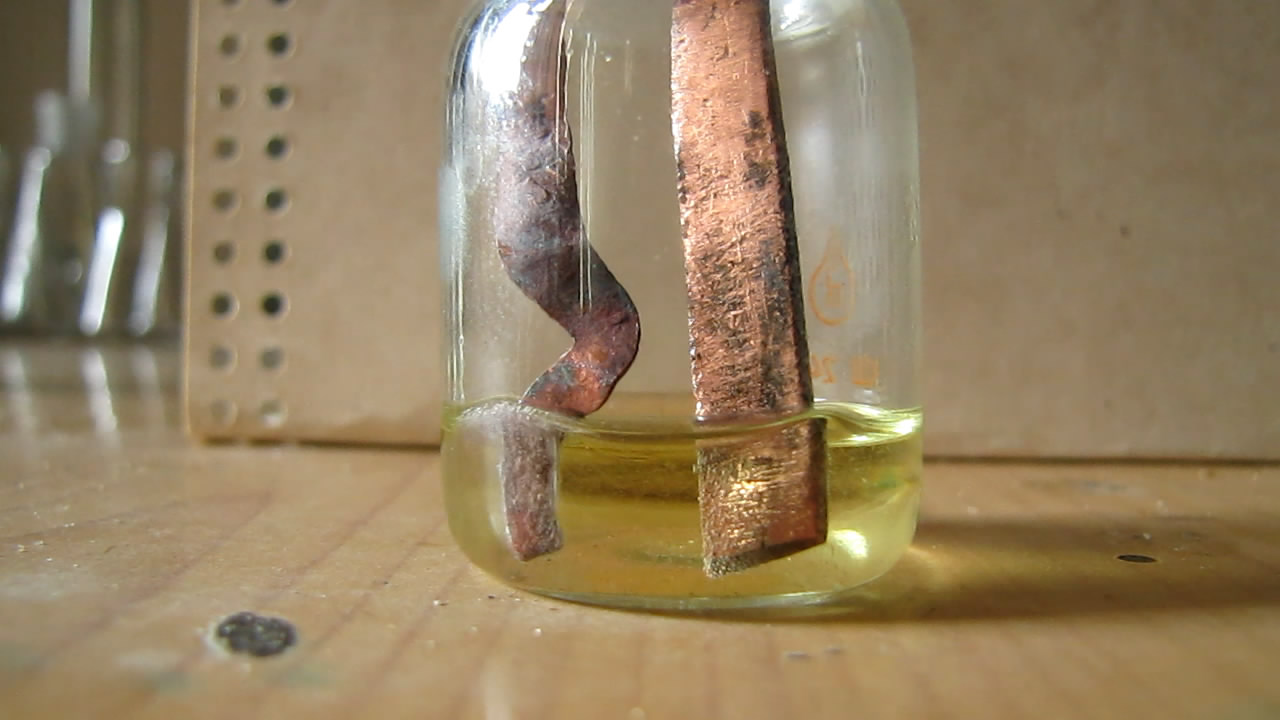
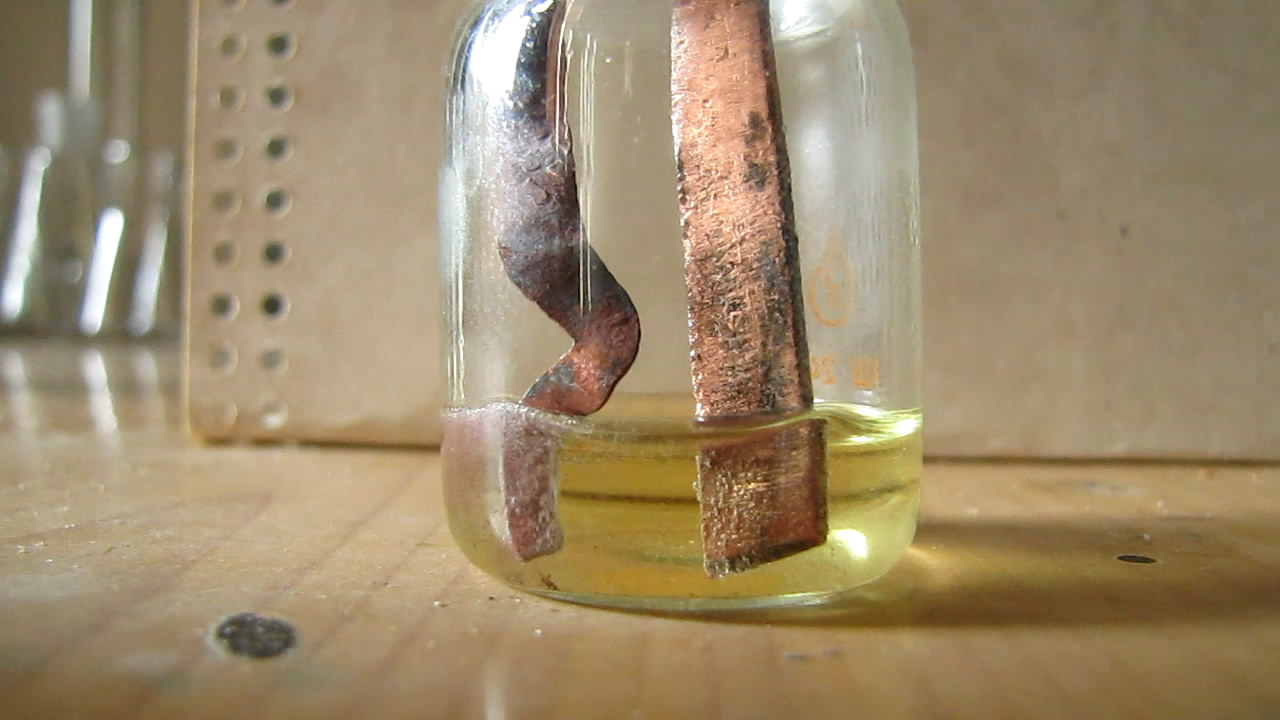
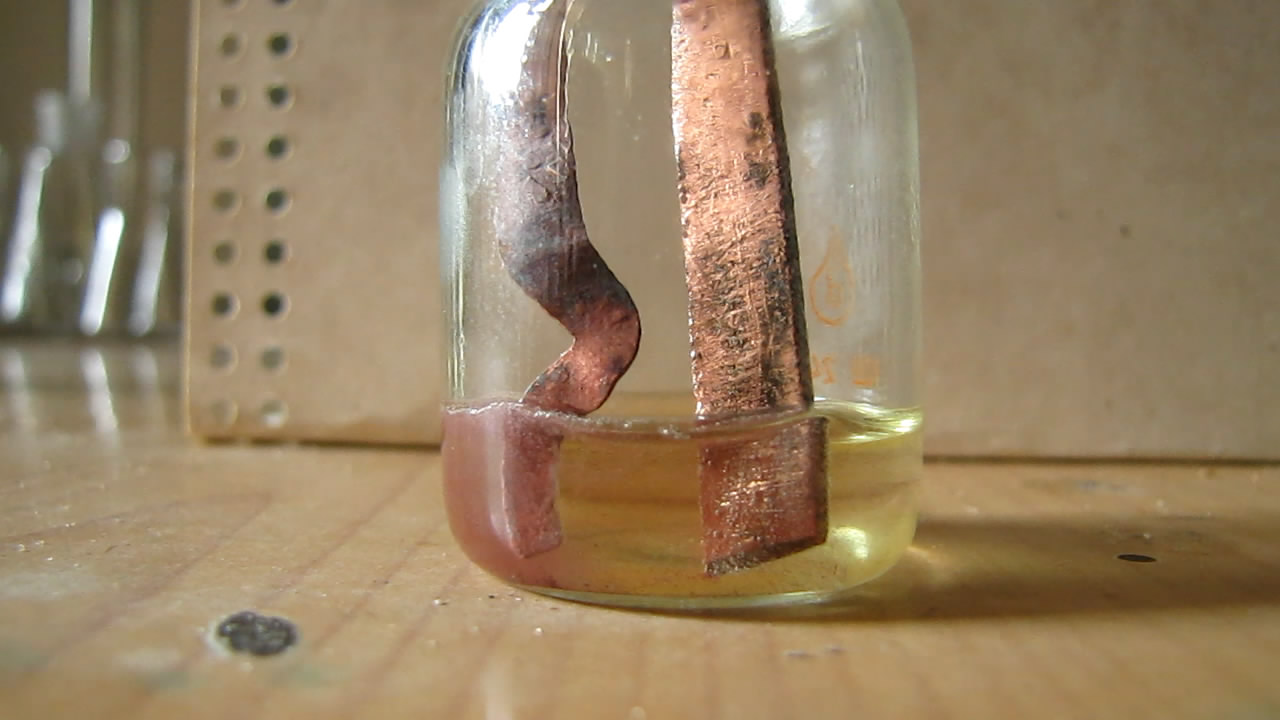
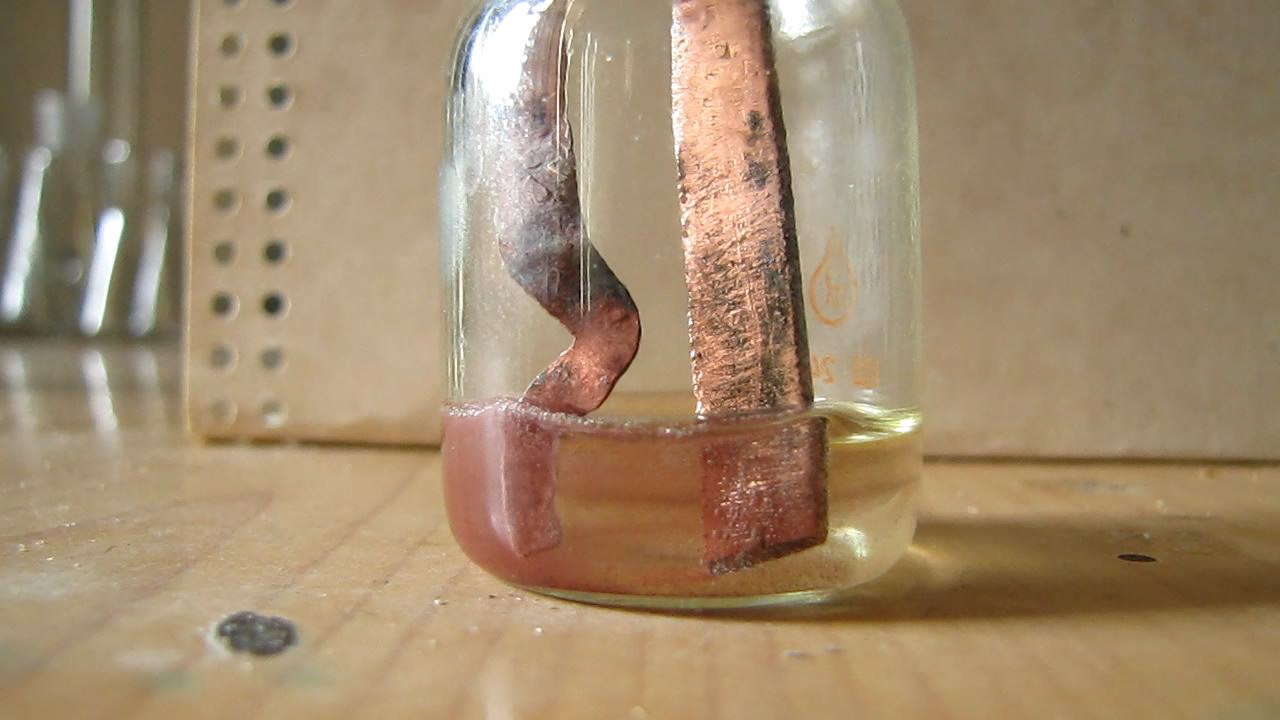

















| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 3 2015 Журнал Химиков-Энтузиастов |
Электропроводность, электролиты, электролиз с переменным током ч.7 В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Электролиз с переменным током (соляная кислота, медные электроды)
Попробовал, как ведут себя медные электроды в концентрированной соляной кислоте. Один электрод представлял собой медную пластинку, другой - расплющенную проволоку. От контакта меди с кислотой раствор слегка окрасился в желтый цвет (растворение оксидной пленки и постепенное растворение металла - за счет совместного действия кислоты и воздуха).
Электроды подключил к ЛАТРу и дал напряжение 10 В. На обоих электродах началось выделение газа: на проволоке - сильное, с поверхности пластинки - сравнительно слабое. Раствор стал окрашиваться в красный цвет, образовался красный осадок (мелкодисперсная медь). Проволока начала заметно разрушаться. Образование мелкодисперсной меди можно объяснить циклами растворения-осаждения меди. Сначала медь растворяется с поверхности электрода (когда тот играет роль анода) и переходит в раствор в виде соли (вернее - комплексных кислот: H[CuCl2] и H2[CuCl4]). Потом - когда электрод становится катодом - происходит осаждение меди из раствора в виде металла, только осажденная медь не образует компактное покрытие, а выделяется в виде мелких частиц, которые дают суспензию в растворе, а также осадок на дне бюкса и на поверхности электродов. Минут через 10 раствор нагрелся, выделение газов значительно усилилось, запахло соляной кислотой. Опыт прекратил. Со временем жидкость расслоилась: выпал красный осадок и образовался желтый раствор (цвет хлоридного комплекса двухвалентной меди). Вскоре в электролизере образовалось не два, а три слоя. Верхние несколько миллиметров - желтые, снизу - красный осадок (немного), а между ними почти бесцветный мутный раствор (хлоридный комплекс одновалентной меди и муть неосевших частиц). При стоянии на воздухе с раствором соляной кислоты мелкодисперсная медь должна была раствориться. На следующее утро не посмотрел (забыл), но еще через день в бюксе был желтый раствор: осадок меди полностью исчез. Чтобы промыть электроды (сразу же после опыта), опустил их в стакан с водой (из-под крана). На всякий случай включил ток. При напряжении 20 В с поверхности проволоки стал выделяться газ, с поверхности пластинки - тоже, но еле заметно. При 30 В выделение газа резко усилилось. БОльшее напряжение давать не стал - можно сжечь ЛАТР (а он не мой). Вспомнил, что когда проводил электрохимическое растворение родия в бромистоводородной кислоте (переменный ток), тоже растворялся преимущественно только один электрод. Часть родия была в осадке (но не много). Раствор также грелся. |
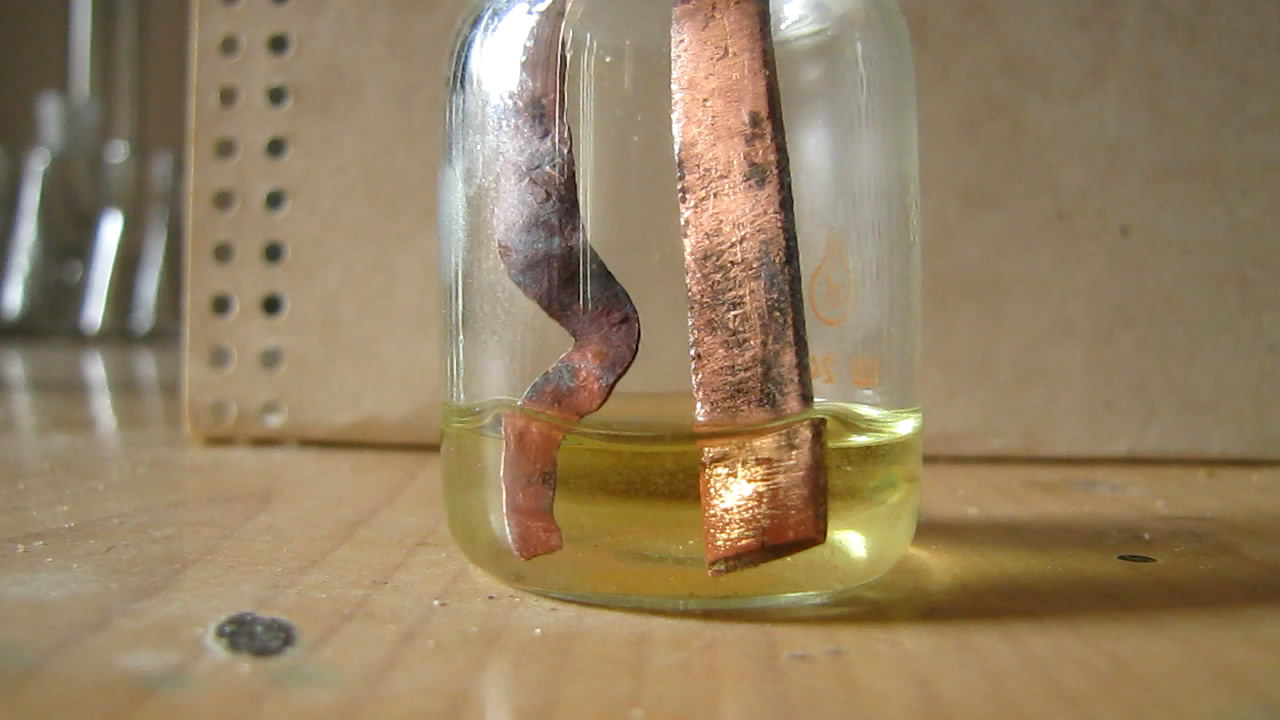
Электролиз с переменным током (соляная кислота, медные электроды) |
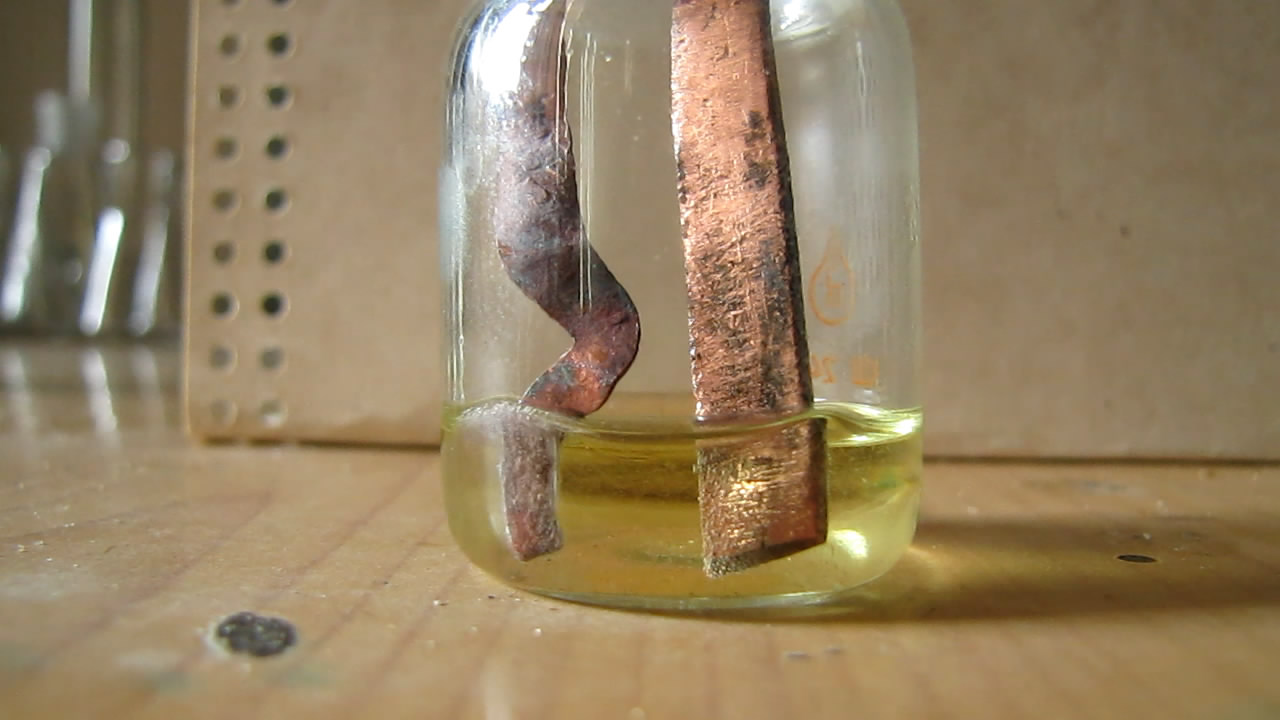
|
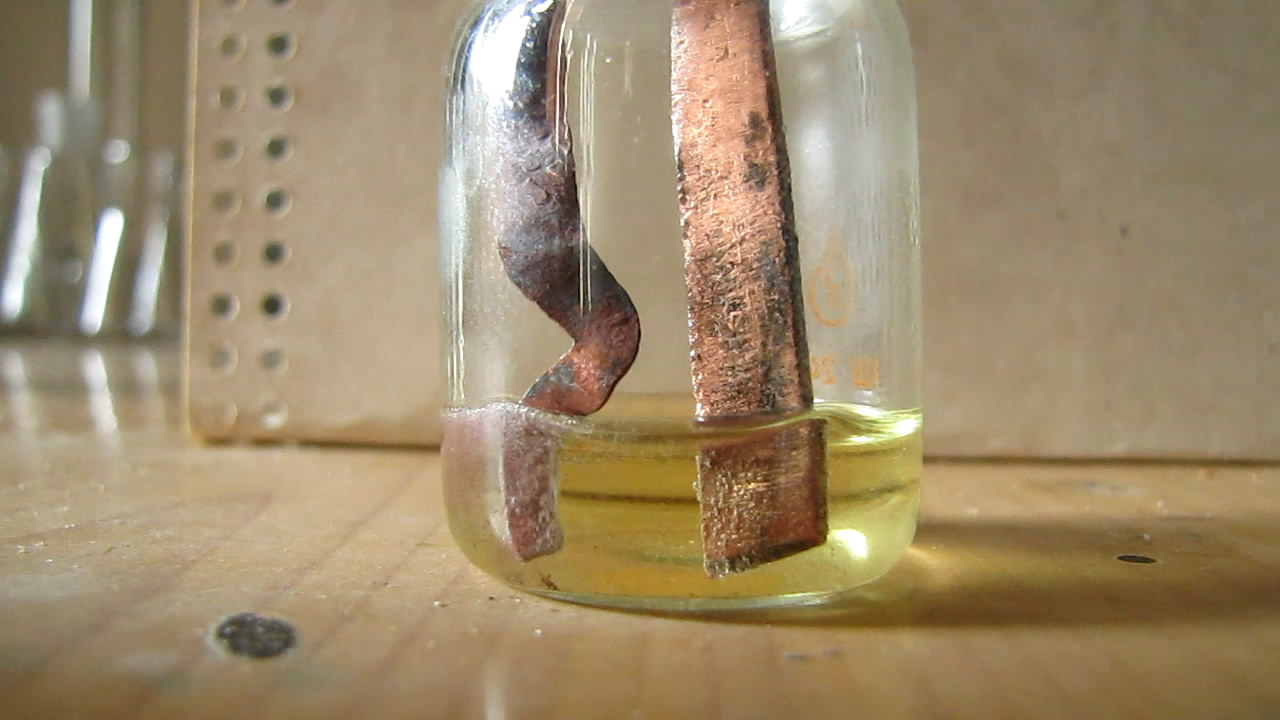
|
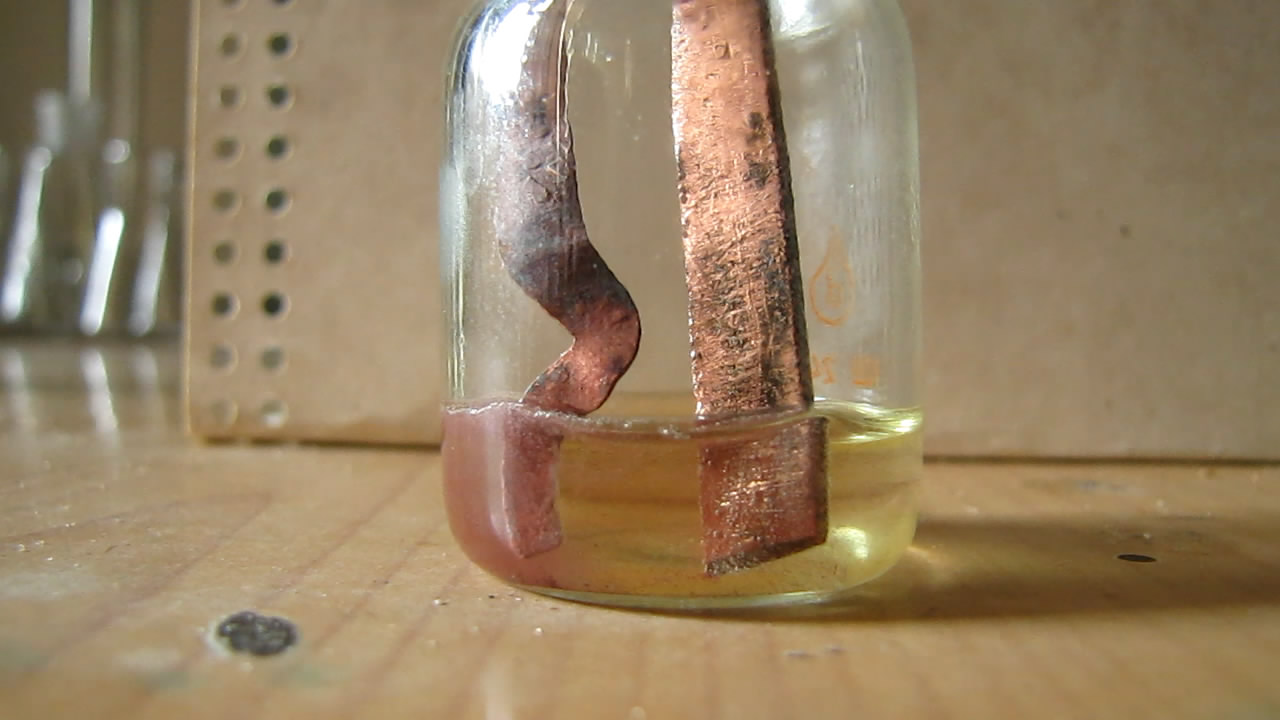
|
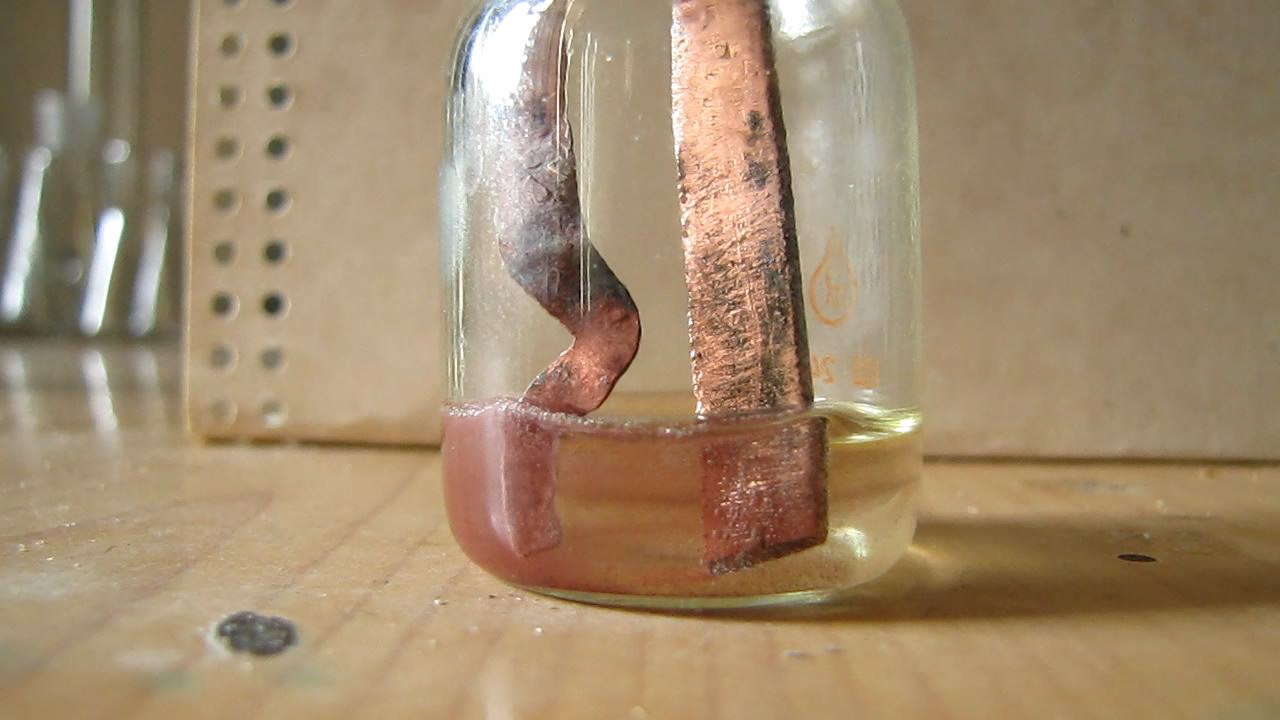
|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
Электропроводность, электролиты, электролиз с переменным током ч.8 В.Н. Витер |
|
Электролиз с переменным током (хлорид натрия, медные электроды)
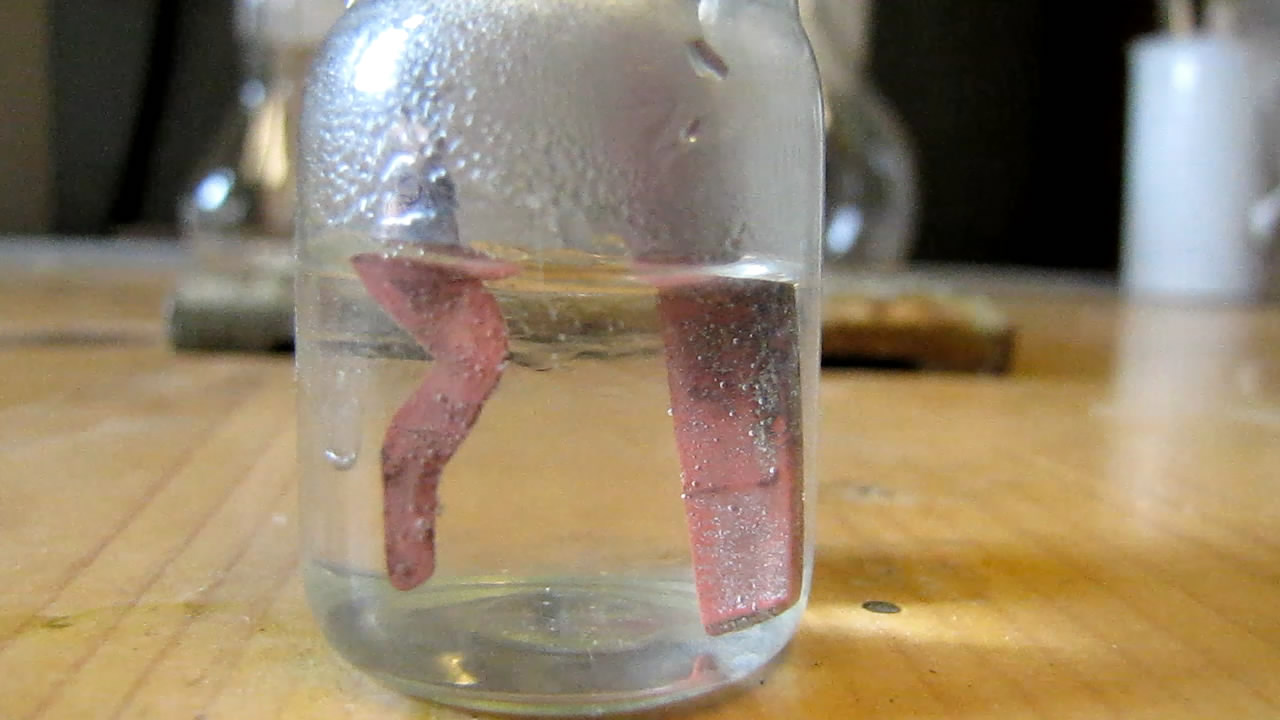
Провел несколько опытов по электролизу хлорида натрия переменным током. В первом опыте налил в бюкс насыщенный раствор поваренной соли (профильтрованная каменная соль), опустил два медных электрода (те же, что и в предыдущем опыте) и дал 10 вольт (от розетки 220 В через ЛАТР). Первоначально не наблюдалось видимых изменений, но потом стало видно, что поверхность электродов стала "губчатой". Когда поднял напряжение до 20 В, раствор начал греться и закипать - пришлось снизить напряжение до 10 В.
Добавил в бюкс раствор фенолфталеина и встряхнул - электролит стал малиновым, с электродов осыпался осадок. Началось активное выделение газа. |

Электролиз с переменным током (хлорид натрия, медные электроды) |
|
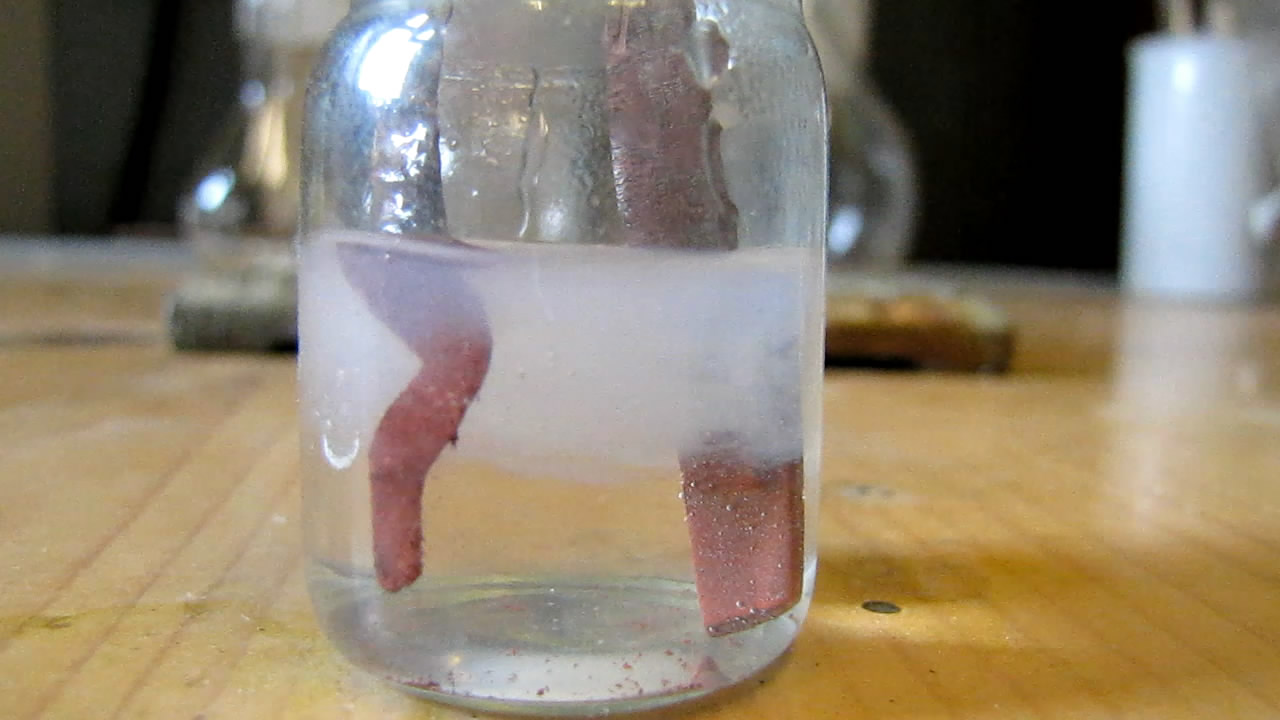
Добавлен фенолфталеин (спиртовый раствор) |

|

|

|

|

|

|
|
Второй опыт. Заменил электролит, электроды не промывал (чтобы не затронуть губку). Остатки фенолфталеина окрасили сначала электроды, а потом и раствор в слабо-малиновый цвет. Было заметно, как на расплющенной проволоке образуется губчатая медь, часть ее непрерывно опадала на дно. Временами на электродах выделялся газ.
Раствор грелся, но не сильно. Примерно через 5 минут прекратил электролиз, вынул электроды. Стало видно, что оба они покрыты губчатой медью. |

Электролиз с переменным током (хлорид натрия, медные электроды) |

|

|

|

|

|

|
|
Губку стер, электролит заменил, начал третий опыт. К большой неожиданности в момент включения тока на электродах начал выделяться газ (довольно интенсивно), а раствор становился желтым. Минут через пять раствор стал непрозрачным, выделение газа продолжалось. Со временем на меньшем электроде стало видно образование медной губки (которая частично опадала).
|

Электролиз с переменным током (хлорид натрия, медные электроды) |
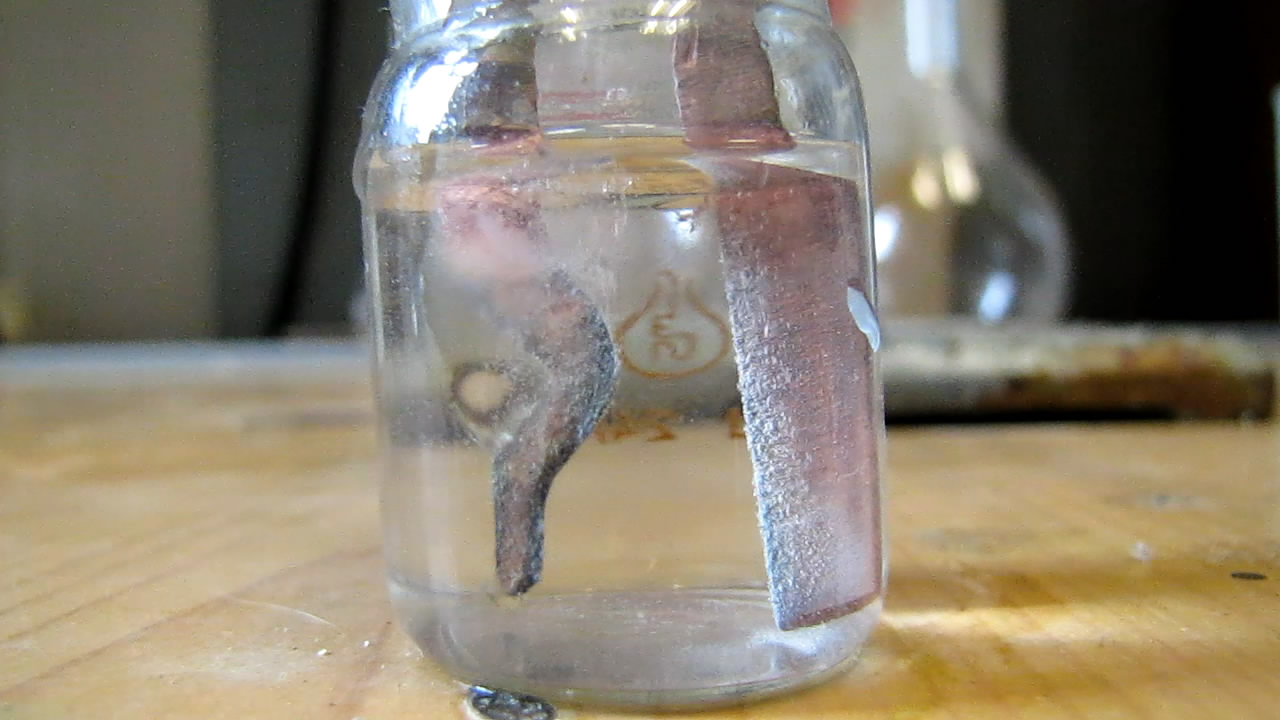
|

|

|

|

|

|

|
Электропроводность, электролиты, электролиз с переменным током ч.9 В.Н. Витер |
|
Электролиз с переменным током (хлорид натрия, медный и железный электроды)
В данном эксперименте напряжение было не 10, а 220 В (переменный ток), ячейка с насыщенным раствором поваренной соли была подключена не через ЛАТР, а последовательно с лампой накаливания, как в опыте по демонстрации электропроводности (собственно, с этого опыта все и началось). Электроды: в одном случае - медь и сталь, в другом - два железных гвоздя.
После включения тока лампа загорелась, зато в ячейке никаких видимых изменений не происходило (в некоторых случаях было слабое и непродолжительное выделения газа). Добавил фенолфталеин (раствор в спирте). Жидкость возле обоих электродов окрасилась в малиновый цвет, но окрашенным был только приэлектродный слой, примем, окрашенный слой был несплошной и нестабильный: в одном месте окраска появлялась, в другом исчезала. |

Электролиз с переменным током (хлорид натрия, железный и медный электроды) |

|

|

|

|

|

|

|

|

|

|

|