Химия и Химики № 3 2021
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 3 2021 Журнал Химиков-Энтузиастов |
Имидазолины, ингибиторы коррозии, моющие средства и знакомство с новой лабораторией - ч.1, 2, 3 Imidazolines, corrosion inhibitors, detergents and introduction to new laboratory Добрьій Химик |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Пробный эксперимент / Test experiment
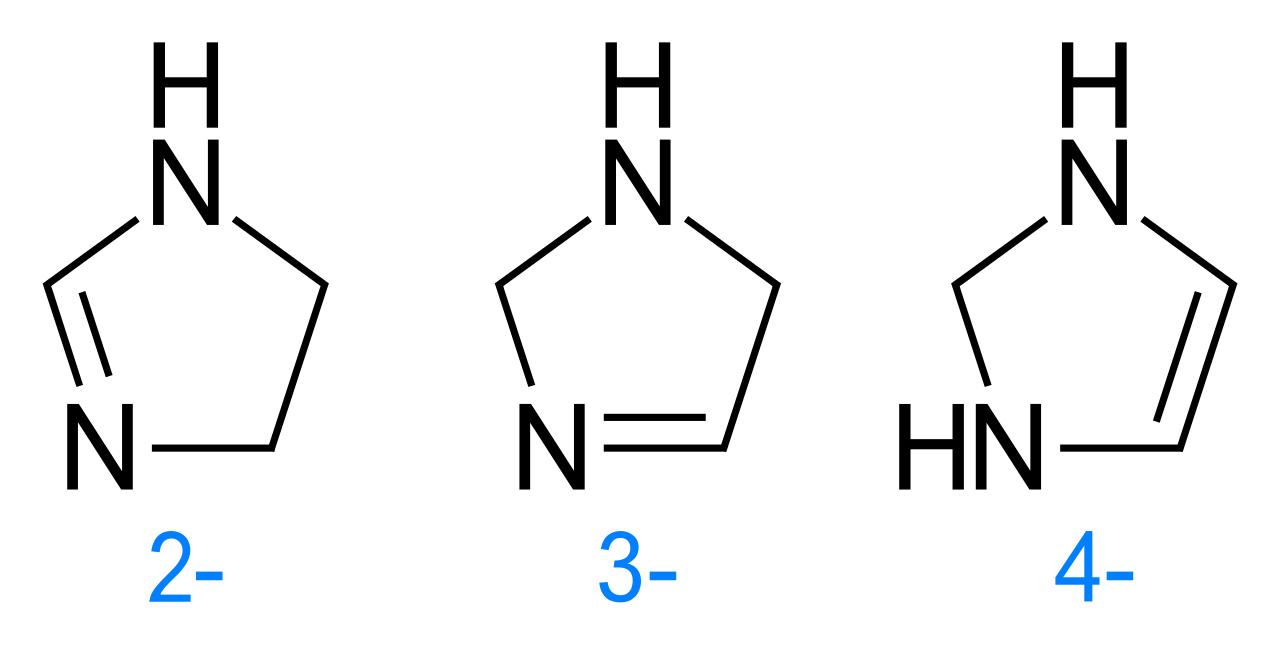
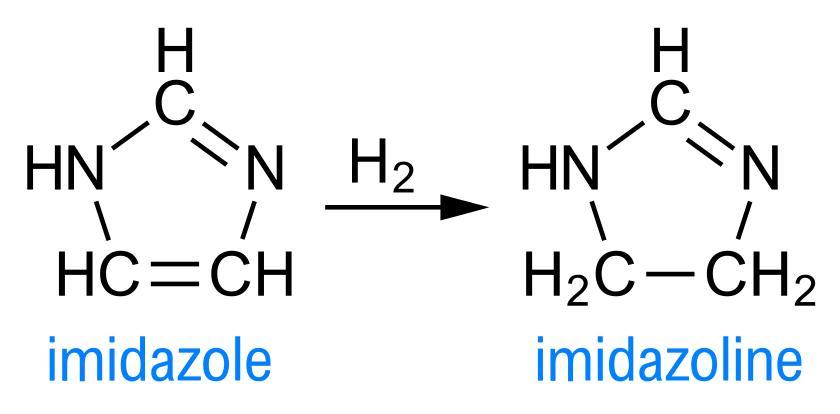
Что такое имидазолины? Это пятичленные гетероциклы, содержащие два атома азота и одну двойную связь в цикле:
  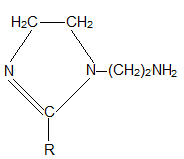 где R - радикал из жирных кислот (кокосового, пальмового, подсолнечного или таллового масла) Аминоэтилалкилимидазолин получают азеотропной отгонкой воды при взаимодействии технических жирных кислот с ДЕТА (диэтилентриамин). У нас для этой цели (азеотропной отгонки) использовали толуол, в промышленности берут ксилолы. 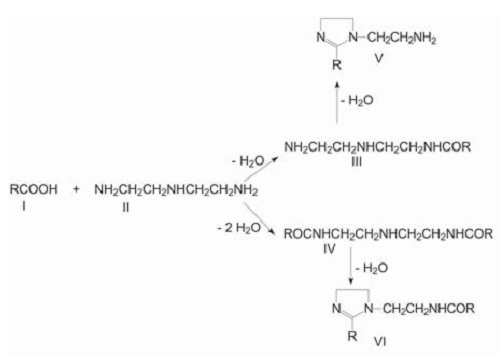 В числе прочего нашел статью по теме [1] - теперь стало понятно, как получают данный продукт и что от меня хотят. А хотели от меня синтеза новых производных из технического аминоэтилалкилимидазолина - дешевых и эффективных в качестве ингибиторов коррозии. Раз дешевых, значит, и исходные вещества должны быть дешевыми и доступными. Для начала коллега предложил провести взаимодействие аминоэтилалкилимидазолина с малеиновым ангидридом: в мягких и жестких условиях. Допущение было такое. В жестких условиях образуется циклический амид - кислород в цикле малеинового ангидрида заместится на азот (с боковым заместителем, содержащим цикл имидазолина) - произойдет реакция конденсации (реакция 1). В мягких условиях произойдет присоединение молекулы аминоэтилалкилимидазолина с раскрытием цикла малеинового ангидрида (реакция 2). 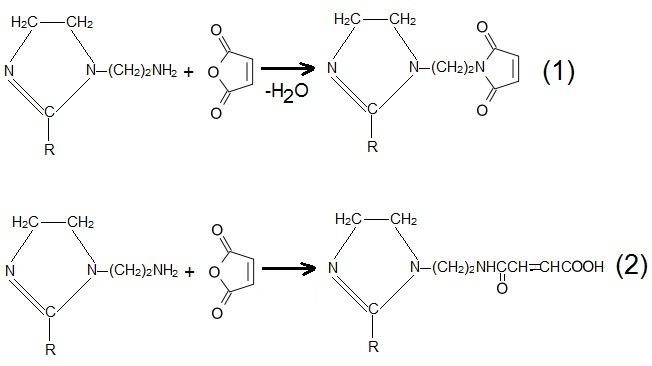 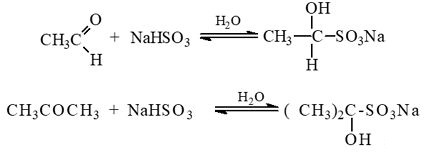 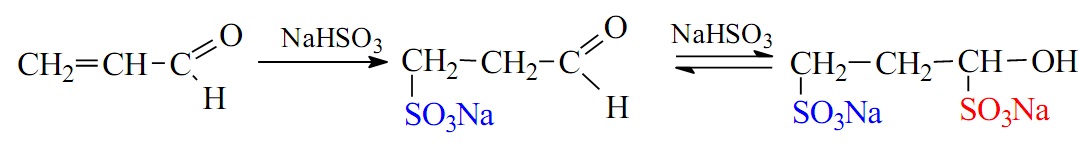 Теория - теорией, но как это выглядит на практике? Коллега сказал мне среднюю молекулярную массу нашего аминоэтилалкилимидазолина, и я взвесил две равные навески этого вещества и две навески малеинового ангидрида (в расчете на эквимолярные количества: 35 г производного имидазолина, 10 г малеинового ангидрида). Первая система - "жесткие условия": поставил аминоэтилалкилимидазолин в конической колбе на магнитную мешалку, стал добавлять порциями малеиновый ангидрид. Произошел самопроизвольный разогрев до 60°С, смесь загустела, якорь магнитной мешалка остановился (завяз). Позже - включил нагрев примерно до 120°С, периодически пытался перемешивать толстой стеклянной палочкой. Вторая система - "мягкие условия". Решили, чтобы температура не поднималась выше комнатной. Как? К навеске аминоэтилалкилимидазолина добавил 82 г EtAc (этилацетат) и 20 г этилацетата - к малеиновому ангидриду. Малеиновый ангидрид растворился не полностью. Раствор аминоэтилалкилимидазолина в колбе поставил на водяную баню с холодной водой, под баней - магнитная мешалка. Небольшими порциями добавлял раствор малеинового ангидрида в этилацетате. Каждый раз контролировал температуру инфракрасным термометром. При добавлении порции раствора наблюдался небольшой нагрев, но температуру удалось удержать не выше 28°С. В результате образовался красно-коричневый, почти черный раствор с белым осадком не растворившегося малеинового ангидрида (вероятно, при хранении произошла частичная его полимеризация). Оставил на ночь - осадок остался. Отделил его декантацией. Потом раствор упарили на роторнике (роторный испаритель), не допуская нагрева выше 40°С (или 30°С - не помню). Получилась коричневая вязкая смола. Зато первая реакционная смесь ("жесткие условия") застыла в твердую и хрупкую смолу, похожую на канифоль. Вероятно, вместо предлагаемой реакции (1) [- см. рисунок выше], имела место межмолекулярная поликонденсация. При нагревании смола немного размягчалась, при охлаждении - застывала. Смола - мечта ВМС-ника и проклятие органика, а поскольку я ни в одной из этих областей почти не работал, отнесся к ней без эмоций. __________________________________________________ 1 См. статью: СИНТЕЗ ПРОИЗВОДНЫХ 1,2-ИМИДАЗОЛИНА - АКТИВНОЙ ОСНОВЫ ИНГИБИТОРОВ КОРРОЗИИ. КОМПЛЕКСНЫЙ ПОДХОД К АНАЛИЗУ ИМИДАЗОЛИНОВ НА ПРИМЕРЕ ПОЛУЧЕННЫХ СОЕДИНЕНИЙ [ссылка]. |

Исходные вещества: аминоэтилалкилимидазолин и малеиновый ангидрид |

|

|

|

Первую реакционную смесь просто нагрели на плитке |

Вторую реакционную смесь (слева) разбавили этилацетатом и перемешивали на водяной бане, не допуская нагрева. (По центру - первая реакционная смесь, справа - подсолнечное масло [это - другой эксперимент]) |

|

Вскоре первая реакционная смесь стала насколько вязкой, что якорь магнитной мешалки остановился - пришлось перемешивать толстой стеклянной палочкой |

Вторую реакционную смесь декантировал и упарил на роторном испарителе |

|

|

Вторая реакционную смесь после упаривания |

|

Инфракрасный термометр |

|
|
Смолу получил, даже в двух экземплярах... Теперь нужно довести ее до ума. Сначала - попробовал, в чем она растворима. Взял второй образец (полученный в мягких условиях). С водой - дает суспензию/эмульсию и пену. В уксусной кислоте 1 к 1 растворяется хорошо, дает коричневый раствор без опалесценции. В этаноле растворяется хорошо. С разбавленным раствором едкого натра дает суспензию/эмульсию при добавлении еще едкого натра - выпадает в осадок.
Следующая стадия - сульфирование. Действие водного раствора гидросульфита натрия (другое название - метабисульфит натрия) [K1]. Задача: наколупать по 12-14 грамм продуктов (1) и (2), перенести их в колбу. Учитывая, что смола пристала к колбе, задача была непростая. Первая смола была твердой и хрупкой, вторая - вязкой и липкой. Хорошо, что в лаборатории были подходящие шпатели. Количество гидросульфита натрия рассчитал из допущения, что в первом случае молекулы аминоэтилалкилимидазолина и малеиновый ангидрида объединяются, отщепляя молекулу воды, а во втором - что происходит просто реакция присоединения. Поскольку молекулярные массы обеих продуктов большие, это не имело существенного значения (навески смолы были около 13 г, навески гидросульфита - около 3 г в 10 г воды). Залил образцы смолы раствором гидросульфита, поставил на магнитные мешалки. Первоначально - было грустное зрелище: комок смолы под слоем раствора, комок колотит якорь магнитной мешалки. Продукт 1 не растворялся, продукт 2 - медленно эмульгировался. Добавил по 10 г этанола, повысил температуру до 40°С. Продукт 2 стал растворяться, поднял температуру до 50°С - он растворился полностью, образовался раствор без опалесценции. Зато продукт 1 - растворился лишь частично - больше размазался по колбе. Добавки еще 20 мл этанола и 10 мл воды не спасли. Итого получился: раствор с осадком из продукта 1 и коричневый раствор - из продукта 2. Заключительная стадия приготовления ингибитора - добавка эквимолярного количества триэтаноламина (получилось 4.4 г). Образец 2 отдали на испытания. Оказалось, что он работает не хуже, чем продажные ингибиторы коррозии. Причем, если имидазолины обычно растворимы в кислотах и не растворимы в щелочах, что этот продукт растворим в щелочах, что хорошо для защиты от коррозии в среде гипохлорита натрия. Образец 1 я перелил в другую колбу, он долго стоял под вытяжкой - набухшая, но нерастворимая смола, пока через несколько месяцев его не выкинули. |

Продукт 1 (перед сульфированием) |

|

|

|

Продукт 2 (перед сульфированием) |

|

|

|

Гидросульфит натрия |

Сульфирование (слева - продукт 1, справа - продукт 2) |

|

|

|

Добавляем триэтаноламин (продукт 2) |

|

Добавляем триэтаноламин (продукт 1) |

|

|

|

Продукт 2 - перед испытанием ингибирующих свойств |

Продукт 1 - стоял-стоял, пока не выкинули |

Исходные вещества |

|

|

|

|

|

Аминоэтилалкилимидазолин в этилацетате |

|

|

|

|

Завершение реакции |

Удаление этилацетата в роторном испарителе |

|

|

|

|

|

Дополнительный холодильник роторного испарителя |

Этилацетат, который конденсировался |

|

Гидросульфит натрия |

|

|

|

|

|

|

|

|

Триэтаноламин |

|

|

Готовый ингибитор |
|

|

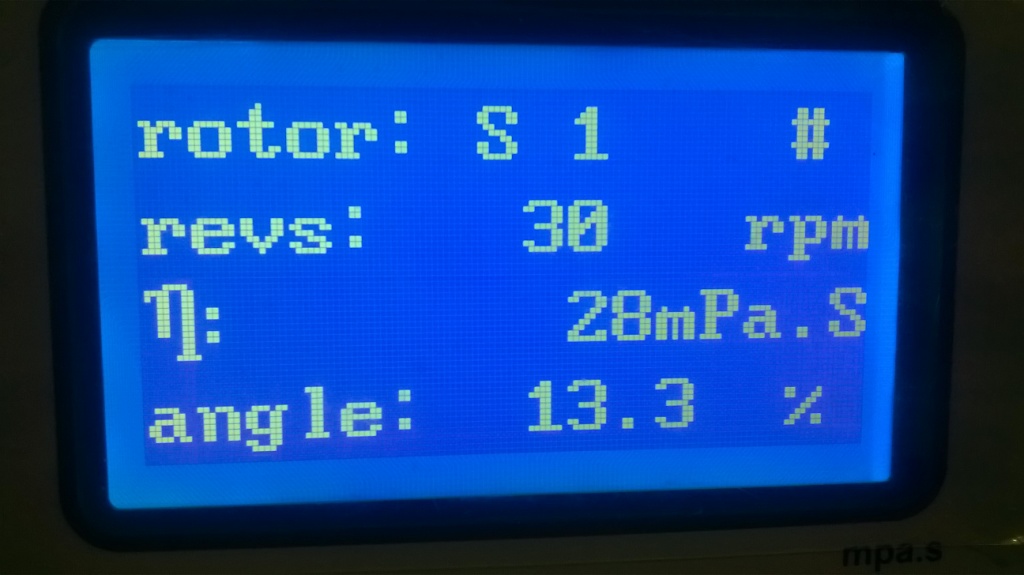
Измерение вязкости |

|
|
|

|
|
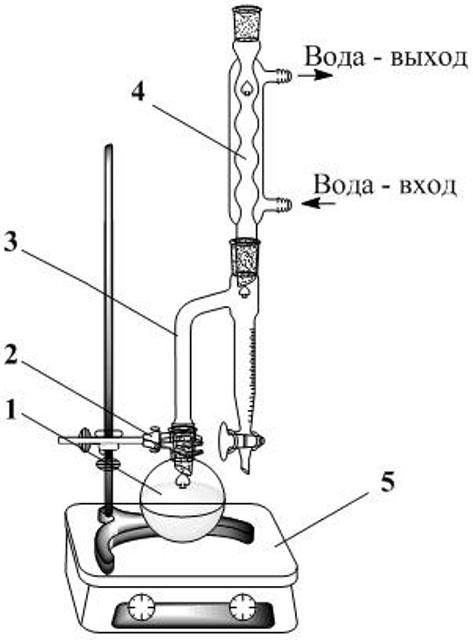
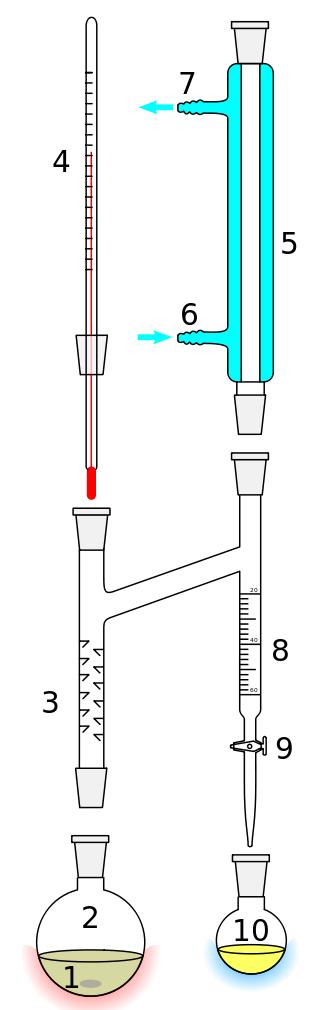
Возможны также некоторые усложнения, вроде дефлегматора, термометра и т.п. В конкретном случае вместо дефлегматора мы наоборот укутывали нижнюю часть насадки стеклотканью, чтобы пары толуола и воды "дотянули" до обратного холодильника (а не конденсировались в нижней части насадки и стекали назад в колбу безо всякой пользы).
|
|
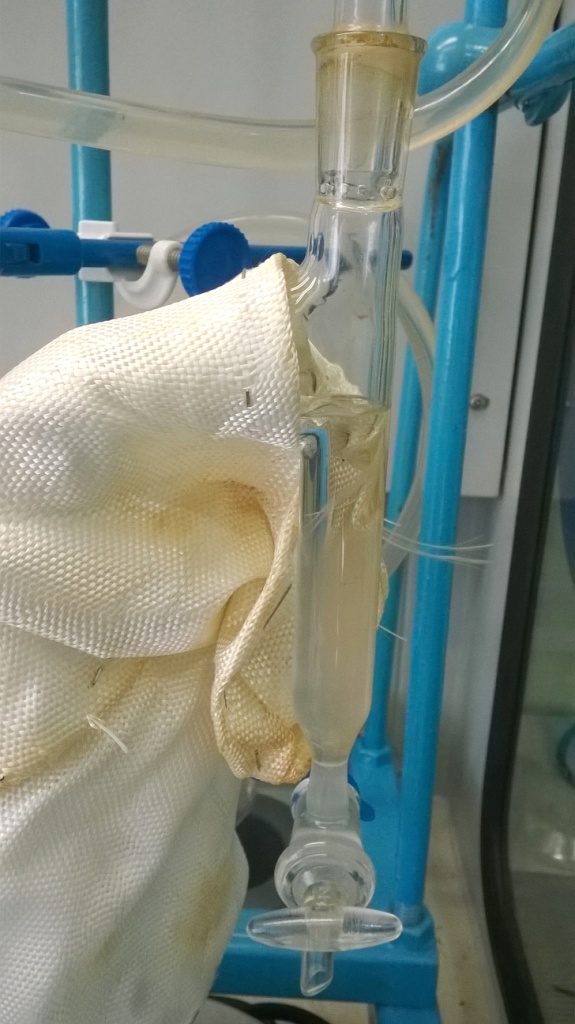
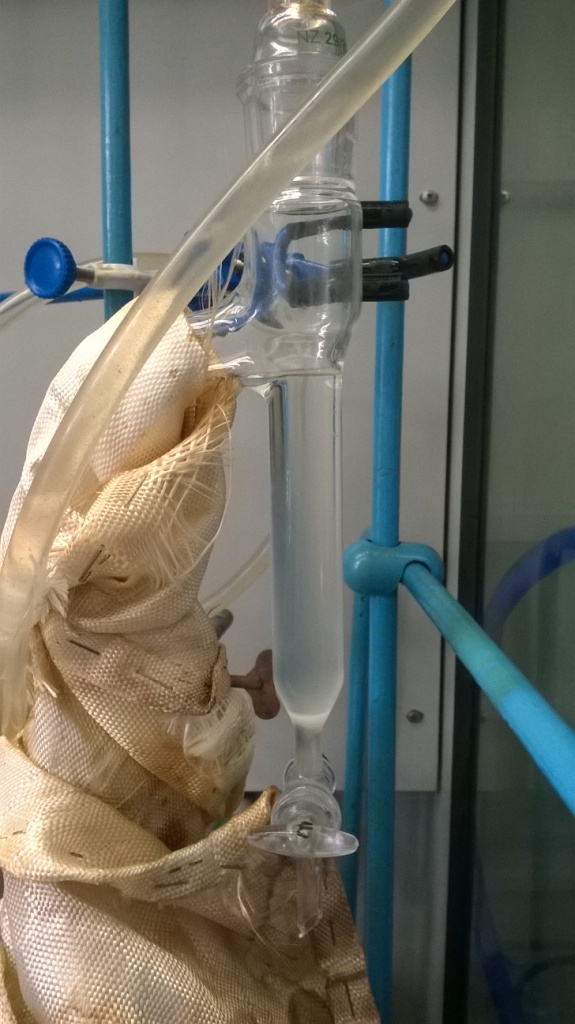
Насадка Дина-Старка в работе (синтез диэтаноламидов из растительных масел) |
|
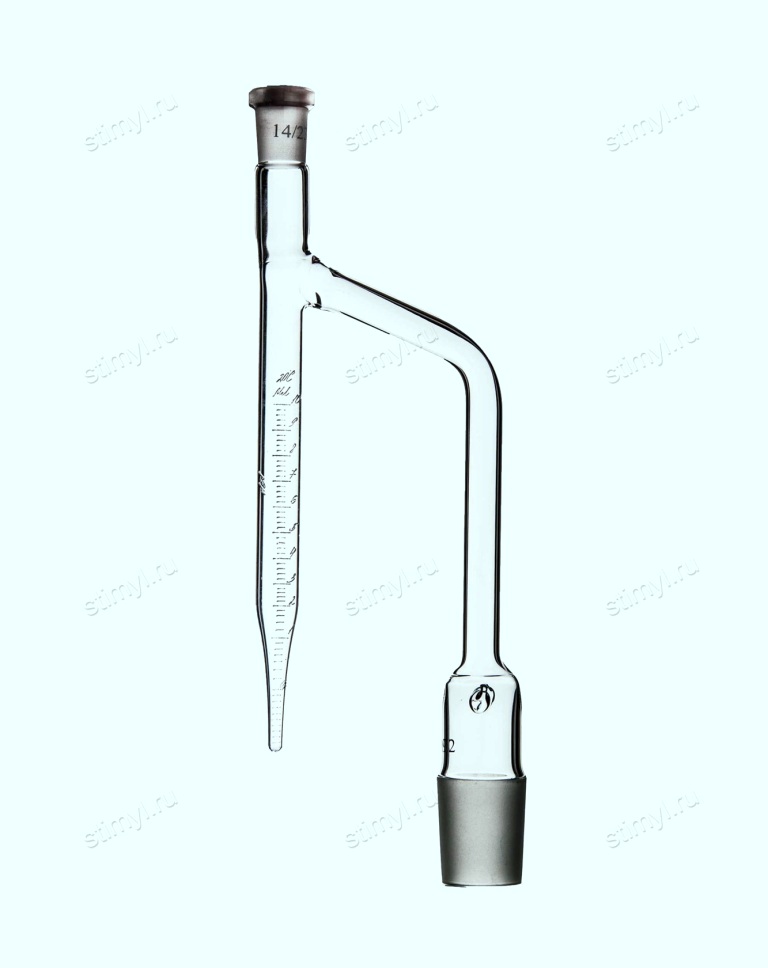
Перед тем, как слить воду, можно измерить ее объем по специальной шкале. Благодаря этому, насадка Дина-Старка используется не только в синтезе, но и в химическом анализе. Насадки, предназначенные именно для количественного анализа (содержания воды в продукте), могут вообще не иметь нижнего крана - только глухое дно: кран может протекать (это некритично при синтезе, но абсолютно недопустимо при анализе).
Например, такая насадка Дина-Старка используется для определения содержания воды в нефти |
|
|
Разумеется, насадка Дина-Старка может быть использована не только для пары вода - органический растворитель, но и для любой пары жидкостей, которые не смешиваются и образуют азеотроп. Просто система органический растворитель - вода является наиболее распространенным на практике случаем.
Некоторые органические растворители тяжелее воды, например, хлороформ, хлористый метилен. В таких случаях берут "обратную" насадку Дина-Старка, для работы с тяжелыми жидкостями - в ней в колбу сливается не верхний слой жидкости, а нижний. Товарищ рассказывал, что у них во время студенческого практикума некоторые личности (почему-то особенно часто - дамы) брали вместо прямой насадки Дина-Старка обратную. Результат - истерика, т.к. потрачено масса времени и труда, а синтез не получается. Вживую таких насадок я не видел, но поиск в интернете быстро дал результаты: |
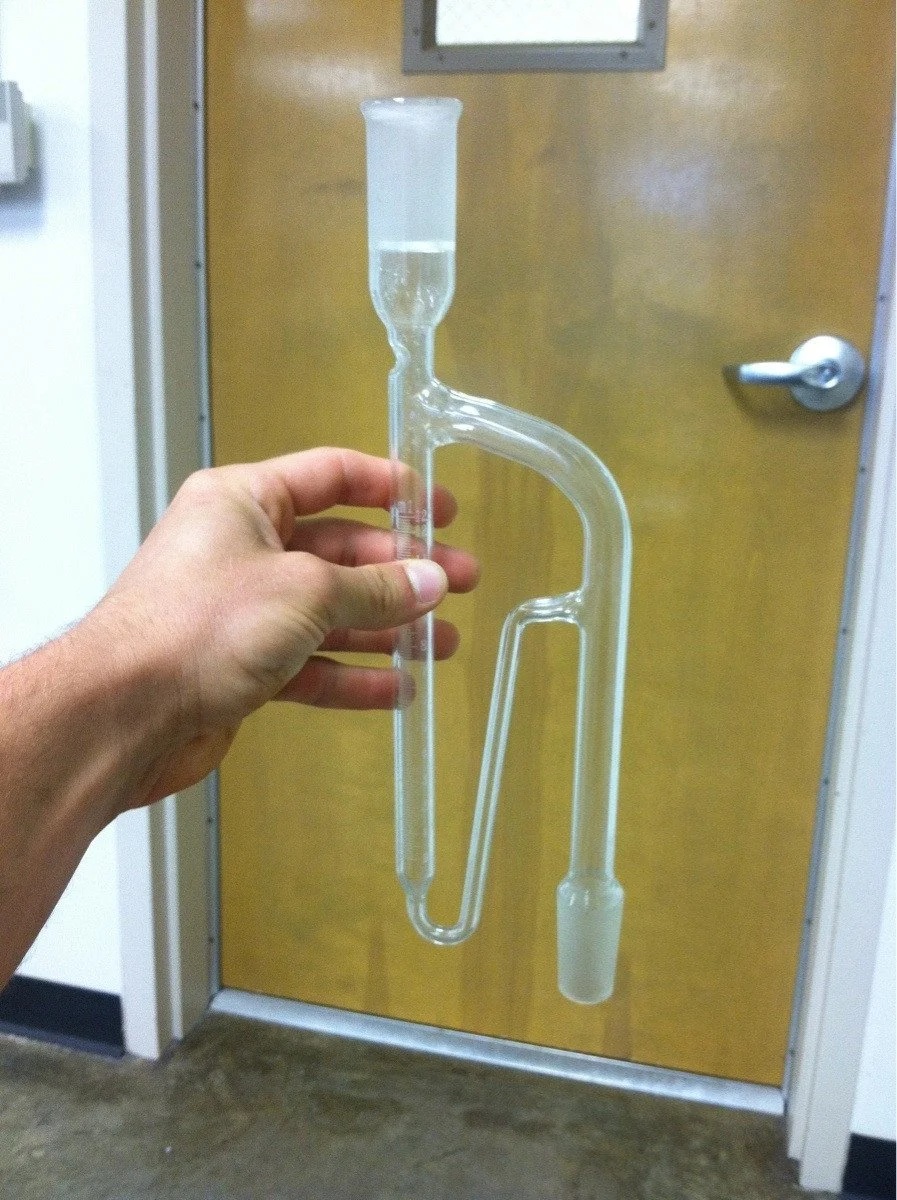
Насадка Дина-Старка для тяжелых жидкостей |

|
|
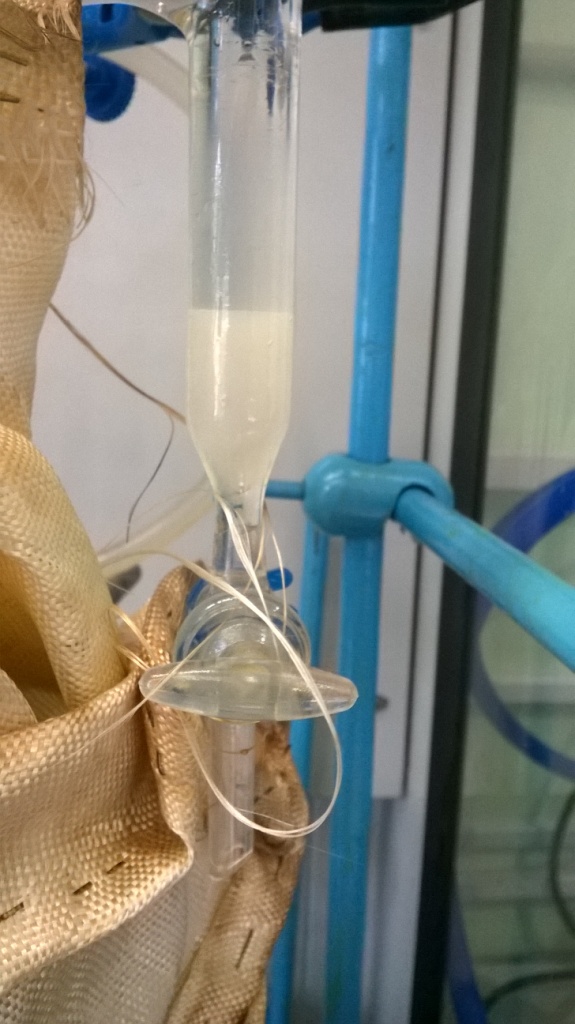
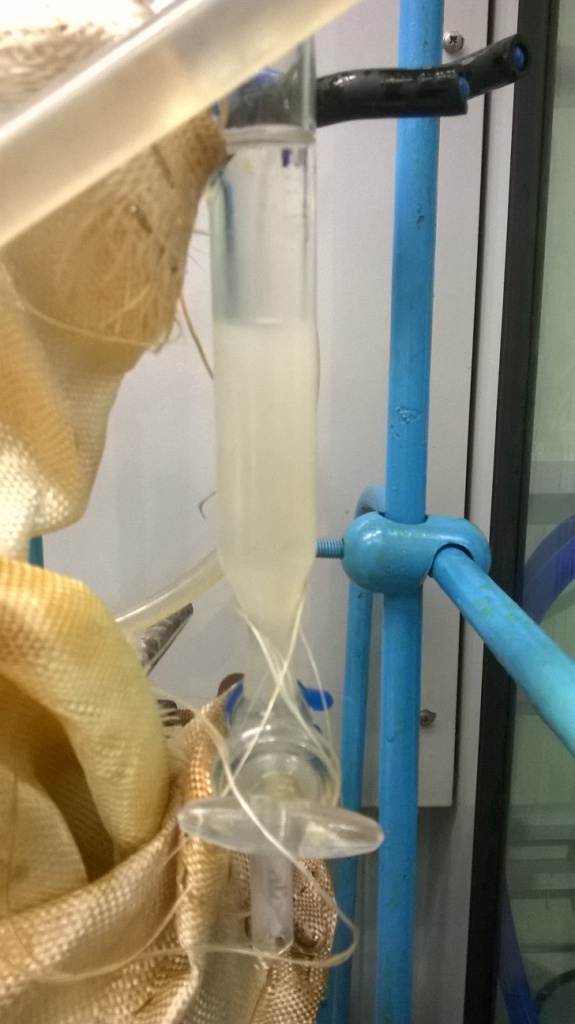
Но вернемся к нашим боранам. Точнее, не к гидридам бора, а к имидазолинам. В лаборатории долго стояла двухлитровая колба с недоваренным аминоэтилалкилимидазолином: часть воды из реакционной смеси еще предстояло отогнать. Сколько? Неизвестно. Посчитать, сколько нужно отогнать воды теоретически, - минутное дело, но не осталось записей, сколько воды из этой реакционной смеси уже отогнали. Решили имидазолин доварить. Добавил в колбу 100 мл толуола, поставил на плитку с магнитной мешалкой, присоединил насадку Дина-Старка, обратный холодильник, укутал нижнюю часть насадки (и колбу) стеклотканью, пустил воду в холодильник - и все. Осталось только ждать и следить за процессом отгонки.
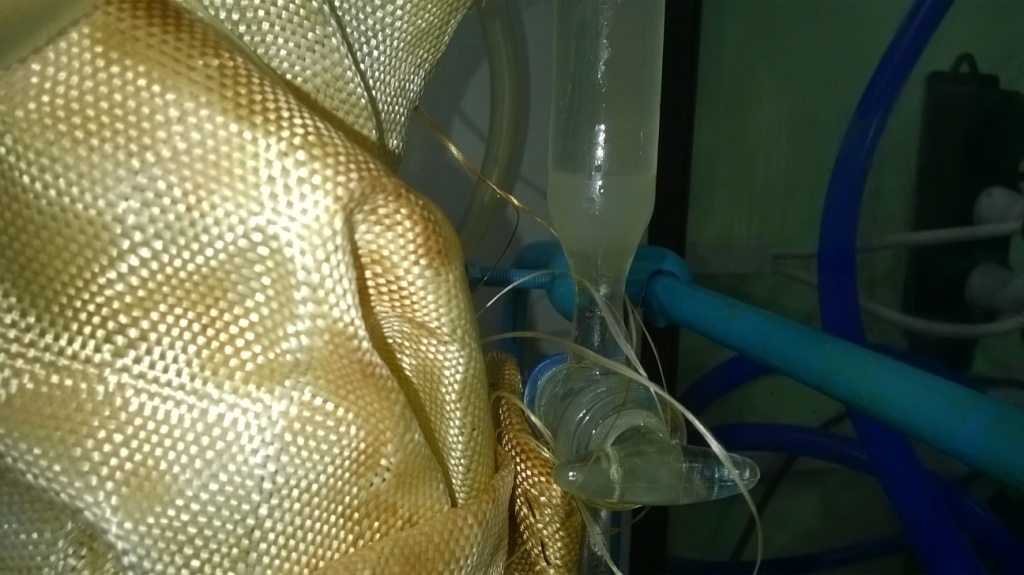
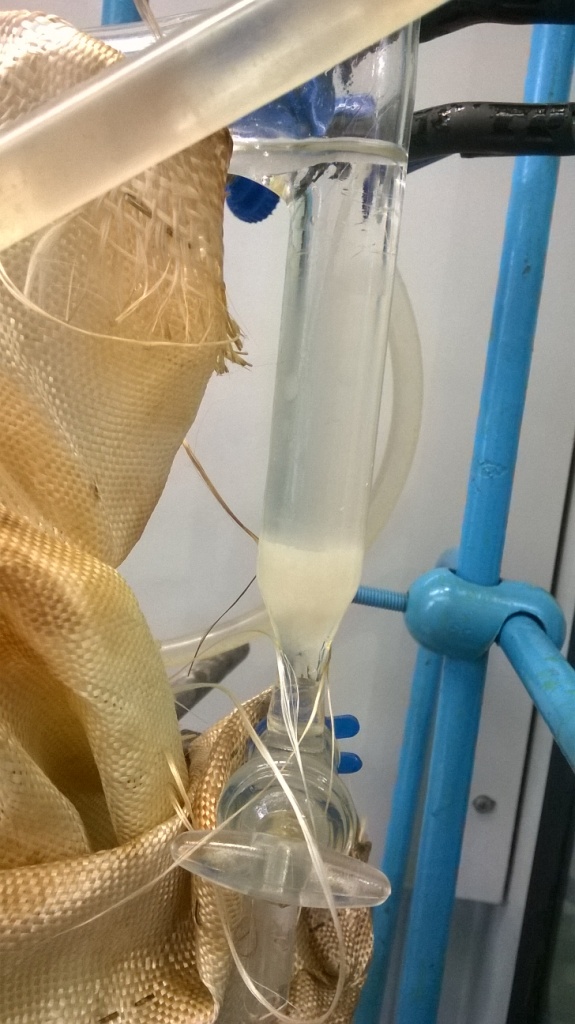
За чем следить? Было за чем. При слишком слабом нагреве пары (толуола и воды) конденсировались в нижней части насадки, не попадая холодильник: капли стекали назад в колбу (естественно безо всякого разделения). Плитка - слабая, поэтому для усиления нагрева приходилось тщательнее укутывать колбу и нижнюю часть насадки стеклотканью. Но и, когда нагрев был достаточный, не все проходило гладко. Иногда возникала ситуация, когда конденсат из холодильника, вместо того чтобы капать в нижнюю часть насадки - ту, что с краном (и там разделяться: вода - вниз, толуол - вверх и назад в колбу), просто стекал по стенкам... обратно в колбу. Т.е., никакого разделения также не было. Коллега сказал, что для этих целей нужен холодильник с выступающим вниз "носиком" шлифа (чтобы место, где конденсат стекает из холодильника, не контактировало со стенкой насадки). Но у нас такого холодильника не было. Проблему решили, вставив внутрь насадки стеклянную палочку: жидкость по палочке стекала из холодильника в нижнюю часть насадки. (Забыл сказать: все стеклянные палочки оказались слишком короткими, поэтому на дно насадки набросал немного колец Рашига - в качестве подставки для палочки.) В конце концов, отгонка воды прекратилась и стал конденсироваться только прозрачный толуол. Синтез закончен. |

|

|

|
|
|

|
|

|

|
|

|

|
|

|

|

|

|

|
|
Комментарии
К1
Грубая ошибка, это совершенно разные соединения.Гидросульфит сухой получают так: NaHCO3+SO2=NaHSO3+CO2 Метабисульфит (пиросульфит) Na2S2O5 получается выпариванием водного раствора NaHSO3: 2NaHSO3=Na2S2O5+H2O При растворении в воде реакция вроде везде описано обратима. По личным ощущениям - многие реакции присоединения к =C=O связи у меня великолепно шли с NaHSO3 и совершенно не шли с Na2S2O5, после нескольких промахов пиросульфит не использую. |