Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
1. «Алкалоид» Оптически неактивный алифатический алкалоид Х, который можно в
одну стадию синтезировать из триметиламина, впервые был выделен из желчи. В
водных растворах Х является сильным электролитом. При растворении 1,21 г
вещества Х в соответствующем количестве воды образуется 1 л раствора А, рН
которого равен 12,0; плотность 1,00 г/см3, а температура замерзания на 0,0372 К ниже
температуры замерзания воды (криоскопическая константа воды 1,86). Вследствие
прокаливания 1,21 г Х с избытком оксида меди(ІІ) образовалась газовая смесь (при
150°С и давлении 1 атм ее объем был равен V0), которую последовательно пропустили
через концентрированную серную кислоту (объем при 110°С и давлении 1 атм ее
объем был равен V1) и через раствор гидроксида калия (объем при 80°С и таком же
давлении стал V2), причом V0 : V1 : V2 = 31,156 : 11,933 : 1,000.
1) Какие вещества относят к алкалоидам?
2) Определите структурную формулу Х и назовите его.
3) Рассчитайте рН раствора, полученного при смешивании 50 мл раствора А с 60 мл раствора уксусной кислоты с концентрацией 0,015 моль/л (рКа уксусной кислоты 4,76).
4) Какие реактивы необходимы для синтеза Х из триметиламина в одну стадию?
В расчетах используйте значения атомных масс, округленные до целых чисел.
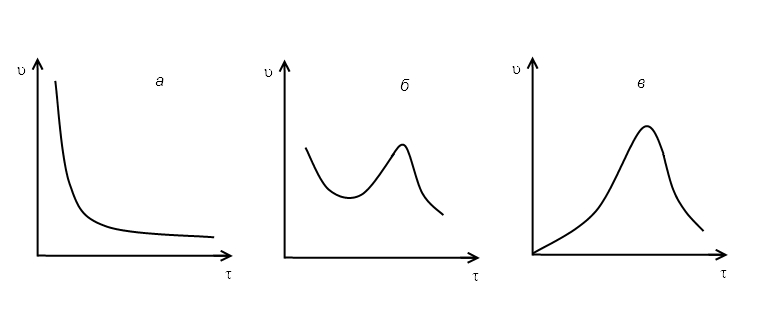
2.«Бешеная скорость» Могут ли наблюдаться в эксперименте приведенные ниже на рис. а-в виды зависимостей скорости гомогенной реакции (v) от времени (t)? Если да, приведите по одному примеру таких реакций.
3. «Чемпионат по титрованию» Ниф-Ниф, Наф-Наф и Нуф-Нуф определяли концентрацию раствора фосфорной кислоты, соревнуясь в точности результатов. Каждый из них использовал мерную посуду, позволяющую измерять объем с относительной погрешностью 0,5%, и один и тот же раствор гидроксида натрия с молярной концентрацией 0,0250 моль/л. Для титрования отбирали по 20,0 мл раствора кислоты, а для определения конечной точки титрования Ниф-Ниф выбрал индикатор метиловый оранжевый (интервал рН перехода окраски 3,0–4,4), Наф-Наф – тимолфталеин, синяя окраска которого, по данным И.Кольтгофа, начинает появляться при рН 9,7. Нуф-Нуф решил воспользоваться потенциометрическим прибором, позволяющим измерять рН с погрешностью ±0,02.
1) Если концентрация раствора фосфорной кислоты равна 0,0080 моль/л, какой объем титранта добавят Ниф-Ниф и Наф-Наф к моменту, когда изменится окраска индикатора?
2) Если Ниф-Ниф и Наф-Наф одинаково хорошо владеют приемами титрования и имеют нормальное цветовое зрение, кто из них может получить более точный результат? Подтвердите ответ расчетными оценками погрешностей, считая, что погрешность визуального определения рН составляет ±0,5.
3) Какое значение рН получилось у Нуф-Нуфа после добавления 10,0 мл титранта? При каком значении рН кислота будет полностью оттитрована до гидрофосфата? Нуф-Нуф закончил титрование при этом значении рН и утверждает, что погрешность индикации в этом случае отсутствует. Прав ли он?
4) Предложите методику титрования фосфорной кислоты как трехосновной в водном растворе.
Количественные оценки получите на основе использования концентрационно-логарифмической диаграммы. Значения логарифмов концентрационных констант диссоциации фосфорной кислоты:
lg Ka1 = -2,148 ± 0,001; lg Ka2 = -7,199 ± 0,002; lg Ka3 = -12,35 ± 0,02.
4. «Встреча с Гиллеспи и Бете»
1) Укажите характер изменения валентных углов в следующих рядах:
а) NH4+, NH3, NH2-
б) PH3, PF3, PCl3
в) [Ag(NH3)2]+, [Cu(NH3)4]2+, [Co(NH3)6]3+, [Co(NH3)6]2+.
2) В группе б) обсудите характер и причины изменения полярности молекул и энергий связи.
3) Укажите характер гибридизации центральных ионов комплексных частиц, которые указаны в группе в).
4) Укажите число неспаренных электронов в комплексных катионах и оцените их магнитные моменты.
5. «Фугитивность»
Студенты разные важны,
Студенты разные нужны.
Хорош студент, который знает,
Что "фугитивность" означает.
1) Объясните смысл понятия "фугитивность", где и для чего его используют?
2) 1 моль NH3 при Р = 40 атм и Т = 423 К занимает объем 0,769 л. Рассчитайте значение фугитивности.
Универсальная газовая постоянная R = 8,314 Дж•моль-1•К-1 = 0,082 л•атм•моль-1•К-1.
6. «Полосы и сигналы...» В результате взаимодействия бензальдегида с ацетилацетоном и ацетатом аммония в спиртовой среде получено соединение А (C17H19NO2), ИК спектр которого содержал полосы поглощения при 3310, 1670, 1630 и 1570 см-1. Кипячение соединения А с эквимолярным количеством гидроксиламина в спирте привело к образованию соединения В, в масс-спектре которого присутствовал пик молекулярного иона с m/z 284, а спектр ПМР содержал сигналы со значениями d, м. д.: 6,9–7,4 (5H, м), 4,82 (1Н, д, J = 2.3 Гц), 4,49 (1Н, с), 3,46 (1Н, д), 2,46 (3Н, с), 2,06 (3Н, с), 1,96 (3Н, с), 1,45 (3Н, с).
1) Установить строение соединений А и В, написать схему и механизм их образования.
2) Произведите отнесение наличие полос в ИК-спектре и сигналов в спектре ПМР.
3) Что можно сказать о стереохимии соединения В? Предскажите стереохимию продукта В на основании механизма реакции. Подтверждается ли предполагаемый результат данными ПМР? Как можно экспериментально подтвердить стереохимию данного соединения?
7. «Море» Ларс Гуннар Силлен у 60-х годах ХХ ст. исследовал океан как равновесную химическую систему. В первом приближении модель океана можно получить, смешав HCl, H2O, KOH, Al(OH)3 и SiO2 и дождавшись, когда система достигнет равновесного состояния. При разнообразных соотношениях количеств компонентов в состоянии равновесия одновременно существуют такие фазы: газовая (в основном пары Н2О), водный раствор, кварц, каолинит Al2Si2O5(OH)4 и калиевая слюда KAl3Si3O10(OH)2.
1) Напишите уравнение гетерогенной реакции превращения слюды в каолинит. Рассмотрев эту реакцию и учитывая условие электронейтральности фаз, объясните, как изменится значение рН водной фазы при введении в ситему а) КОН, б) HCl (Т = const)?
2) Приняв, что в равновесии с водным раствором и атмосферным воздухом находится донная фаза FeOOH, оцените общую (суммарную) концентрацию растворенных форм железе.
3) Какие выводы можно сделать. Вашу оценку с результатами измерений, согласно которым концентрация в океане растворимых форм железа ~10-7 моль/л?
Справочные данные: рН океанической воды равен 8,1;
8. «Алмаз»
Алмаз и графит в технике очень нужны,
Но при обычных условиях они не дружны.
Алмаз блестит, сверкает,
Прекрасных женщин украшает.
3) В.Н.Каразин превращением графита в алмаз занимался,
Да эксперимент у него не получался.
Вы сможете найти одну из причин неудачи,
Разобравшись в решении такой задачи:
Сохранив условие изотермичности процесса в п. 2), оцените давление, при котором алмаз и графит находятся в равновесии. Разность мольных объемов графита и алмаза Vалм - Vграф = -1,91 см3•моль-1 и не зависит от давления.
(bestnet.ua/chemistry/index.html, перевод с украинского)
1) Какие вещества относят к алкалоидам?
2) Определите структурную формулу Х и назовите его.
3) Рассчитайте рН раствора, полученного при смешивании 50 мл раствора А с 60 мл раствора уксусной кислоты с концентрацией 0,015 моль/л (рКа уксусной кислоты 4,76).
4) Какие реактивы необходимы для синтеза Х из триметиламина в одну стадию?
В расчетах используйте значения атомных масс, округленные до целых чисел.
2.«Бешеная скорость» Могут ли наблюдаться в эксперименте приведенные ниже на рис. а-в виды зависимостей скорости гомогенной реакции (v) от времени (t)? Если да, приведите по одному примеру таких реакций.

3. «Чемпионат по титрованию» Ниф-Ниф, Наф-Наф и Нуф-Нуф определяли концентрацию раствора фосфорной кислоты, соревнуясь в точности результатов. Каждый из них использовал мерную посуду, позволяющую измерять объем с относительной погрешностью 0,5%, и один и тот же раствор гидроксида натрия с молярной концентрацией 0,0250 моль/л. Для титрования отбирали по 20,0 мл раствора кислоты, а для определения конечной точки титрования Ниф-Ниф выбрал индикатор метиловый оранжевый (интервал рН перехода окраски 3,0–4,4), Наф-Наф – тимолфталеин, синяя окраска которого, по данным И.Кольтгофа, начинает появляться при рН 9,7. Нуф-Нуф решил воспользоваться потенциометрическим прибором, позволяющим измерять рН с погрешностью ±0,02.
1) Если концентрация раствора фосфорной кислоты равна 0,0080 моль/л, какой объем титранта добавят Ниф-Ниф и Наф-Наф к моменту, когда изменится окраска индикатора?
2) Если Ниф-Ниф и Наф-Наф одинаково хорошо владеют приемами титрования и имеют нормальное цветовое зрение, кто из них может получить более точный результат? Подтвердите ответ расчетными оценками погрешностей, считая, что погрешность визуального определения рН составляет ±0,5.
3) Какое значение рН получилось у Нуф-Нуфа после добавления 10,0 мл титранта? При каком значении рН кислота будет полностью оттитрована до гидрофосфата? Нуф-Нуф закончил титрование при этом значении рН и утверждает, что погрешность индикации в этом случае отсутствует. Прав ли он?
4) Предложите методику титрования фосфорной кислоты как трехосновной в водном растворе.
Количественные оценки получите на основе использования концентрационно-логарифмической диаграммы. Значения логарифмов концентрационных констант диссоциации фосфорной кислоты:
lg Ka1 = -2,148 ± 0,001; lg Ka2 = -7,199 ± 0,002; lg Ka3 = -12,35 ± 0,02.
4. «Встреча с Гиллеспи и Бете»
1) Укажите характер изменения валентных углов в следующих рядах:
а) NH4+, NH3, NH2-
б) PH3, PF3, PCl3
в) [Ag(NH3)2]+, [Cu(NH3)4]2+, [Co(NH3)6]3+, [Co(NH3)6]2+.
2) В группе б) обсудите характер и причины изменения полярности молекул и энергий связи.
3) Укажите характер гибридизации центральных ионов комплексных частиц, которые указаны в группе в).
4) Укажите число неспаренных электронов в комплексных катионах и оцените их магнитные моменты.
5. «Фугитивность»
Студенты разные важны,
Студенты разные нужны.
Хорош студент, который знает,
Что "фугитивность" означает.
1) Объясните смысл понятия "фугитивность", где и для чего его используют?
2) 1 моль NH3 при Р = 40 атм и Т = 423 К занимает объем 0,769 л. Рассчитайте значение фугитивности.
Универсальная газовая постоянная R = 8,314 Дж•моль-1•К-1 = 0,082 л•атм•моль-1•К-1.
6. «Полосы и сигналы...» В результате взаимодействия бензальдегида с ацетилацетоном и ацетатом аммония в спиртовой среде получено соединение А (C17H19NO2), ИК спектр которого содержал полосы поглощения при 3310, 1670, 1630 и 1570 см-1. Кипячение соединения А с эквимолярным количеством гидроксиламина в спирте привело к образованию соединения В, в масс-спектре которого присутствовал пик молекулярного иона с m/z 284, а спектр ПМР содержал сигналы со значениями d, м. д.: 6,9–7,4 (5H, м), 4,82 (1Н, д, J = 2.3 Гц), 4,49 (1Н, с), 3,46 (1Н, д), 2,46 (3Н, с), 2,06 (3Н, с), 1,96 (3Н, с), 1,45 (3Н, с).
1) Установить строение соединений А и В, написать схему и механизм их образования.
2) Произведите отнесение наличие полос в ИК-спектре и сигналов в спектре ПМР.
3) Что можно сказать о стереохимии соединения В? Предскажите стереохимию продукта В на основании механизма реакции. Подтверждается ли предполагаемый результат данными ПМР? Как можно экспериментально подтвердить стереохимию данного соединения?
7. «Море» Ларс Гуннар Силлен у 60-х годах ХХ ст. исследовал океан как равновесную химическую систему. В первом приближении модель океана можно получить, смешав HCl, H2O, KOH, Al(OH)3 и SiO2 и дождавшись, когда система достигнет равновесного состояния. При разнообразных соотношениях количеств компонентов в состоянии равновесия одновременно существуют такие фазы: газовая (в основном пары Н2О), водный раствор, кварц, каолинит Al2Si2O5(OH)4 и калиевая слюда KAl3Si3O10(OH)2.
1) Напишите уравнение гетерогенной реакции превращения слюды в каолинит. Рассмотрев эту реакцию и учитывая условие электронейтральности фаз, объясните, как изменится значение рН водной фазы при введении в ситему а) КОН, б) HCl (Т = const)?
2) Приняв, что в равновесии с водным раствором и атмосферным воздухом находится донная фаза FeOOH, оцените общую (суммарную) концентрацию растворенных форм железе.
3) Какие выводы можно сделать. Вашу оценку с результатами измерений, согласно которым концентрация в океане растворимых форм железа ~10-7 моль/л?
Справочные данные: рН океанической воды равен 8,1;
| FeOOH + 3H+ = Fe3+ + 2H2O | lg K = 3,96 | Fe3+ + H2O = FeOH2+ + H+ | lg K = -3,05 |
| FeOH2+ + H2O = Fe(OH)2+ + H+ | lg K = -3,26 | 2Fe3+ + 2H2O = Fe2(OH)24+ + 2H+ | lg K = -2,91 |
| Fe3+ + e- = Fe2+ | lg K = 13,0 | O2 + 2H2O + 4e- = 4OH- | E0 = 0,40 B |
8. «Алмаз»
... Так бриллиант не видим нам,
Пока он гранями не заиграл в алмазе.
В.В. Брюсов
Пока он гранями не заиграл в алмазе.
В.В. Брюсов
Алмаз и графит в технике очень нужны,
Но при обычных условиях они не дружны.
Алмаз блестит, сверкает,
Прекрасных женщин украшает.
3) В.Н.Каразин превращением графита в алмаз занимался,
Да эксперимент у него не получался.
Вы сможете найти одну из причин неудачи,
Разобравшись в решении такой задачи:
Сохранив условие изотермичности процесса в п. 2), оцените давление, при котором алмаз и графит находятся в равновесии. Разность мольных объемов графита и алмаза Vалм - Vграф = -1,91 см3•моль-1 и не зависит от давления.