
Обугливание сахара концентрированной серной кислотой
















| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 4 2013 Журнал Химиков-Энтузиастов |
Обугливание сахара концентрированной серной кислотой В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Концентрированная серная кислота - сильный водоотнимающий агент. Она способна не просто поглощать воду и ее пары, но и отнимать у веществ т.н. конституционную воду, которая "содержится" в них в виде изолированных групп -Н и -ОН. Например, при нагревании этилового спирта с серной кислотой в мягких условиях образуется диэтиловый эфир:
C2H5-OH + H-OC2H5 => C2H5-O-C2H5 + H-O-H
При более высокой температуре образуется этилен: C2H5-OH => H-O-H + CH2=CH2
Углеводы серная кислота способна обугливать уже при комнатной температуре - на этом основан красивый опыт "Серная кислота обугливает сахар". Приведем описание из практикума Рипан Р. Четяну И. Руководство к практическим работам по неорганической химии (1965) [ссылка] При смешивании стеклянной палочкой 30 г сахарного песку, слегка смоченного водой, с 30 мл концентрированной серной кислоты бурно протекает реакция обугливания сахара. Опыт проводят в химическом стакане емкостью 250-300 мл, помещенном в сосуд с песком или водой. Дегидратация глюкозы и сахарозы в этом случае протекает по уравнению C6H12O6 => 6C + 6H2O
C12H22O11 => 12C + 11H2O Благодаря выделяющимся при реакции парам воды обугливающаяся масса вспучивается наподобие черной пены. В стакан на 300 мл я поместил 30 г сахара, который предварительно растер в ступке (до состояния сахарной пудры). Предварительно увлажнять сахар не стал. В цилиндр налил 30 мл серной кислоты (согласно приведенному выше описанию) и начал добавлять кислоту в стакан с сахаром, перемешивая содержимое стеклянной палочкой. Однако когда я добавил 20 мл кислоты, масса стала достаточно жидкой на вид, и я решил, что кислоты хватит. Содержимое стакана стало сначала желтым, затем бурым и, наконец, черным. Примерно через две минуты началась бурная реакция. Масса стала вспучиваться и подниматься вверх. Активно выделялся белый пар. Запахло аэрозолем серной кислоты, сернистым газом и, как утверждает мой коллега, муравьиной кислотой. Параллельно с дегидратацией (обезвоживанием) сахара происходит окисление угля и сахара - этим и объясняется образование сернистого газа (и, возможно, муравьиной кислоты). Несмотря на бурную реакцию, черная масса так и не достигла краев стакана - сахара явно было мало. Во втором эксперименте я взял 60 г растертого сахара (водой не смачивал) и 30 мл серной кислоты. В этот раз до начала бурной реакции прошло примерно две с половиной минуты. Черная масса вышла за пределы стакана, хотя под конец она росла довольно медленно. После прекращения реакции обугленную массу удалось в целости вынуть из стакана. Третий эксперимент провел не в стакане, а в мерном цилиндре на 100 мл. Взял 50 г растертого сахара и 25 мл концентрированной серной кислоты. Опыт прошел аналогично, но менее эффектно. Разница заключалась в том, что когда черная масса достигла верха цилиндра, она оставалась еще жидкой и частично стекла вниз. |

Обугливание сахара концентрированной серной кислотой |

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

Обугливание сахара концентрированной серной кислотой |

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

Обугливание сахара концентрированной серной кислотой |

|

|

|

|

|

|

|

|

|

|

|

|

|

|
|
Возможно, для ускорения начала реакции сахарный песок все-таки целесообразно увлажнить водой (при контакте воды с серной кислотой произойдет разогрев, что ускорит обугливание сахара), но добавить в смесь воду у меня рука не поднялась.
Уже после опытов в другой книге - О.І. Астахов Цікаві роботи з хімії (Занимательные работы по химии) [ссылка] я увидел описание, в котором рекомендуют брать количества веществ, близкие к тем, что я использовал (и опять же сахар рекомендуют увлажнять): Капризное обугливание сахара Насыпьте 40 г растертого в мелкий порошок сахара в химический стакан емкостью 100 мл. Смешайте сахар с 3-4 мл воды. Добавьте к полученной массе 20-25 мл концентрированной серной кислоты (d=1.84) и снова хорошо перемешайте массу стеклянной палочкой. Палочку не вынимайте. Через несколько минут температура смеси повышается, смесь потемнеет и образуется пушистая масса, которая "вырастает" из стаканчика. Это - пористый уголь. Его образование объясняется дегидратацией сахара серной кислотой C12H22O11 => 12C + 11H2O Кроме того, происходит восстановление концентрированной серной кислоты углем: 2H2SO4 + C = CO2 + 2SO2 + 2H2O 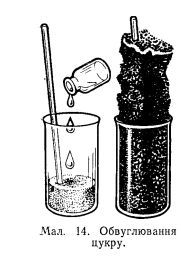 Если у вас нет концентрированной серной кислоты, для этого опыта вполне подойдет упаренный электролит для свинцовых аккумуляторов. Он представляет собой разбавленный раствор серной кислоты. Электролит упаривают до прекращения активного кипения и начала образования густых белых паров. Делать эту процедуру можно под хорошей тягой или на улице, но, ни в коем случае не в жилой квартире. Аэрозоль серной кислоты вдыхать недопустимо. Кстати, в свое время я пробовал добавлять к сахару еще горячую серную кислоту (которая не успела остыть после упаривания) - реакция начиналась быстро, без зазора в несколько минут, но работая с горячей кислотой нужно быть крайне осторожным. Попутно отмечу, что если вам на одежду или обувь попадет разбавленная серная кислота (например, тот же электролит), в большинстве случаев дырки сразу не будет, но со временем часть воды испарится и на вашей одежде (обуви) начнут расти дырки - все больших размеров. Я в таких случаях смачивал место попадания кислоты ваткой с аммиаком - это останавливало рост дырок (или даже предотвращало их образование), но аммиак может оказаться далеко не безразличным к некоторым красителям, которыми окрашивают ткани. |
Обугливание сахара концентрированной серной кислотой В.Н. Витер |
|
Обугливание сахара концентрированной серной кислотой |
||