Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
При смешивании концентрированной серной кислоты и воды выделяется много тепла. Для химика этот факт очень важен, поскольку и в лаборатории, и в промышленности часто приходится готовить разбавленные растворы серной кислоты. Для этого нужно смешивать концентрированную серную кислоту с водой - не всегда, но часто.
Как смешать концентрированную серную кислоту и воду?
Во всех учебниках и практикумах настоятельно рекомендуют лить серную кислоту в воду (тонкой струйкой и при хорошем перемешивании) - а не наоборот: нельзя лить воду в концентрированную серную кислоту!
Почему? Серная кислота более тяжелая, чем вода.
Если лить кислоту тонкой струйкой в воду, то кислота опустится на дно. Тепло, которое выделится при смешивании, рассеется - пойдет на нагрев всей массы раствора, поскольку над слоем кислоты, которая опустилась на дно сосуда, расположено большое количество воды.
Тепло рассеется, раствор нагреется - и ничего плохого не произойдет, особенно, если в процессе добавлении кислоты к воде жидкость хорошо перемешивать.
А что будет, если сделать неправильно, - в концентрированную серную кислоту добавить воду? Когда первые порции воды попадут в серную кислоту, они останутся на поверхности (поскольку вода легче, чем концентрированная серная кислота). Выделится много тепла, которое пойдет на нагрев маленького количества воды.
Вода резко вскипит, в результате полетят брызги серной кислоты и образуется едкий аэрозоль. Эффект может быть примерно такой, как при добавлении воды на горячую сковородку с маслом. Брызги серной кислоты могут попасть в глаза, на кожу и одежду. Аэрозоль серной кислоты не только очень неприятен при вдыхании, но и опасен для легких.
Если стекло не термостойкое - сосуд может треснуть.
Поэтому во всех практикумах рекомендуют добавлять концентрированную серную кислоту к воде, а не наоборот!
Чтобы это правило было легче запомнить, придумывают специальные стишки вроде:
"Сначала вода, а потом кислота - иначе случиться большая беда!".
Используют также специальные фразы для запоминания - "мемы", например:
"Чай с лимоном".
Книги - хорошо, но решил заснять, как выглядит результат неправильного смешивания концентрированной серной кислоты и воды на практике.
Разумеется, со всеми мерами предосторожности: начиная от защитных очков, заканчивая использованием небольших количеств веществ.
Провел несколько экспериментов - я пробовал смешивать серную кислоту с водой (и правильно, и неправильно). Во обоих случаях наблюдался лишь сильный разогрев. А закипания, разбрызгивания, и подобного не происходило.
Для примера, опишу один из экспериментов, проведенный в пробирке. Концентрированной серной кислоты взял 20 мл, воды 5 мл. Обе жидкости комнатной температуры.
Начал добавлять к серной кислоте воду. Вода закипела лишь в момент, когда приливал первые порции воды к кислоте. Новые порции воды погасили кипение. Едкий аэрозоль полетел (к этому я был не готов, пришлось на несколько секунд отойти). Попробовал перемешать алюминиевой проволочкой (то, что было под рукой). Эффекта ноль. Измерил температуру термометром. Оказалось 80 градусов по Цельсию. Эксперимент удался едва ли.
Новый эксперимент провел в колбе: чтобы поверхность соприкосновения двух жидкостей была максимальной (это обеспечит более резкое выделение тепла), а толщина слоя воды над серной кислотой - минимальной. Воду добавлял не всю сразу, а небольшими порциями (чтобы тепло пошло на кипение воды, а не на нагрев всей массы воды).
Итак, в коническую колбу налил около 10-15 мл концентрированной серной кислоты. Воды использовал около 10 мл.
Пока готовился к опыту, кислота под палящим солнцем разогрелась до 36-37 градусов (что градусов на 20 выше, чем начальная температура кислоты в прошлом опыте). Вода в пробирке тоже слегка нагрелась, но не так сильно. Думаю, это сыграло большую роль в успехе опыта.
При добавлении основной порции воды в серную кислоту заметно летели брызги и едкий аэрозоль. К счастью, их сносило ветром, который дул с моей стороны, поэтому я даже ничего не ощутил.
В итоге, температура в пробирке поднялась выше 100 градусов!
Какие можно сделать выводы? Если нарушить правило, что нельзя добавлять воду к концентрированной серной кислоте, разбрызгивание происходит не всегда, но оно возможно - особенно, когда вода и кислота теплые. Особенно - если добавлять воду медленно, небольшими порциями и в широкой посуде.
При работе с бОльшими количествами воды и кислоты вероятность резкого разогрева и разбрызгивания возрастает (напоминаю: мы взяли всего несколько миллилитров).
Опыт, который демонстрирует, что нельзя добавлять воду в концентрированную серную кислоту, описан в практикуме авторов Рипан и Четяну [1].
Приведу цитату:
Если в концентрированную серную кислоту наливать воду, то первые капли воды, попавшие в нее, моментально превращаются в пар и из сосуда вылетают брызги жидкости. Это происходит по той причине, что вода, обладая небольшим удельным весом, не погружается в кислоту, а кислота ввиду малой теплоемкости не поглощает выделившейся теплоты. При вливании горячей воды наблюдается более сильное разбрызгивание серной кислоты.
Опыт. Смешивание воды с концентрированной Н2SO4. Стаканчик с концентрированной серной кислотой ставят на дно большого стакана, прикрытого воронкой. Теплую воду вливают при помощи пипетки (рис. 161). При вливании горячей воды внутренние стенки большого стакана и воронки моментально покрываются брызгами жидкости.
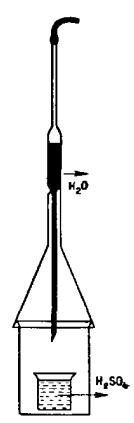
Рис. 161
За неимением стеклянной воронки можно воспользоваться картонной, внутрь которой вводят пипетку с водой.
Если в стакан с водой приливать по каплям или тонкой струей концентрированную серную кислоту, то можно заметить, как более тяжелая серная кислота опускается на дно стакана.
При смешивании концентрированной Н2SO4 со льдом можно одновременно наблюдать два явления: гидратацию кислоты, сопровождающуюся выделением тепла, и плавление льда, сопровождающееся поглощением тепла. Поэтому в результате смешивания можно наблюдать либо повышение, либо понижение температуры. Так, при смешивании 1 кг льда с 4 кг кислоты температура повышается почти до 100°, а при смешивании 4 кг льда с 1 кг кислоты температура снижается почти до -20°.

__________________________________________________
1 Р. Рипан, И. Четяну Руководство к практическим работам по неорганической химии [ссылка]
Как смешать концентрированную серную кислоту и воду?
Во всех учебниках и практикумах настоятельно рекомендуют лить серную кислоту в воду (тонкой струйкой и при хорошем перемешивании) - а не наоборот: нельзя лить воду в концентрированную серную кислоту!
Почему? Серная кислота более тяжелая, чем вода.
Если лить кислоту тонкой струйкой в воду, то кислота опустится на дно. Тепло, которое выделится при смешивании, рассеется - пойдет на нагрев всей массы раствора, поскольку над слоем кислоты, которая опустилась на дно сосуда, расположено большое количество воды.
Тепло рассеется, раствор нагреется - и ничего плохого не произойдет, особенно, если в процессе добавлении кислоты к воде жидкость хорошо перемешивать.
А что будет, если сделать неправильно, - в концентрированную серную кислоту добавить воду? Когда первые порции воды попадут в серную кислоту, они останутся на поверхности (поскольку вода легче, чем концентрированная серная кислота). Выделится много тепла, которое пойдет на нагрев маленького количества воды.
Вода резко вскипит, в результате полетят брызги серной кислоты и образуется едкий аэрозоль. Эффект может быть примерно такой, как при добавлении воды на горячую сковородку с маслом. Брызги серной кислоты могут попасть в глаза, на кожу и одежду. Аэрозоль серной кислоты не только очень неприятен при вдыхании, но и опасен для легких.
Если стекло не термостойкое - сосуд может треснуть.
Поэтому во всех практикумах рекомендуют добавлять концентрированную серную кислоту к воде, а не наоборот!
Чтобы это правило было легче запомнить, придумывают специальные стишки вроде:
"Сначала вода, а потом кислота - иначе случиться большая беда!".
Используют также специальные фразы для запоминания - "мемы", например:
"Чай с лимоном".
Книги - хорошо, но решил заснять, как выглядит результат неправильного смешивания концентрированной серной кислоты и воды на практике.
Разумеется, со всеми мерами предосторожности: начиная от защитных очков, заканчивая использованием небольших количеств веществ.
Провел несколько экспериментов - я пробовал смешивать серную кислоту с водой (и правильно, и неправильно). Во обоих случаях наблюдался лишь сильный разогрев. А закипания, разбрызгивания, и подобного не происходило.
Для примера, опишу один из экспериментов, проведенный в пробирке. Концентрированной серной кислоты взял 20 мл, воды 5 мл. Обе жидкости комнатной температуры.
Начал добавлять к серной кислоте воду. Вода закипела лишь в момент, когда приливал первые порции воды к кислоте. Новые порции воды погасили кипение. Едкий аэрозоль полетел (к этому я был не готов, пришлось на несколько секунд отойти). Попробовал перемешать алюминиевой проволочкой (то, что было под рукой). Эффекта ноль. Измерил температуру термометром. Оказалось 80 градусов по Цельсию. Эксперимент удался едва ли.
Новый эксперимент провел в колбе: чтобы поверхность соприкосновения двух жидкостей была максимальной (это обеспечит более резкое выделение тепла), а толщина слоя воды над серной кислотой - минимальной. Воду добавлял не всю сразу, а небольшими порциями (чтобы тепло пошло на кипение воды, а не на нагрев всей массы воды).
Итак, в коническую колбу налил около 10-15 мл концентрированной серной кислоты. Воды использовал около 10 мл.
Пока готовился к опыту, кислота под палящим солнцем разогрелась до 36-37 градусов (что градусов на 20 выше, чем начальная температура кислоты в прошлом опыте). Вода в пробирке тоже слегка нагрелась, но не так сильно. Думаю, это сыграло большую роль в успехе опыта.
При добавлении основной порции воды в серную кислоту заметно летели брызги и едкий аэрозоль. К счастью, их сносило ветром, который дул с моей стороны, поэтому я даже ничего не ощутил.
В итоге, температура в пробирке поднялась выше 100 градусов!
Какие можно сделать выводы? Если нарушить правило, что нельзя добавлять воду к концентрированной серной кислоте, разбрызгивание происходит не всегда, но оно возможно - особенно, когда вода и кислота теплые. Особенно - если добавлять воду медленно, небольшими порциями и в широкой посуде.
При работе с бОльшими количествами воды и кислоты вероятность резкого разогрева и разбрызгивания возрастает (напоминаю: мы взяли всего несколько миллилитров).
Опыт, который демонстрирует, что нельзя добавлять воду в концентрированную серную кислоту, описан в практикуме авторов Рипан и Четяну [1].
Приведу цитату:
Если в концентрированную серную кислоту наливать воду, то первые капли воды, попавшие в нее, моментально превращаются в пар и из сосуда вылетают брызги жидкости. Это происходит по той причине, что вода, обладая небольшим удельным весом, не погружается в кислоту, а кислота ввиду малой теплоемкости не поглощает выделившейся теплоты. При вливании горячей воды наблюдается более сильное разбрызгивание серной кислоты.
Опыт. Смешивание воды с концентрированной Н2SO4. Стаканчик с концентрированной серной кислотой ставят на дно большого стакана, прикрытого воронкой. Теплую воду вливают при помощи пипетки (рис. 161). При вливании горячей воды внутренние стенки большого стакана и воронки моментально покрываются брызгами жидкости.

Рис. 161
За неимением стеклянной воронки можно воспользоваться картонной, внутрь которой вводят пипетку с водой.
Если в стакан с водой приливать по каплям или тонкой струей концентрированную серную кислоту, то можно заметить, как более тяжелая серная кислота опускается на дно стакана.
При смешивании концентрированной Н2SO4 со льдом можно одновременно наблюдать два явления: гидратацию кислоты, сопровождающуюся выделением тепла, и плавление льда, сопровождающееся поглощением тепла. Поэтому в результате смешивания можно наблюдать либо повышение, либо понижение температуры. Так, при смешивании 1 кг льда с 4 кг кислоты температура повышается почти до 100°, а при смешивании 4 кг льда с 1 кг кислоты температура снижается почти до -20°.

Были взяты лед и концентрированная серная кислота с температурой около 0°С. При добавлении Н2SO4 ко льду температура сначала немного возрастает, но потом значительно понижается
(соотношение льда и кислоты не такое, как указано в цитате)
(соотношение льда и кислоты не такое, как указано в цитате)
__________________________________________________
1 Р. Рипан, И. Четяну Руководство к практическим работам по неорганической химии [ссылка]



















