Химия и Химики № 4 2021
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 4 2021 Журнал Химиков-Энтузиастов |
Эксперименты с магнием ч. 5, 6 Experiments with magnesium В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Магний и концентрированная серная кислота: просто добавь воды! / Magnesium and concentrated sulfuric acid: just add water!
Магний, который мы поместили в разбавленную серную кислоту, быстро растворился. А сам раствор послужил для экспериментов с катионом магния. Зато, магниевая стружка, помещенная в концентрированную серную кислоту, не растворилась: реакция началась и прекратилась. При нагреве реакция, сначала возобновилась, потом - прекратилась. Логичное объяснение: сульфат магния плохо растворим в концентрированной кислоте, что ведет к пассивации поверхности. Эксперимент #1 / Experiment #1 Поделился с коллегой. - Так добавь воды! - Ага, сейчас: ты знаешь, что я не боюсь (делал и не такое), но... Пока провожу эксперименты не в лаборатории, а на кухне. Лицо можно защитить маской из оргстекла, одежду - взять старую, но не хочу, чтобы обои сожгло брызгами кислоты. Ведь ясно же, что если: *при добавлении воды в концентрированную серную кислоту происходит сильный разогрев, вода остается на поверхности и вскипает, вызывая разбрызгивание серной кислоты; *разбавленная серная кислота реагирует с магнием бурно; то при добавлении воды в концентрированную серную кислоту с магнием реакция будет очень активной. Есть проблема - есть решение. Подобное я уже делал: взял большую стеклянную банку, на дно поставил перевернутый стакан, на него - стакан с концентрированной серной кислотой и магнием. Банку накрыл лотком из пенопласта. В лотке проделал отверстие и вставил сквозь него пластиковую пипетку с водой (сейчас такие пипетки называют "пипетка Пастера") - вот и все. При таком способе съемки очевидных проблем две: *стекло банки искажает картинку и дает блики от осветительной лампы; *в процессе реакции полетят брызги, выделится водяной пар - в результате банка запотеет изнутри, что ухудшит картинку [1]. Но для начала решил попробовать так. Включил съемку, добавил воду в кислоту. Ожидал бурной реакции с разбрызгиванием. Не исключал, что стакан упадет и разобьется, может быть, даже банка треснет: она нетермостойкая и может не выдержать резкого неравномерного нагрева. Произошедшее глобально можно описать словом: "разочарование". Сначала добавил примерно полмиллилитра воды. Выделился газ, пошипело-покипело, но несильно. Вскоре реакция стала затихать. Еще полмиллилитра - реакция снова пошла активно, но без намека на катастрофические процессы. Снова - постепенное угасание. Добавил больше миллилитра воды - реакция активизировалась, магниевая стружка, наконец, всплыла от пузырьков водорода. Только теперь реакция по интенсивности стала частично напоминать реакцию магния и разбавленной серной кислоты. Мелкие капельки воды оседали на стенках из-за конденсации пара: видимость медленно, но неумолимо ухудшалась. Знал бы, что реакция пройдет спокойно - обошелся бы без банки. Следующая порция воды - реакция пошла бурно, примерно, как с разбавленной кислотой. Со временем добавил еще воды. Внутренние стенки банки сильно запотели. Магний, наконец, растворился. В кислоте был заметный массивный осадок сульфата магния: т.е. пассивация продолжается даже после добавления воды, она просто уменьшилась, дав реакции начаться и пройти до конца. Достал стакан из банки, его содержимое представляло собой белую кашу (из-за осадка сульфата магния). Позже вспомнил, что подобный прием используется в химической технологии. Например, для разложения концентрата нефелина серной кислотой (нефелин - алюмосиликат калия и натрия, служит источником оксида алюминия - глинозема). Твердый нефелин смешивают с концентрированной серной кислотой, перемешивают все это в реакторе со шнеком - реакция почти не идет, потом резко добавляют воду. Начинается активная реакция, которая заканчивается за несколько секунд (пока смесь находится в шнеке). __________________________________________________ 1 Помню даже, что при съемке опыта "вулкан в стакане" (разложение бихромата аммония внутри большого стакана) специально нагревал стакан перед опытом (в сушильном шкафу), чтобы водяной пар, который образуется в ходе реакции, не конденсировался на холодном стекле. См. Вулкан в стакане (разложение бихромата аммония) [ссылка]. |

В стакане - магний в концентрированной серной кислоте. В пипетке - вода |

|

|

|

|

|

|

|

|

|

|
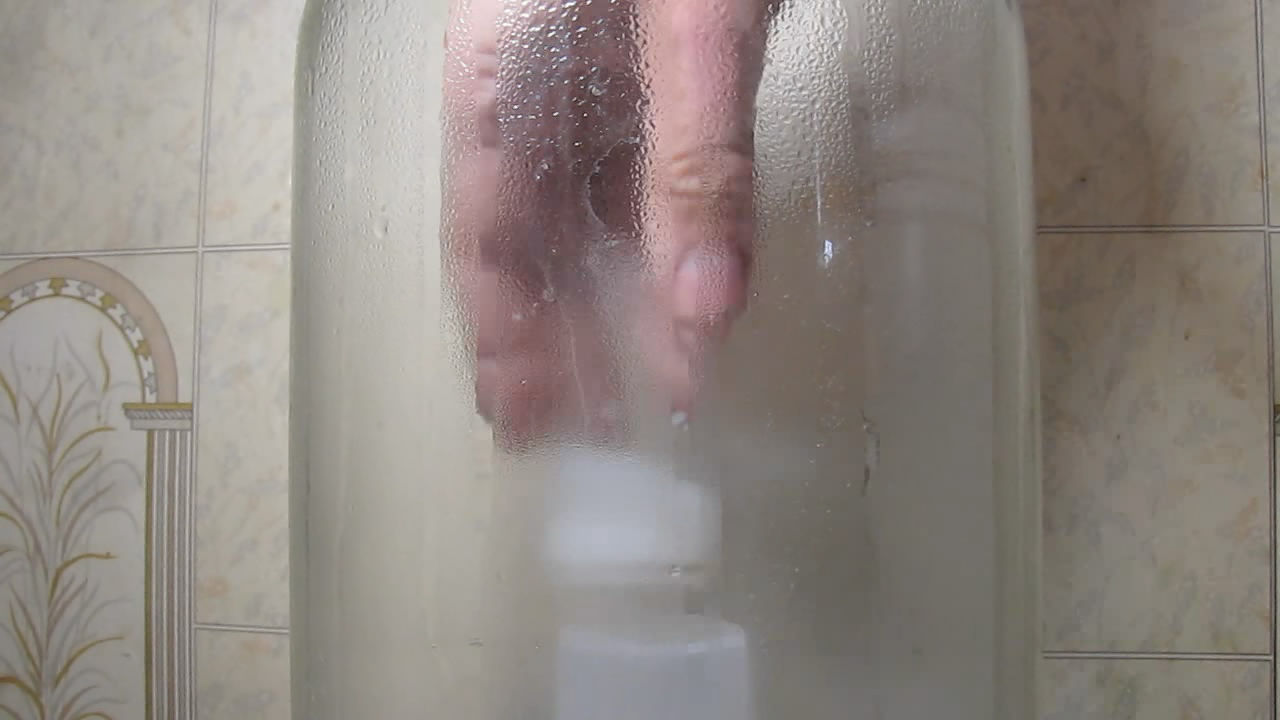
|

|

Магний и концентрированная серная кислота |

|

|

|

Реакция прекратилась |

Добавим воды |

|

|

|

|

|

|

|

Добавим еще одну магниевую стружку |

|

|

|

|

|

|

|
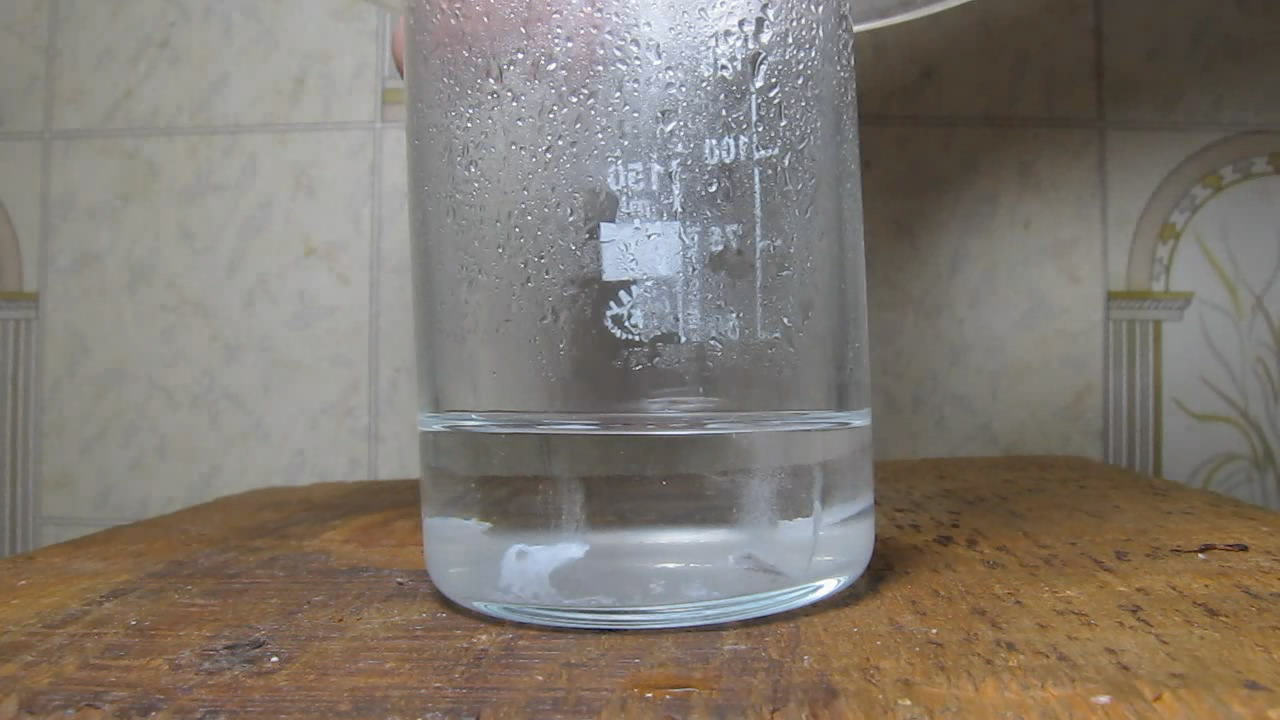
|

|
Эксперименты с магнием ч. 7 Experiments with magnesium В.Н. Витер |
|
Реакция магния с водой / Reaction of magnesium with water
Щелочные металлы бурно реагируют с водой: рубидий и цезий - со взрывом, калий - тоже взрывается. Натрий - воспламеняется и взрывается только если кусочек имеет достаточные размеры. Литий реагирует без взрыва, но бурно. Барий, стронций, кальций - тоже реагируют с водой, но менее активно. Алюминий и бериллий устойчивы по отношению к воде и воздуху: хотя эти металлы активные, их защищает прочная оксидная пленка на поверхности. Есть способ решить эту проблему - действие металлической ртути или ее солей на алюминий (на поверхности металла образуется амальгама, на которой оксидная пленка уже не держится, и алюминий начинает активно реагировать с водой и воздухом), но не буде отвлекаться. Магний по отношению к воде и воздуху занимает промежуточное положение между щелочными (щелочноземельными) металлами с одной стороны и алюминием (бериллием) с другой. В одном учебнике (а, может, в практикуме) прочитал, что магний не реагирует с холодной водой, но реагирует с горячей. Если добавить горячую воду с магнием фенолфталеин, раствор окрасится в малиновый цвет (признак щелочной реакции). Дело было еще в школе - название книги я не запомнил. Думал, что это учебник химии Ю.В. Ходаков, Д.А. Эпштейн, Р.А. Глориозов - Неорганическая химия 7-8 и 9 класс. (См. страницу Изучаем химию "с нуля" [ссылка]). Посмотрел - нет. В учебнике Г.Е. Рудзитис, Ф.Г. Фельдман - Химия 7-11 класс. ч.1, ч.2 этого тоже нет. А вообще я был неприятно удивлен, почти раздосадован: как мало материала давали в школьных учебниках! Например, в упомянутых книгах по магнию не было параграфа или даже подраздела параграфа. Так: отрывчатые сведения по всей книге. Я уже успел это забыть. Вспоминаю слова коллеги: - То рациональное, что дают в школе за учебный год, можно было, не напрягаясь, выучить за один месяц (не спеша и не мучая детей), но чем тогда заниматься в школе остальные восемь месяцев? Значит, про реакцию магния с водой я прочитал не в школьном учебнике, в другой книге. Важно то, что перед экспериментом я ожидал отсутствие реакции магния с холодной водой и умеренно-активное взаимодействие с горячей. Взял стакан с дистиллированной водой комнатной температуры и поместил в нее стружку магния (дистиллированная вода необходима, т.к. в водопроводной воде есть растворенные соли: они исказят пробу с фенолфталеином в случае горячей воды). Сразу же обнаружил интересный факт, хотя к химии он имел косвенное отношение. Для экспериментов по демонстрации поверхностного натяжения воды или флотации хорошо подходят изделия из магния (плотность 1.738 г/см3). В нашем случае - стружка. Магний легче алюминия, хотя монет из магния не делают (алюминиевые монеты, которые держатся поверхности воды и не тонут, - один из самых эффектных опытов). Стружка магния не просто хорошо плавает на поверхности воды, но в одном из экспериментов я не мог ее утопить (добиться погружения металла на дно) - это вам не стальная игла, для которой нужна специальная техника опыта, чтобы она плавала по поверхности воды. Руководствуясь предубеждениями, я планировал заснять магний под водой, чтобы показать, что с холодной водой реакция практически не идет (комнатная температура - около 20°С). Оказалось, что с поверхности магния начали выделяться пузырьки водорода: они были маленькие и их было мало, т.е., реакция хоть и медленно, но шла. Позже - уже после эксперимента по взаимодействию магния с горячей водой, попробовал еще раз (с холодной водой). Именно в этот раз немного намучился, пытаясь утопить стружку стеклянной палочкой. Попутно опять заметил маленькие пузырьки водорода. Добавил спиртовый раствор фенолфталеина - сразу же появилась четкая малиновая окраска, что подтвердило присутствие гидроксида магния - основания средней силы: 2Mg + 2H2O = Mg(OH)2 + H2 Гидроксид магния малорастворим, но все же его растворимости достаточно, чтобы дать малиновую окраску индикатора. Таким образом, при комнатной температуре водород тоже выделялся. А вдруг механизм образования гидроксида магния другой. Например, такой: 2Mg + O2 = 2MgO MgO + H2O = Mg(OH)2 Пузырьки газа? Но их было мало. Зато оксидная пленка на поверхности магния (который хранился на воздухе) есть всегда. Раз так, водород, который выделяется, нужно собрать - чтобы показать, что он образуется в заметном количестве. Взял небольшую пробирку, она оказалась из пластика, скорее всего - из оргстекла (полиметилметакрилат). В пробирку поместил магниевую стружку, до верху ее наполнил дистиллированной водой. Горлышко закрыл пальцем и перевернул, погрузив в заполненный водой стакан. Получилось с первого раза - в пробирку не попали пузырьки воздуха. Оставил реагировать (весь водород должен собираться в верхней части пробирки). Через 40 минут под перевернутым дном пробирки собралось несколько маленьких пузырьков водорода, поверхность магния покрылась пузырьками. Через 7 часов вверху пробирки образовался слой водорода миллиметра 4 высотой. Через 20 часов - слой водорода высотой 5-6 мм, через 30 часов - пузырек водорода увеличился, но непропорционально времени. Реакция замедляется? Уже во время просмотра видео обнаружил, что много пузырьков водорода, которые не успели всплыть, т.к. прилипли к поверхности пробирки, расположены не внутри, а на наружных стенках(!). При этом на поверхности стакана почти не было пузырьков (это не воздух, который выделился из воды: ДО опыта вода долгое время стояла). Т.е. водород в "лошадиных дозах" прошел через пластик пробирки. Впрочем, это не было неожиданностью: резиновый шарик, надутый водородом, за пару часов сдувается, как плотно его не завязывай: Н2 проходит сквозь полимерные стенки. Слышал даже про специальный состав, которым (в виде аэрозоля) обрызгивают стенки воздушных шариков изнутри, чтобы уменьшить утечку гелия из шарика (водород огне- и взрывоопасен, поэтому шарики, чтобы они поднимались вверх, надувают гелием; гелий тоже имеет высокую способность к диффузии). |

Магний и холодная вода (дистиллят) |

|

Наблюдалось слабое выделение водорода |

|

Добавим фенолфталеин |

|

|

Соберем водород в перевернутой пробирке с водой |

|

|

|

|

|

|

|

Много пузырьков водорода оказалось с внешней стороны пробирки |

|

|
|
Теперь реакция магния с горячей водой. Можно было поместить магний в стакан с дистиллированной водой и поставить греться на плитку. Проблема в том, что вода сама по себе закипит и выделение пузырьков пара замаскирует образование пузырьков водорода. Поэтому сначала нагрел воду до кипения, снял стакан с плитки, а только потом поместил в него магниевую стружку. С поверхности металла начали выделяться пузырьки водорода - с вполне заметной скоростью, но реакцию не назовешь активной. Поставил стакан на плитку - реакция активизировалась, но скоро возобновилось кипение воды. Добавил фенолфталеин. Раствор окрасился в малиновый цвет. Через некоторое время снял стакан с плитки. Пока он не остыл, можно было наблюдать образование пузырьков водорода - не особо интенсивное.
Вывод очевиден: магний по активности ближе к алюминию, чем к щелочным металлам. Кстати, магниевые аноды используются для защиты от коррозии в бойлерах: т.е., металл анода постоянно контактирует с водой, при этом пишут, что средний срок службы таких анодов порядка 2-х лет. |

Магний и горячая вода (дистиллят) |

|

|

|

Наблюдается выделение газа, но неинтенсивное |

|

Добавим фенолфталеин |

|

|

|
Эксперименты с магнием ч.8 Experiments with magnesium Феерверкер |
|
Магний и лед (горение смеси) / Magnesium and ice (burning of mixture)
Материал в продолжение темы. (Дошли руки разобраться в разных отснятых ранее экспериментах, какие ещё не успел нигде опубликовать). Итак, реакция магния с водой. Но на этот раз пиротехническая. Было использовано: 100 грамм магниевой стружки, и 75 грамм воды в твёрдом агрегатном состоянии (снег). Для запала использовал пиротехническую звёздку типа "тигриный хвост". Хотя, похоже, что данный состав не составит труда зажечь и обычной спичкой. |

Магний - 100 г |

Снег - 75 г |

Смешиваем |

|

|

|
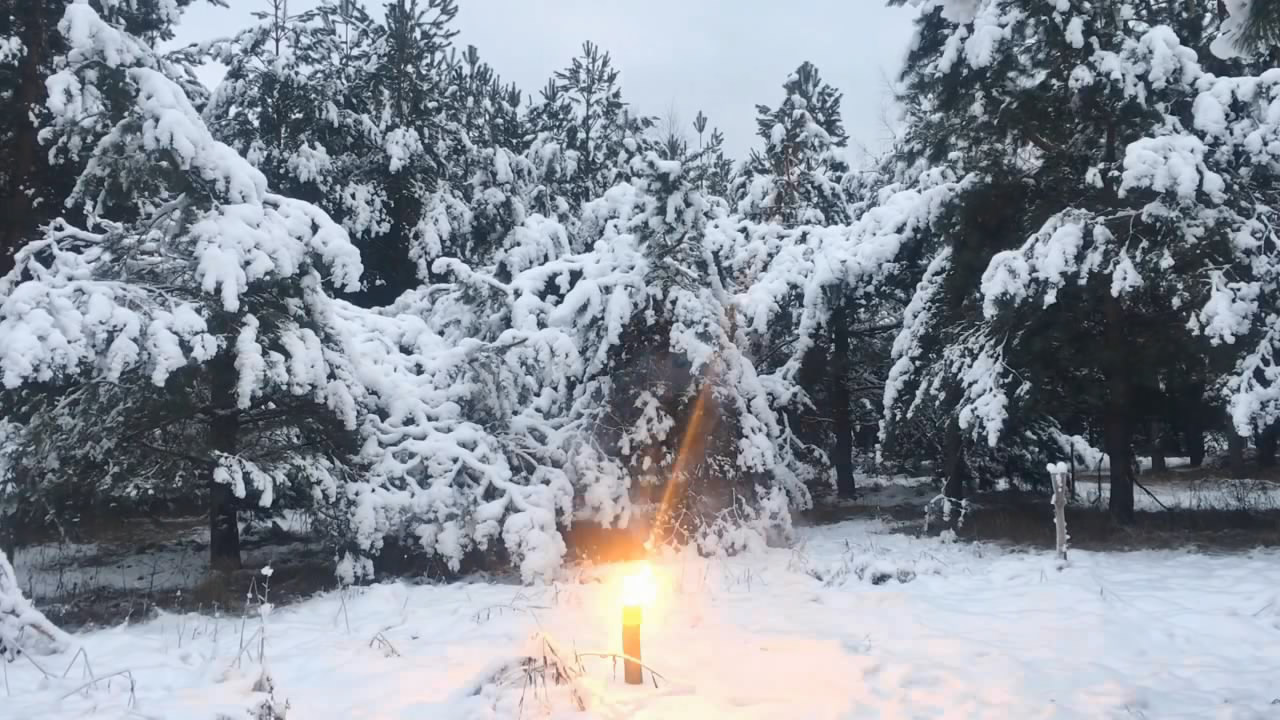
|

|

|

|

|

|

|

|