Химия и Химики № 4 2021
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 4 2021 Журнал Химиков-Энтузиастов |
Гидролиз (водопроводная вода) Hydrolysis (tap water) В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
В данном эксперименте мы продемонстрируем гидролиз воды. Первое предложение содержит явную ошибку (гидролиз - реакция разложения веществ водой), но даже в откровенной ерунде может быть зерно истины: для наблюдения гидролиза солей нам понадобится только вода (а еще - нагреватель и индикатор), но никаких дополнительных реактивов. Соли? Они уже есть в водопроводной воде - в растворенном виде.
В одном практикуме (увы, дело было давно, поэтому название вспомнить не удалось) я прочитал описание такого эксперимента - передаю своими словами по памяти: В стакан налейте водопроводной воды, прибавьте несколько капель раствора фенолфталеина. Вода в стакане останется бесцветной. Нагрейте воду до кипения. В результате нагревания усилится гидролиз растворенных в воде солей, и фенолфталеин окрасится в малиновый цвет. После охлаждения через некоторое время окраска индикатора исчезнет. Попробовал повторить этот эксперимент в немного измененном виде. В один стакан налил дистиллированную воду, в другой - водопроводную воду. В оба стакана добавил по несколько капель спиртового раствора фенолфталеина, перемешал. Вода в стаканах осталась бесцветной. Поместил стаканы на электрическую плитку, начал греть. Дистиллированная вода просто закипела: ее окраска в ходе эксперимента не изменилась. Логично. Водопроводная вода сначала оставалась бесцветной, но потом появился слабый розовый оттенок, который по мере нагревания стал усиливаться. Когда вода закипела, ее цвет стал малиновым, по ходу кипячения интенсивность окраски постепенно увеличивалась, пока содержимое стакана не стало интенсивно-малиновым. Переход от светло-розового до интенсивно-малинового цвета произошел не моментально: на это потребовалось несколько минут (когда кипение стало интенсивным, скорость увеличения интенсивности значительно возросла). Охладил, оставил стаканы стоять. Прошло семь часов, а водопроводная вода все еще интенсивно-малинового цвета: окраска немного ослабла, но не исчезла. Оставил на ночь - окраска еще ослабела, но все еще осталась интенсивной. Но полного исчезновения окраски фенолфталеина после охлаждения и стояния водопроводной воды (обещанного в практикуме) не произошло. Почему? Сказать по правде, это не стало неожиданностью. Какие ионы есть в водопроводной воде? В водопроводной воде присутствуют: натрий, калий, кальций и магний (опустим клинические случаи, вроде наличия в воде железа - ржавые трубы и даже наличия марганца). Из анионов - хлорид, сульфат, гидрокарбонат. Кальций и магний способны дать легенькое закисление (если они связаны с анионами сильных кислот), зато гидрокарбонат при нагревании разлагается, давая карбонат и углекислый газ. Углекислый газ улетает из кипящей воды, а карбонаты натрия и калия в результате последующего гидролиза дают щелочную среду. Настолько щелочную, что фенолфталеин окрашивается в малиновый цвет. Именно потому переход окраски фенолфталеина при нагревании водопроводной воды произошел не моментально, а плавно: по сути, мы наблюдали кинетику разложения аниона гидрокарбоната до карбоната и испарения углекислого газа из кипящего раствора. Обратный переход окраски при охлаждении? А с какой стати? Растворы карбоната натрия и калия окрашивают фенолфталеин в малиновый цвет и при комнатной температуре (гидролиз этих солей все равно идет в достаточной степени). Разве что в воде карбонатов будет очень мало и, в результате постепенного поглощения водой углекислого газа из воздуха, карбонат перейдет в гидрокарбонат, и окраска фенолфталеина постепенно исчезнет. В нашем случае при охлаждении и стоянии воды на воздухе окраска индикатора не исчезла, а только ослабла. Оставил стакан с водой (в открытом виде), чтобы наблюдать, что будет дальше - в надежде, что окраска фенолфталеина со временем все-таки исчезнет. Результат: через 48 часов окраска сильно ослабла (расвтор розовый), 60 часов - раствор уже бледно-розовый, 76 часов - раствор почти обесцветился, но еще заметен легкий розовый оттенок. |

Слева - дистиллят, справа - водопроводная вода |

Добавляем фенолфталеин - малиновая окраска не появляется ни в одном стакане |

|

Ставим стаканы греться на плитку |

|

|
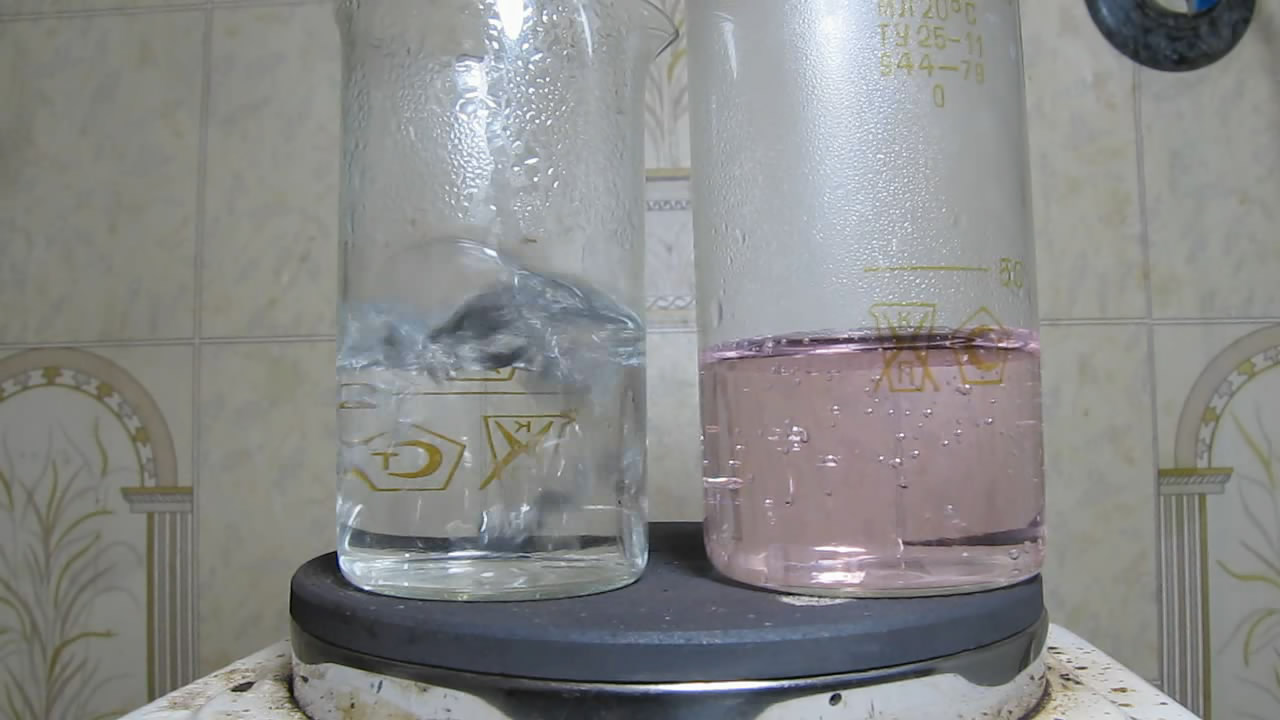
|
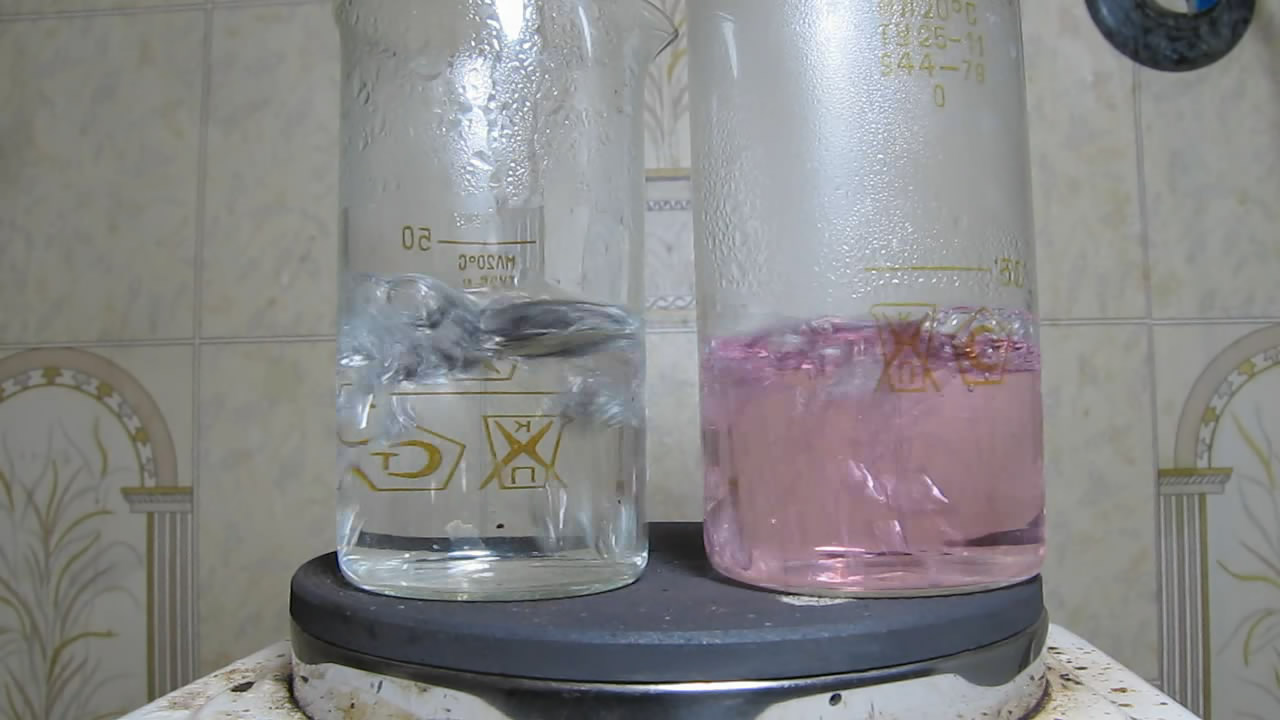
|

|

|

|

Снимаем стаканы с плитки |

Через сутки (открытые стаканы на воздухе) |

Прошло 60 часов |

Прошло 76 часов |
Разложение гидрокарбоната натрия Decomposition of sodium bicarbonate В.Н. Витер |
|