Химия и Химики № 5 2020
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 5 2020 Журнал Химиков-Энтузиастов |
Неправильный амин (забавное титрование) Wrong amine (funny titration) Химик |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Суть задачи: синтезировать амиды исходя из амина и технической смеси жирных кислот или вообще - из растительного масла (природная смесь триглицеридов жирных кислот). Амины? Разные. Например, диэтаноламин - вещество, формула которого напоминает птицу:
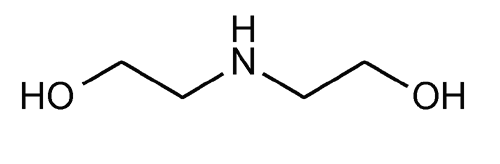
Диэтаноламин / Diethanolamine Орнитологи знают еще такое пернатое: 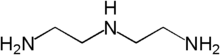
Диэтилентриамин / Diethylenetriamine or DETA …но оно прилетело из другой оперы. Чаще всего был диэтаноламин. Техника эксперимента простая: в колбу помещаются исходники (исходные вещества) и якорь магнитной мешалки. Колба ставится на мешалку с плиткой и накрывается: елочным дефлегматором, обратным холодильником, обратным холодильником с насадкой Дина-Старка… (ненужное вычеркнуть). Еще добавляется катализатор. Или не добавляется (в надежде на старую-добрую азеотропную отгонку воды с толуолом или не с толуолом). Независимо от всего этого разнообразия в конце синтеза необходимо проконтролировать полноту протекания реакции. Критерием служит концентрация остаточного амина (исходное вещество). Как его проанализировать? Берут навеску реакционной смеси, добавляют спирт до растворения, разбавляют водой - получается эмульсия. Ее и титруют соляной кислотой. Остаточный амин титруется, продукт реакции (амид) - нет. Титрование ведут с рН-метром на магнитной мешалке (потенциометрическое титрование). Потом нужно построить кривую в координатах: рН - объем соляной кислоты (точнее там была немного нетипичная величина: количество ммоль солянки в пересчете на 1 кг навески). Именно по кривой титрования рассчитывают концентрацию остаточного амина. Но, зная навеску реакционной смеси и результаты прошлых титрований, уже в процессе титрования можно сказать, прореагировали ли вещества в достаточной мере (т.е., еще ДО построения графика). Титрую солянкой очередной образец - соляной кислоты идет слишком много: уже по ходу титрования видно, что амин почти не прореагировал. В чем дело? Смеси с таким амином я еще не титровал. Показываю коллеге: он говорит, что с данным веществом - все по-другому: один азот реагирует, второй - частично. Коллега ушел. Титрую дальше. Появились проблемы: рН-метр погрузился ниже места, где прикручивается электрод. Почему? Большой объем титранта. Закрепил выше, титрую дальше. Смотрю, а носик бюретки тонет в растворе. Бюретка автоматическая - т.е. закреплена она не в штативе, а на бутылке. Была бы бюретка в штативе, приподнять ее - секундное дело, но эту просто так не поднимешь. Стакан тоже не опустишь - он на мешалке. Чтобы приподнять бюретку, пришлось подставлять под бутылку стопку бумаги (книги для этой цели пожалел - их могло залить солянкой). Титрую дальше - очередная проблема: хватит ли места в стакане? Слишком много идет титранта. Не придется ли переливать раствор в другой стакан прямо по ходу титрования (можно, но это - извращение). Поднял рН-метр до максимума. Места хватило впритык. Верхнее деление стакана - 150 мл, на титрование пошло почти 75 мл раствора, а первоначальный объем пробы, разведенной водой и спиртом, был 100+ мл. Я, еще не дотитровал, но уже стал думать: где ошибка. В N,N-диметилпропиламине азот только один. Читаю надпись на бутылочке - все правильно. Попросил прочесть соседа - правильно. 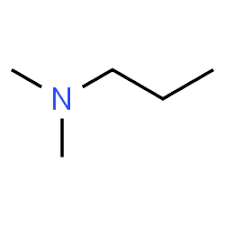
Диметилпропиламин / Dimethylpropylamine Ищу в интернете про амиды кислот, полученные из третичных аминов и тут понимаю, что третичные амины НЕ образуют амидов. Значит, вещество - другое. Кроме третичного азота должен быть хотя бы один первичный или вторичный. Иначе нечему образовывать с кислотами амиды. Не зная органики, прикинул варианты. Скорее всего - N,N-диметилАминопропиламин - на этикетке пропущена приставка "амино-" 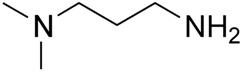
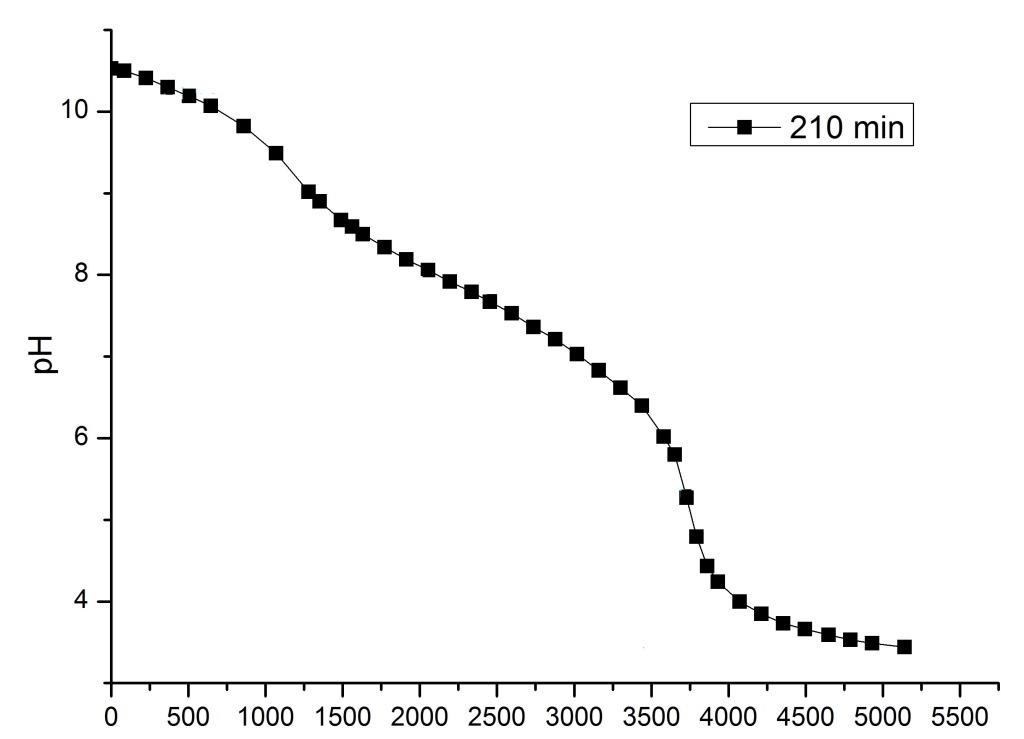
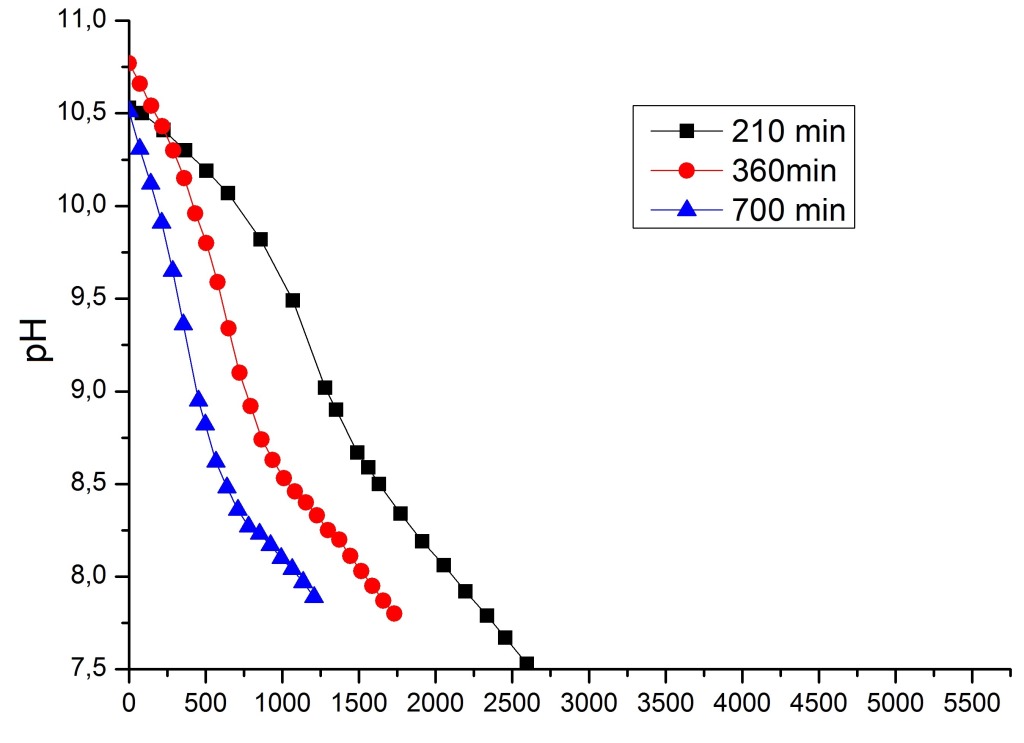
Диметиламинопропиламин / Dimethylpropylamine Пришел коллега - спросил. Так и оказалось. Оказалось, также, что титровать "до упора" (конечное рН у меня около 3.5) было не обязательно, т.к. для расчетов нужен был скачек титрования, который происходит до рН=8. Что за переход такой при рН>8: во время титрования чего-либо сильной кислотой - долго не мог понять. И сам не знаю, и никто из знакомых на этот вопрос не ответил. Если титровать слабое или среднее основание сильной кислотой (в данном случае - соляной кислотой), точка эквивалентности будет при рН<7, если титровать сильное основания сильной кислотой - то при рН=7. Чтобы при титровании сильной кислотой сместить точку эквивалентности в область рН>7, нужно "супер-основание", но в водных растворах таковые не живут. Возможно, это ошибка в технологическом регламенте? Но в таком случае ее давно бы заметили (полезное правило: "не стоит принимать за аксиому, что ты - самый умный"). На следующий день вопрос разрешился. Коллега вспомнил - все оказалось банально. Кислота, которой титровали основание - одноосновная, а само основание - двухкислотное (1 молекула амина реагирует с 2-мя протонами). Именно поэтому первый скачек рН на кривой титрования находится в щелочной области, хотя кислота сильная, а основание - так себе. |

|

|

|

|

|

|

|

|

|

|

|

|

|
|
|