Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
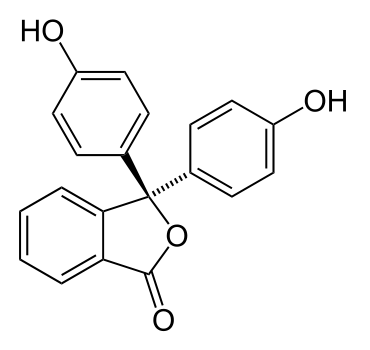
Фенолфталеин (4,4'-диоксифталофенон) - бесцветные кристаллы, без запаха и вкуса, плохо растворимые в воде, но растворимые в спирте. Фенолфталеин - один из самых известных кислотно-основных индикаторов, до недавнего времени фенолфталеин широко применялся в медицине как слабительное средство (пурген).
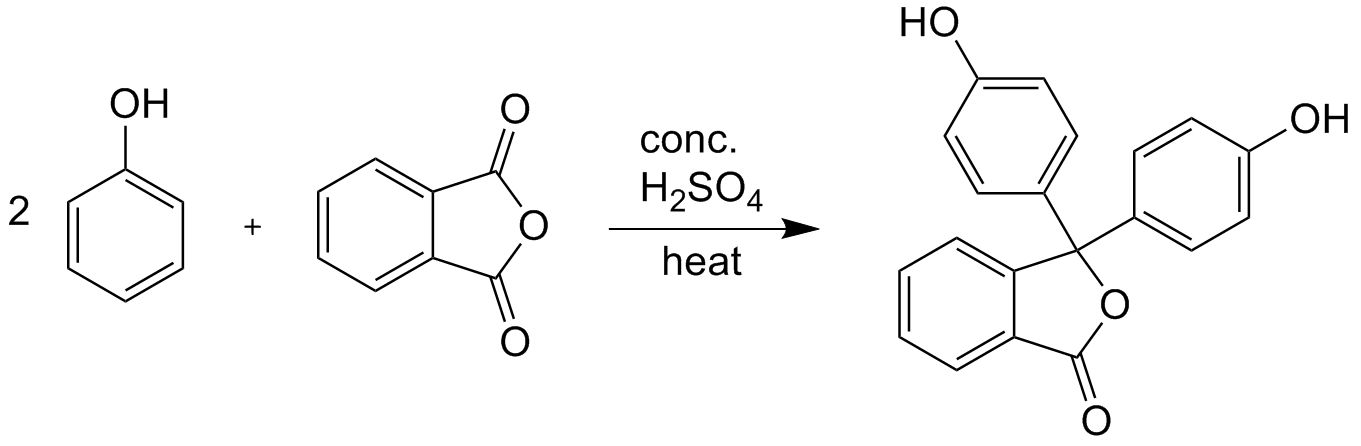
Получают фенолфталеин реакцией конденсации фенола и фталевого ангидрида в присутствии концентрированной серной кислоты (или хлорида цинка) при нагревании.
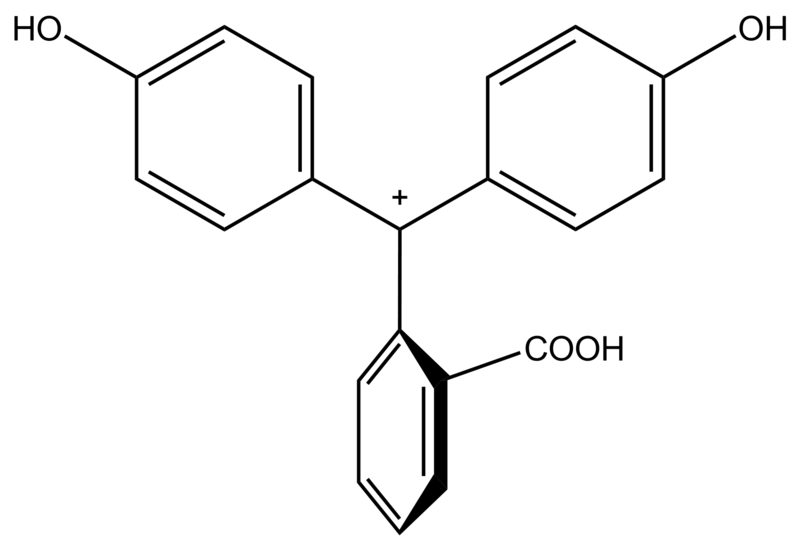
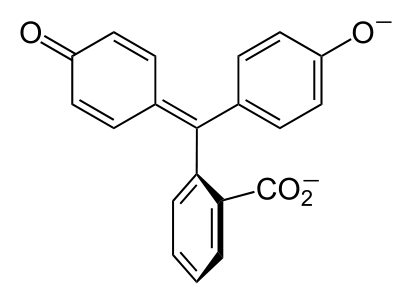
Про окраску фенолфталеина обычно пишут следующее: в кислой среде бесцветен, в щелочной - малиновый [при pH<8.2 - бесцветен, при pH>8.2 - малиновый (красно-фиолетовый)]. На самом деле поведение этого индикатора намного интереснее.
Возьмем четыре стакана:
1) В первый нальем разбавленную серную кислоту
2) Во второй - разбавленную щелочь
3) В третий нальем концентрированную серную кислоту
4) В четвертый - концентрированный раствор щелочи с осадком (едкий натр или едкое кали)
Во все стаканы добавим по несколько капель спиртового раствора фенолфталеина.
В первом стакане раствор останется бесцветным, во втором, как и ожидалось, раствор окрасится в малиновый цвет.
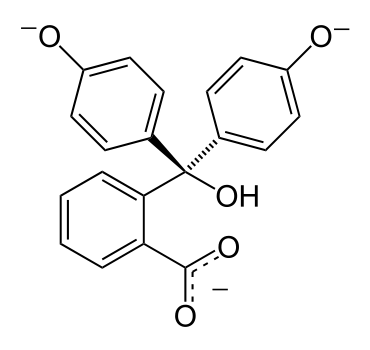
Теперь внимание: в третьем стакане - с концентрированной серной кислотой - фенолфталеин стал оранжевым. В четвертом стакане - с концентрированным раствором щелочи - сначала появилась малиновая окраска, но при перемешивании она исчезла: раствор снова стал бесцветным.
Получают фенолфталеин реакцией конденсации фенола и фталевого ангидрида в присутствии концентрированной серной кислоты (или хлорида цинка) при нагревании.

Про окраску фенолфталеина обычно пишут следующее: в кислой среде бесцветен, в щелочной - малиновый [при pH<8.2 - бесцветен, при pH>8.2 - малиновый (красно-фиолетовый)]. На самом деле поведение этого индикатора намного интереснее.
Возьмем четыре стакана:
1) В первый нальем разбавленную серную кислоту
2) Во второй - разбавленную щелочь
3) В третий нальем концентрированную серную кислоту
4) В четвертый - концентрированный раствор щелочи с осадком (едкий натр или едкое кали)
Во все стаканы добавим по несколько капель спиртового раствора фенолфталеина.
В первом стакане раствор останется бесцветным, во втором, как и ожидалось, раствор окрасится в малиновый цвет.
Теперь внимание: в третьем стакане - с концентрированной серной кислотой - фенолфталеин стал оранжевым. В четвертом стакане - с концентрированным раствором щелочи - сначала появилась малиновая окраска, но при перемешивании она исчезла: раствор снова стал бесцветным.