
Реакция меди и концентрированной азотной кислоты










| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 8 2013 Журнал Химиков-Энтузиастов |
Эксперименты с магнием ч.4 Experiments with Magnesium В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Горение магния в диоксиде азота. Burning Magnesium in Nitrogen Dioxide
Горение магния в диоксиде азота уже было описано в нашем журнале [1]. Эксперимент пришлось повторить по той же причине, что и другие опыты с магнием: низкое качество снятого видео.
__________________________________________________ 1 См. статью Горение в диоксиде азота, раздел Горение магния в диоксиде азота [ссылка].
Реакция меди и концентрированной азотной кислоты.
Опыт по горению магния решил провести в трехлитровой банке. Поскольку наличие паров воды и азотной кислоты не мешает эксперименту, диоксид азота получил в этом же сосуде. Для этого на дно банки налил 30 мл концентрированной азотной кислоты (60%), бросил туда штук 5 монет из алюминиевой бронзы (украинская монета 10 коп.) и накрыл банку чашкой Петри. Началась бурная реакция. Раствор стал зеленым в результате выделения оксидов азота, пространство банки начал заполнять бурый диоксид азота. Через несколько минут вся банка была заполнена бурыми парами, потом диоксид азота стал выходить сквозь неплотности между банкой и чашкой Петри.
The Reaction of Copper and Concentrated Nitric Acid Сам эксперимент был очень простым, но съемка его неожиданно вызвала трудности. Когда банка заполнилась темным диоксидом азота, картинка на видео стала слишком светлой и нечеткой. Пришлось поэкспериментировать с освещением. Оптимальным оказался вариант, когда свет под вытяжкой был выключен, а в комнате горело слабое освещение. |

Реакция меди и концентрированной азотной кислоты |

|

|

|

|

|

|

|

|

|

|
|
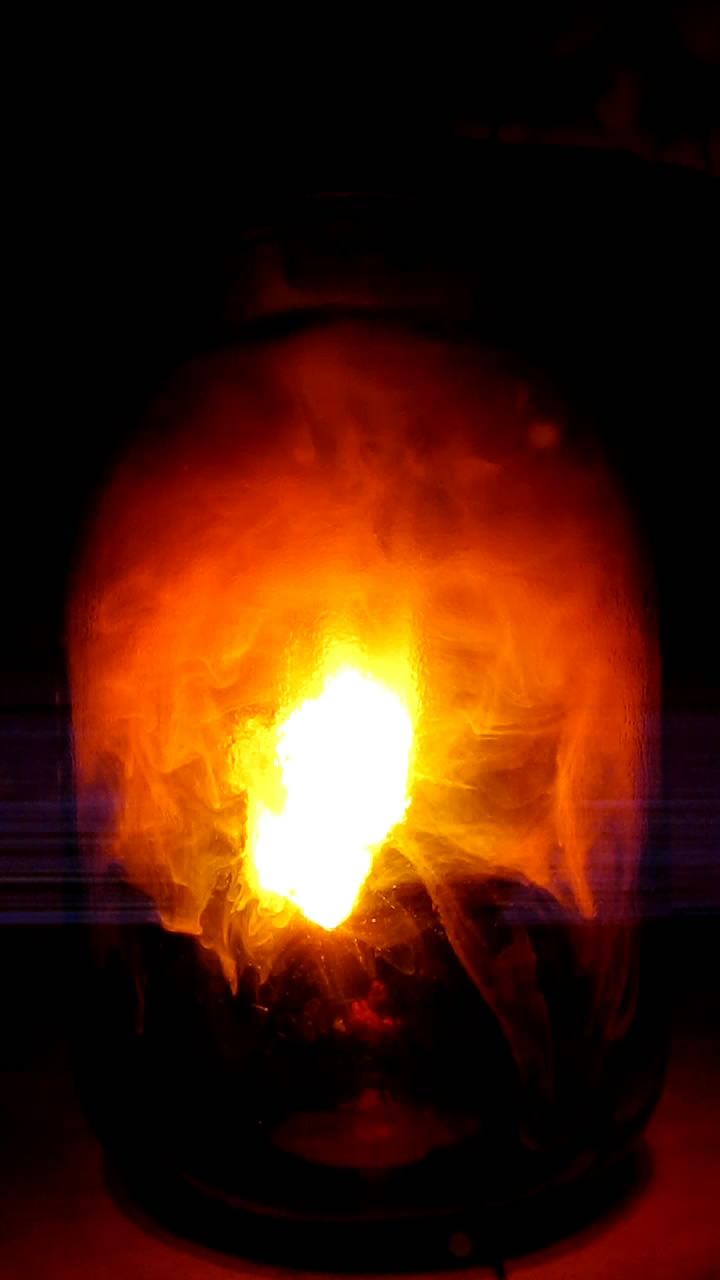
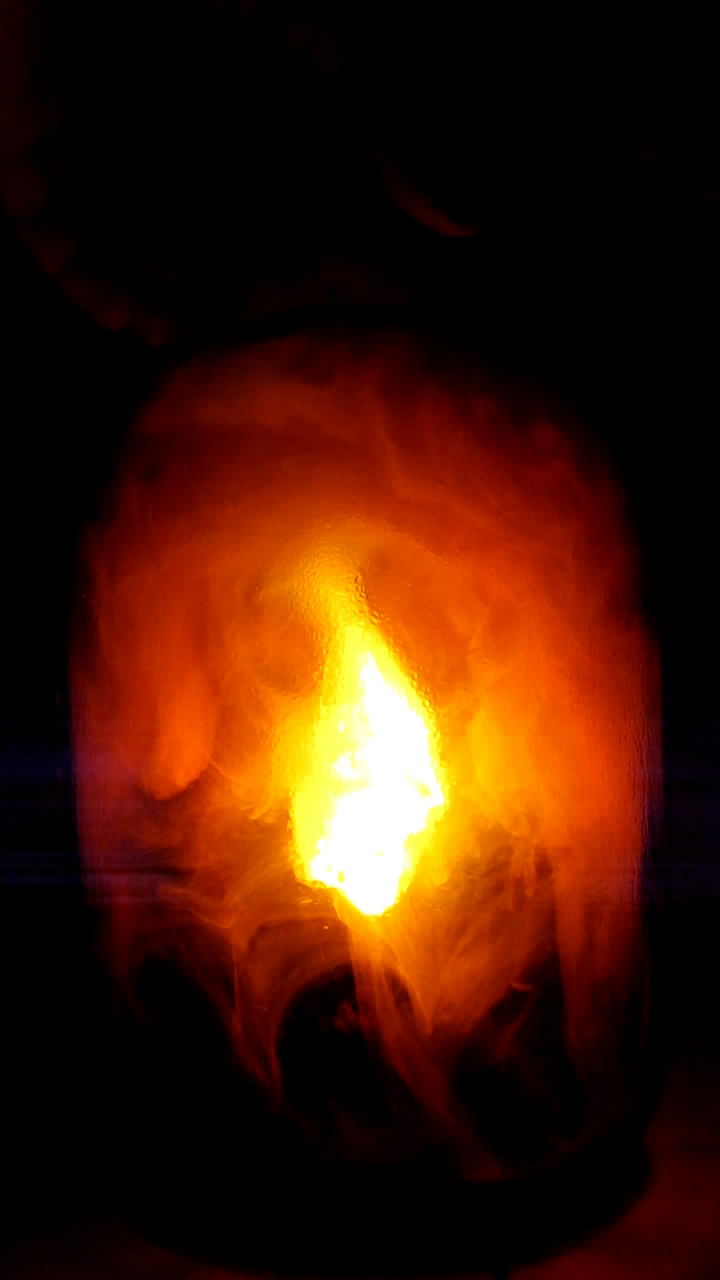
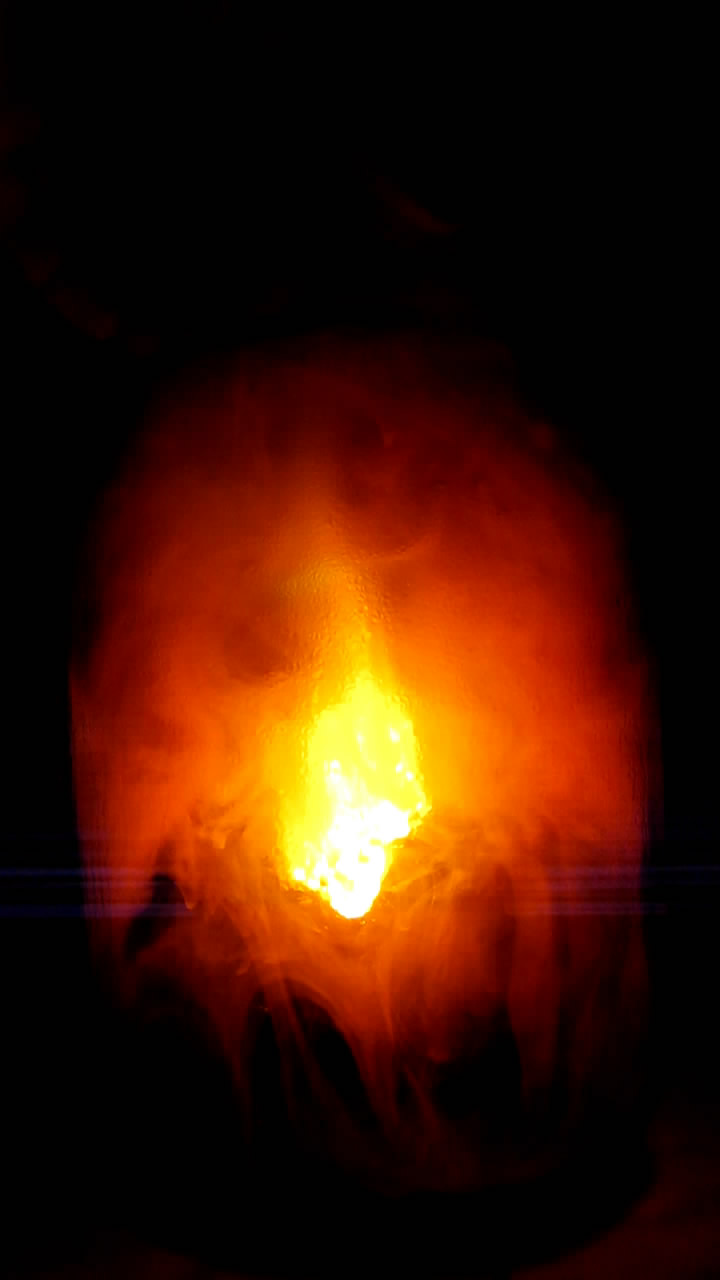
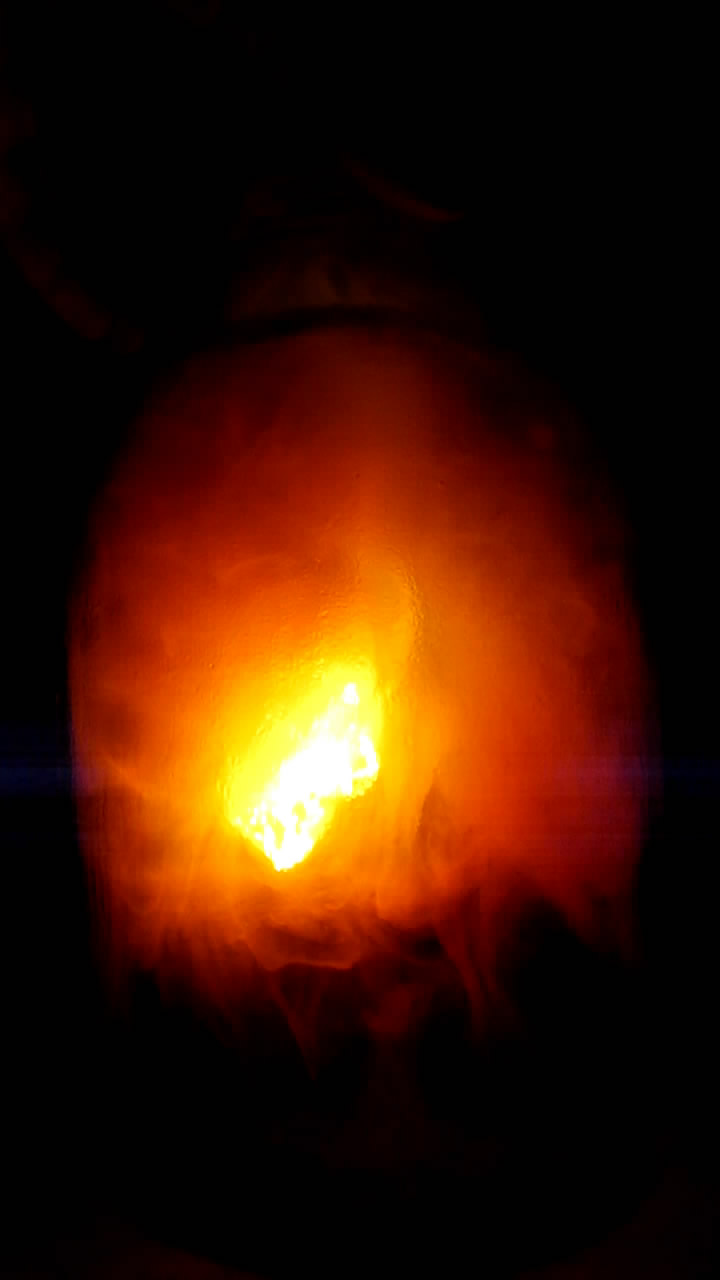
Горение магния в диоксиде азота
Кусочек магния (сплав электрон) нагрел в ложечке из сетки из нержавеющей стали. Магний расплавился в пламени горелки, а затем загорелся. Горящий магний внес в банку с диоксидом азота и сразу же накрыл ее чашкой Петри. Магний продолжил ярко гореть, выделяя белый дым, но сквозь слой бурого диоксида азота проходило мало света - стало очевидным, что этот газ сильно поглощает лучи [2]. Банка излучала нереалистичный желто-бурый свет. Пространство внутри стало заполняться белым дымом оксида магния, который поглощал свет еще больше.
По мере горения магния газ в банке стал светлеть и терять бурый оттенок. Чашка Петри, которой была накрыта банка, не выдержала тепла и разлетелась на кусочки. Газ в банке сильно посветлел, магний начал гаснуть. Но что интересно: постепенное угасание горения магния происходило несколько минут и было очень плавным. Все это время содержимое ложечки оставалось раскаленным. Раньше я такого в опытах с магнием не наблюдал. Сквозь желтоватый газ банки продут горения магния казался желтым, но когда я вынул ложечку, стало очевидно, что это белый оксид магния. Судя по характерным искрам и заметному разрушению материала ложечки, вместе с магнием частично горела и сталь сетки. __________________________________________________ 2 Некоторые художники-фантасты любят рисовать пейзажи планет, атмосфера которых состоит из сильно окрашенных газов, например, из хлора. Можно с уверенностью сказать, как выглядела бы поверхность подобных планет: "тьма египетская" (если только атмосферное давление на этой планете не будет существенно меньше земного). Вспомним, например, Венеру. Солнечный свет достигает поверхности этой планеты, но с поверхности Венеры не видно, ни Солнца, ни звезд. Во время восхода Солнца небо на Венере постепенно и равномерно светлеет, заката - темнеет. Углекислый газ - основной компонент атмосферы Венеры - хорошо пропускает солнечный свет, но там есть еще облака, которые состоят из мелких капелек серной кислоты. Благодаря этому поверхность второй от Солнца планеты надежно скрыта от земных телескопов. Раньше считалось, что Венера имеет плотную облачность, которая пропускает к поверхности только рассеянный и сильно ослабленный свет Солнца. Позже оказалось, что облака на Венере соответствуют легкой облачной дымке на Земле, просто их слой слишком толстый и всегда сплошной. |

Горение магния в диоксиде азота Burning Magnesium in Nitrogen Dioxide |

|

|

|

|

|

|

|

|

|

|

|
|

|

|
|

|
|
|

|

|

|

|

|

|

|

|

|

|
|

|

|

|

|

|

|

|

|

|
Горение в диоксиде азота Burning in nitrogen dioxide В.Н. Витер |
|
Старый вариант - №6 2009
Оксиды азота является сильными окислителями, которые активно поддерживают горение. Например, в среде газообразного диоксида азота NO2 горит много неорганических и органических веществ: сера, фосфор, уголь, водород, некоторые металлы, древесина, бумага, углеводороды, спирты и др. Ниже описаны эксперименты по сжиганию органических и неорганических материалов в среде диоксида азота.
Для получения диоксида азота NO2 мы использовали реакцию меди [3] с концентрированной азотной кислотой HNO3. Во многих случаях с целью упрощения эксперимента диоксид азота получали в том же сосуде, в котором потом проводилось сжигание. Необходимо было подождать определенное время, чтобы осели брызги и туман кислоты. Примесь водяных паров, как правило, не мешала.
Горение серы в диоксиде азота / Burning Sulfur in Nitrogen Dioxide
Несколько кусочков серы поместите в металлическую ложечку и нагрейте в пламени горелки до воспламенения. Сера загорится бледно-синим пламенем. Весите горящую серу в литровый сосуд с диоксидом азота. Сера продолжит гореть очень бледным желтоватым пламенем. В результате реакции образуется серный ангидрид, который дает с влагой густой туман H2SO4. Поэтому весь сосуд скоро заполнится белым дымом. 2S + 3NO2 = 2SO3 + 1.5N2
Если вынуть ложечку с горящей серой из сосуда, на воздухе пламя серы снова станет синим.
SO3 + H2O = H2SO4 __________________________________________________ 3 Вместо меди можно взять украинские монеты из медного сплава |

Горение серы в диоксиде азота Burning sulfur in nitrogen dioxide |

|

|

Горение магния в диоксиде азота Burning Magnesium in Nitrogen Dioxide |

|
 |

Горение в диоксиде азота деревянной лучинки Burning Wood in Nitrogen Dioxide |

|

|

Горение скипидара в диоксиде азота Burning Turpentine in Nitrogen Dioxide |

|

Горение пропан-бутановой смеси в диоксиде азота Burning Propane and Butane in Nitrogen Dioxide |

|

Горение свечи в диоксиде азота Burning Candle in Nitrogen Dioxide |

|

Самовоспламенение и горение несимметричного диметилгидразина (CH3)2N-NH2 в диоксиде азота |

|

|

Горение анилина в диоксиде азота NO2 |

|

|

|

фото chem.leeds.ac.uk |