Реакция калия с водой
Реакция калия с водой протекает бурно. Маленькие кусочки калия загораются красно-фиолетовым пламенем, бегая с шипением по поверхности воды. Средние и большие кусочки взрываются, разбрасывая во все стороны брызги расплавленного горящего калия.
Мне приходилось видеть эту реакцию лишь один раз. Как-то мы с Сашей обнаружили в сейфе большую (литра на два) банку с каким-то щелочным металлом в масле. Мы были уверены, что это натрий. Отрезали небольшой кусочек и бросили его в кристаллизатор с водой. Кусочек металла стал с шипением бегать по поверхности воды. К нашему удивлению появилось не желтое (как в случае натрия), а фиолетовое пламя. Это оказался калий.
Тогда банку с калием можно было беспрепятственно забрать, но не понесешь же ее домой - внутри больше килограмма пожароопасного металла. Теперь, к сожалению, калия в нашем распоряжении нет, но в сети удалось найти немного фотографий и видео реакции калия с водой.
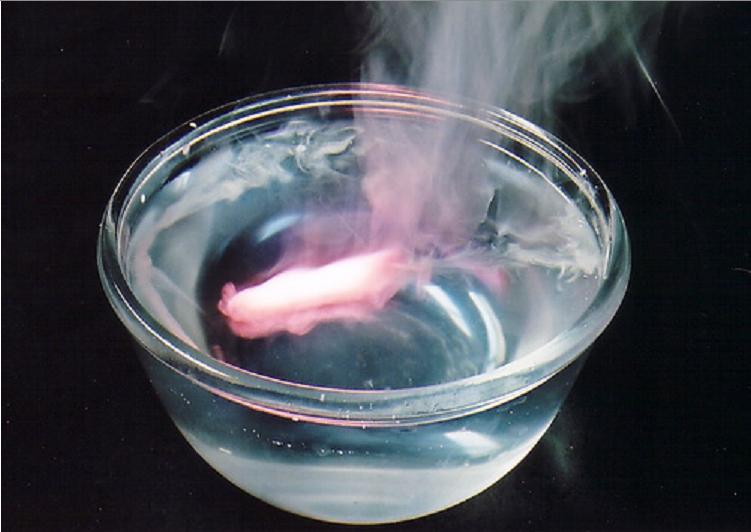

Видео реакции калия с водой
http://chemistry-chemists.com/Video-to- ... -water.mp4
авторы
hydrogen01 сайт home-and-garden.webshots.com
Cyberchemist сайт flickr.com

