
На дне цилиндра - насыщенный раствор сульфата меди и кристаллы, сверху была аккуратно налита дистиллированная вода: так, чтобы не произошло смешивание [K1].
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 1 2015 Журнал Химиков-Энтузиастов |
Диффузия и концентрационный гальванический элемент В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Недавно провел эксперименты с концентрационным гальваническим элементом [1], причем растворы с более высокой и более низкой концентрацией сульфата меди находились в одном сосуде - не разделенные никакой перегородкой. Градиент концентраций существовал только благодаря тому, что диффузия катионов меди со дна цилиндра вверх происходила далеко не моментально. В противном случае концентрация бы выровнялась и напряжение упало бы до нуля. В конце концов, так и произойдет, но насколько быстро?
__________________________________________________ 1 Гальванический элемент. Концентрационный гальванический элемент ч.7. [ссылка] |

На дне цилиндра - насыщенный раствор сульфата меди и кристаллы, сверху была аккуратно налита дистиллированная вода: так, чтобы не произошло смешивание [K1]. |
|
После окончания экспериментов настоятельно рекомендуется все разобрать, помыть и разложить по своим местам - независимо от того, получился эксперимент или нет. В противном случае через несколько недель на лабораторном столе и вокруг него образуются массивные залежи посуды, реактивов, инструментов, вспомогательных материалов и т.д. В результате найти что-либо в этих залежах будет крайне трудно (если вообще возможно) - разве что вы обратитесь за помощью к археологам.
Гальванический элемент получился, фото и видео были отсняты, но я решил его не разбирать его, а оставить на несколько дней - чтобы посмотреть, как изменится напряжение гальванического элемента со временем. Разница потенциалов между верхним и нижним медными электродами возникла за счет того, что нижний электрод соприкасался с насыщенным раствором сульфата меди, верхний электрод - с дистиллированной водой. Как было сказано выше, насыщенный раствор сульфата меди и дистиллированная вода не были разделены мембраной или солевым мостиком. Как долго они будут сосуществовать в одном сосуде? - Другими словами, насколько быстро пройдет диффузия ионов меди снизу цилиндра вверх? На следующий день содержимое цилиндра выглядит так же, как и днем ранее (т.е. в момент опыта). Интенсивно-синий раствор сульфата меди на дне цилиндра и бесцветная жидкость сверху. Причем между "синей" и "бесцветной" зонами нет четкой границы: при движении вверх по цилиндру синий цвет на определенном промежутке слабеет, затем - исчезает. Подключил тестер и померил напряжение - оказалось 22-25 мВ, ток - 16 мкА: все практически, как и вчера. |

Диффузия сульфата меди: прошел 1 день |

|

|
|
Еще через день (т.е. на второй день после сборки гальванического элемента) раствор в цилиндре выглядел так же.
|

Прошло 2 дня |
|
Седьмой день - аналогично, хотя заметно прохождение диффузии.
|

Прошло 7 дней |

|
|
Десятый день - окрашенная зона продвинулась на несколько сантиметров вверх и стала более бледной.
|

Прошло 10 дней |

|
|
Четырнадцатый день - окрашенная зона поднимается вверх, бледнеет, ее граница все более размывается. Стало заметно, что вода из цилиндра испаряется - ее уровень падает.
|

Прошло 14 дней |

|
|
Девятнадцатый день - процесс идет. Подключил электроды тестера: напряжение концентрационного гальванического элемента все то же - 24 мВ: при этом верхняя и нижняя часть сосуда разделены только водой!
|

Прошло 19 дней |

|

|
|
Замкнул электроды гальванического элемента накоротко. Напряжение померил только через 2 дня - на 21 день. Напряжение упало до 9 мВ. Цепь снова разомкнул.
|

Прошел 21 день |

|
|
Двадцать шестой день. Померил напряжение - 10 мВ, синий раствор заметно поднялся, уровень воды в цилиндре упал на несколько сантиметров (результат испарения). Градиент концентрации в цилиндре все еще сохраняется.
|

Прошло 26 дней |
|
Опыт прекратил, т.к. прошел уже почти месяц. Добавлю, что цилиндр с водой и раствором сульфата меди не находился в абсолютном покое: в лаборатории иногда проводились столярные работы, цилиндр один раз аккуратно переставили, плюс при подключении тестера к медным электродам последние иногда сдвигались. Разумеется, даже такое слабое перемешивание способствовало выравниванию концентраций.
Даже такой примитивный эксперимент, проведенный без количественных измерений, наглядно показывает, что диффузия в водных растворах происходит достаточно медленно - если нет перемешивания жидкости. (Например, механического перемешивания мешалкой или перемешивания в результате конвекции). Именно поэтому диффузия может существенно замедлить протекание химической реакции или передачу тепла через жидкость. Довольно наглядное представление о том, что процесс диффузии протекает далеко не мгновенно, дают кристаллики перманганата калия. Достаточно аккуратно добавить несколько кристаллов в пробирку с водой, чтобы убедиться, что они опустятся на дно и окрасят нижний слой воды, который может стоять сутками, не перемешиваясь с верхним бесцветным или слегка окрашенным слоем (только вода и поверхность стекла не должна содержать органики - иначе перманганат с ней прореагирует). |

Растворение перманганата калия |
|
Приведу несколько других примеров.
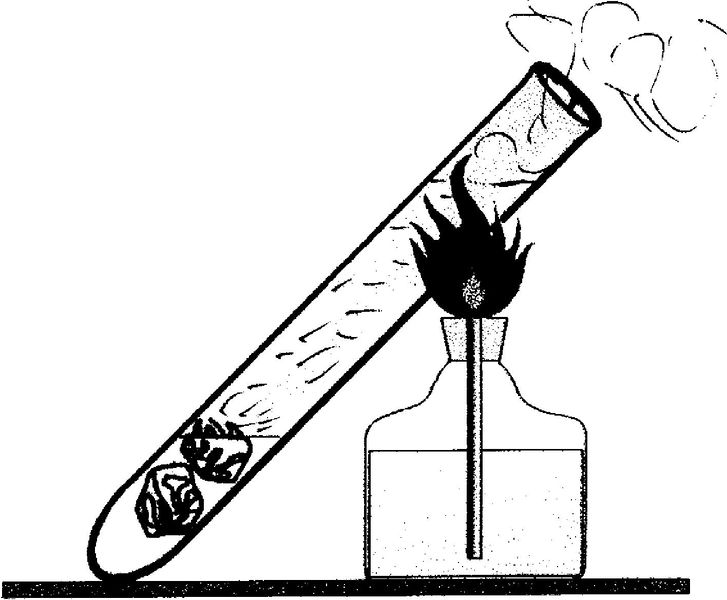
Если на дно пробирки поместить лед (так, чтобы он не всплыл), а сверху налить воду, то можно внести верхнюю часть пробирки в пламя и добиться того, что вода сверху закипит - зато лед на дне останется. Холодная вода снизу тяжелее горячей воды сверху: конвекция отсутствует, а теплопроводность воды не такая и высокая. |
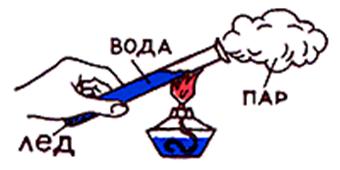
Опыт, который демонстрирует низкую теплопроводность воды |
|
|
Если сделать наоборот: поместить лед сверху, а греть пробирку снизу, то внутри пробирки будет происходить конвекция. Теплая вода будет подниматься со дна пробирки вверх, на ее место будет опускаться холодная вода (охлажденная льдом), которая нагреется возле дна и поднимется вверх, тем временем вниз опустится новая порция холодной воды. В результате лед быстро растает - и только тогда вода во всей пробирке нагреется и закипит.
Другой важный пример. Когда реки впадают в море, соленная и пресная вода смешиваются далеко не моментально. Нередко пресная вода движется сверху, соленная - остается снизу. Самая большая река Планеты - Амазонка, впадая в Атлантический океан, оттесняет соленую воду более чем на 100 км, образуют знаменитое "Пресное море", которое в 1500 г. открыл испанский мореплаватель Висенте Яньес Пинсон. С другой стороны, тяжелая соленая вода может проникать в дельты рек - образуя нижний слой. Это имеет большое значение не только для речных экосистем, но и непосредственно для деятельности человека. Например, во время битвы за Атлантику Гитлер направил свои подводные лодки к побережью США и Канады, поскольку атаки подводных лодок возле берегов Европы стали слишком рискованными - транспорты союзников прикрывали эсминцы и авиация. В частности, немецкие субмарины начали топить корабли в низовьях реки Святого Лаврентия и на некоторое время полностью парализовали в этой реке судоходство. Канадцы оказались плохо подготовленными к такой атаке. На первый взгляд, положение субмарин казалось невыгодным: ведь река - не море: тут значительно меньше пространства, чтобы затеряться (зато много вражеских кораблей и авиации). Однако в устье реки сверху была пресная вода, снизу - соленная (морская), причем граница раздела этих слоев отражала сигналы сонара: лодка могла избежать обнаружения, опустившись ниже границы разделения пресной и соленой воды. В некоторых случаях удается одновременно обнаружить несколько слоев воды с разной соленостью, причем наблюдение границы раздела может облегчиться тем обстоятельством, что в месте, где контактируют речная вода, богатая органическими веществами, и соленая морская вода происходит коагуляция органики с образованием взвеси (мути). Напомню, что растворенные в морской воде соли являются электролитами, а электролиты способны коагулировать коллоидные растворы. Но даже если поблизости нет рек, в океане нередко возникают слои воды, граница между которыми отражает сигналы сонара. Нередко эти слои воды отличаются не соленостью, а температурой воды. В Черном море сверху вода более пресная - в результате того, что в него впадает несколько крупных рек, в частности - Днепр, Дунай и Днестр. В глубинные слои Черного моря поступает более соленая (а значит - и более плотная) вода из Мраморного моря. Менее соленная и более теплая вода верхних слоев практически не смешивается с более соленой и холодной водой глубинных слоев. - Как следствие, в нижние слои Черного моря почти не поступает кислород. - Там преобладают анаэробные процессы гниения, в результате которых выделяется сероводород. Жить в сероводородной зоне могут только некоторые бактерии, поэтому практически весь животный и растительный мир Черного моря сосредоточен в верхнем слое глубиной до 100 м, вода в котором имеет преимущественно "речное происхождение". Любопытно, что менее соленная вода верхних слоев покидает Черное море через пролив Босфор и течет в Мраморное море, а в обратном направлении, но уже по дну Босфорского пролива, течет более соленая вода: из Мраморного моря в Черное море (нижнебосфорское течение). Соленость воды в Черном море меняется с глубиной неравномерно: до глубины 50-100 метров она нарастает быстро (от 17 до 21 г/л), затем вплоть до дна происходит равномерное увеличение солености примерно до 30 г/л. Кстати, это очень напоминает наш цилиндр с сульфатом меди. |
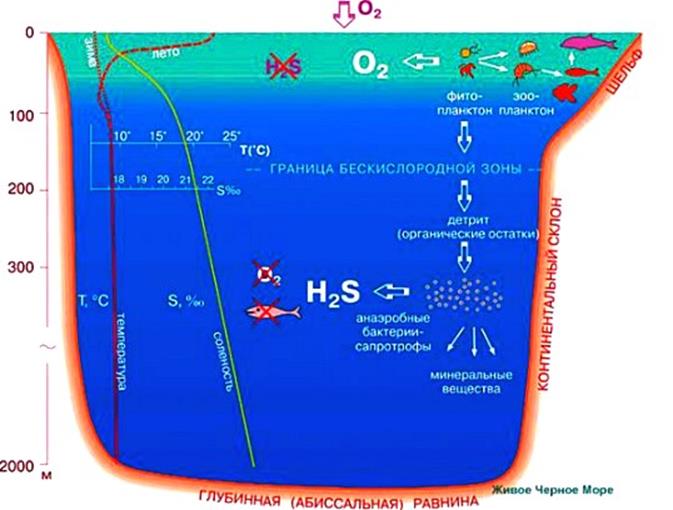
Черное море |
|
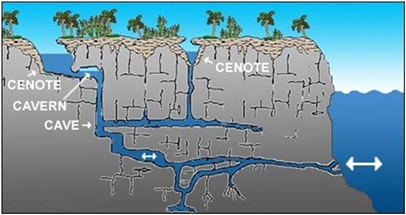
Слои пресной и соленой воды могут чередоваться не только в море или океане. Например, на полуострове Юкатан есть большая сеть пещер - сенотов (англ.- cenotes). Эти пещеры образовались, когда вода стала размывать кратер от падения крупного астероида (который погубил динозавров - согласно наиболее популярной теории). Большинство сенотов похожи на огромные колодцы, которые стоят среди джунглей. Сверху они наполняются пресной дождевой водой, а глубоко под землей связаны с океаном. Между пресной и морской водой часто возникает четкая граница раздела, которую не раз видели аквалангисты. Сеноты служили источниками пресной воды для цивилизации майя - и почитались индейцами как священные.
|

Сеноты |

|

|

|

|
|
|
Комментарии
К1
Возможно, в данном эксперименте вместо дистиллированной воды было бы лучше использовать раствор электролита, например, 0.1 М раствор серной кислоты. Дело в том, что в начале эксперимента сопротивление столба дистиллированной воды в цилиндре должно быть достаточно велико - скорее всего, порядка сотен кОм. Это вполне сопоставимо с сопротивлением стандартного тестера в режиме вольтметра (1-2 МОм). При подключении прибора разность потенциалов гальванического элемента будет делиться между прибором и элементом пропорционально их сопротивлениям. Таким образом, показания прибора окажутся занижены, причем в начале эксперимента больше, чем в конце, когда проводимость столба жидкости возрастет. Эффект от выравнивания концентрации будет смазан. Кстати, перемешивание раствора в цилиндре может происходить не только за счет перемещения частей установки, но и при изменениях температуры в помещении. В высоком вертикальном сосуде конвекция при изменении температуры может быть особенно заметной.
|