Химия и Химики № 1 2022
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 1 2022 Журнал Химиков-Энтузиастов |
Танины (эксперименты) - ч.1-4 Tannins (experiments) В.М. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Танины - вступление / Tannins - introduction
Танины (таннины, дубильные вещества) - природные полифенолы растительного происхождения, т.е. вещества, которые содержат много гидроксильных групп ОН, связанных непосредственно с бензольными кольцами. Строение разных танинов может значительно отличаться, как и их молекулярная масса. Объединяет их то, что танины можно легко выделить из разнообразных растений - в виде сложных природных смесей, которые часто используют без разделения. Кроме того, танины присутствуют во многих растительных продуктах, например, в соках, винах, чае, отварах и настойках лекарственных растений и т.д.Танины делятся на гидролизуемые - производные галловой кислоты (и родственных соединений), в которых гидроксильные группы этерифицированы многоатомными спиртами, например, сахарами и конденсированные танины - производные флавоноидов, образованные за счет конденсации полифенолов. Иногда выделяют также группу танинов, которая является производными флороглюцина. |
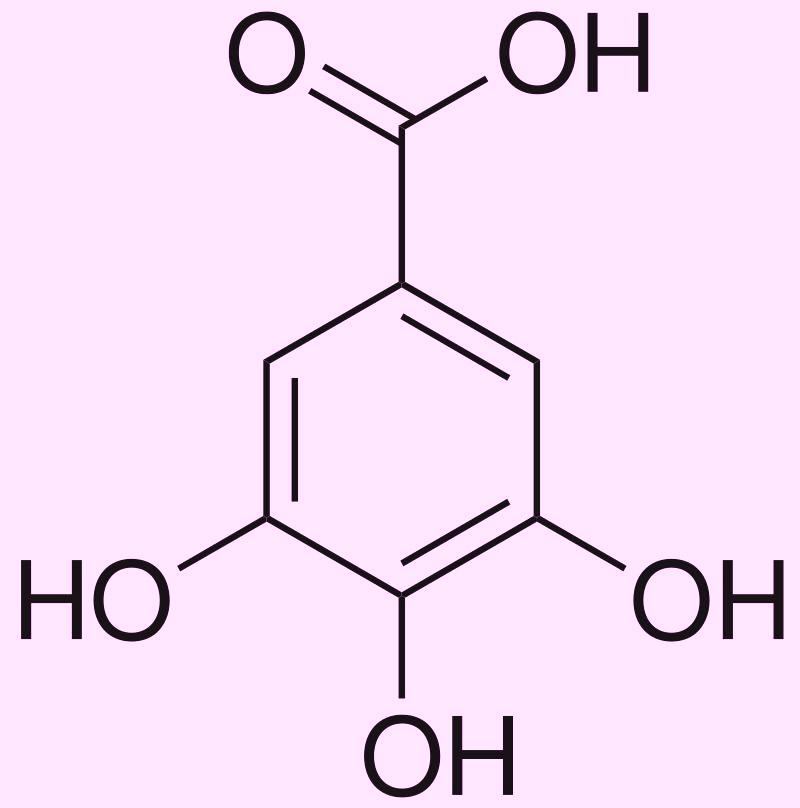
Галловая кислота - структурный элемент гидролизуемых танинов |
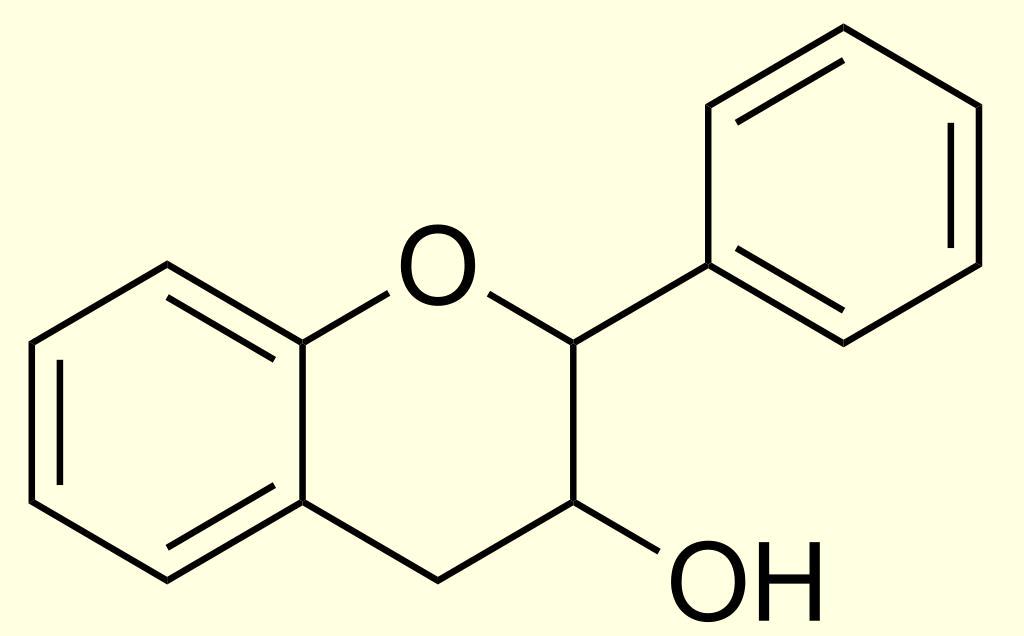
Флаван-3-ол - структурный элемент конденсированных танинов |
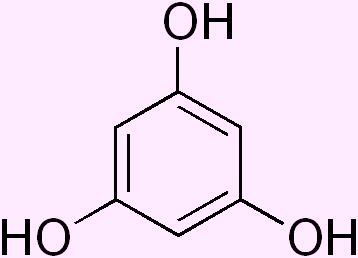
Флороглюцин |
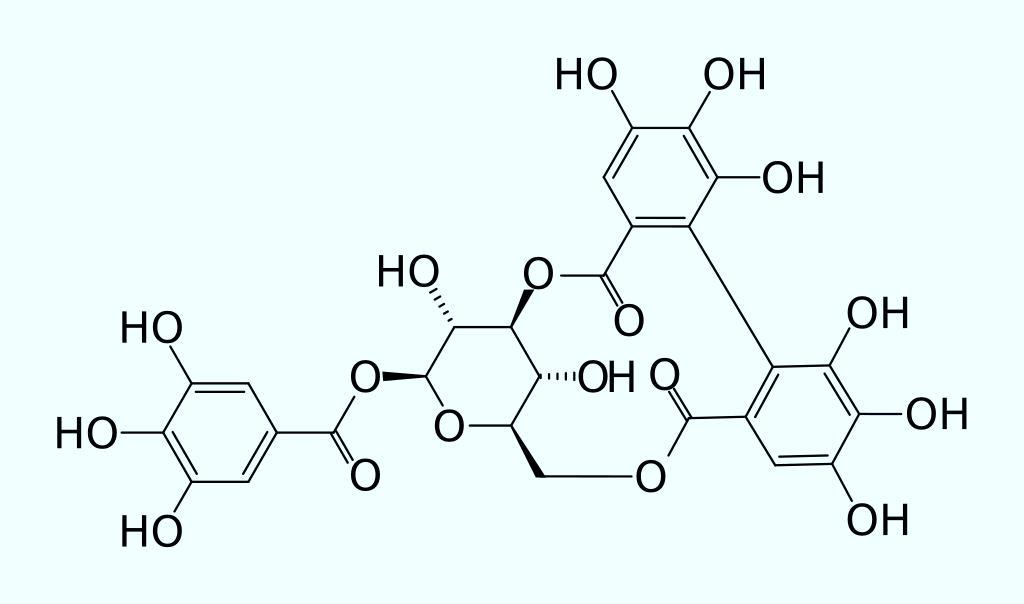
Корилагин (Corilagin) - пример танинов |
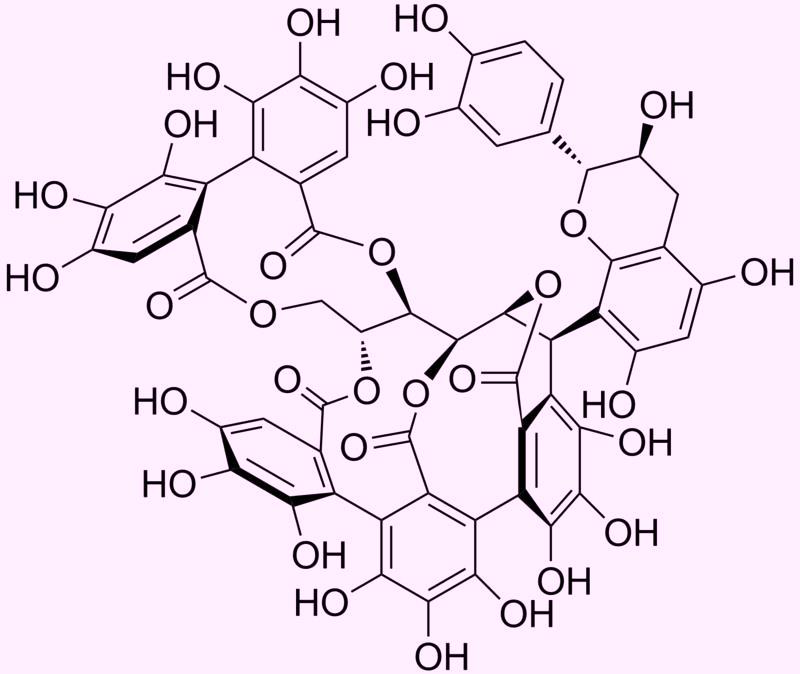
Акутиссимин А (Acutissimin A) - пример танинов |
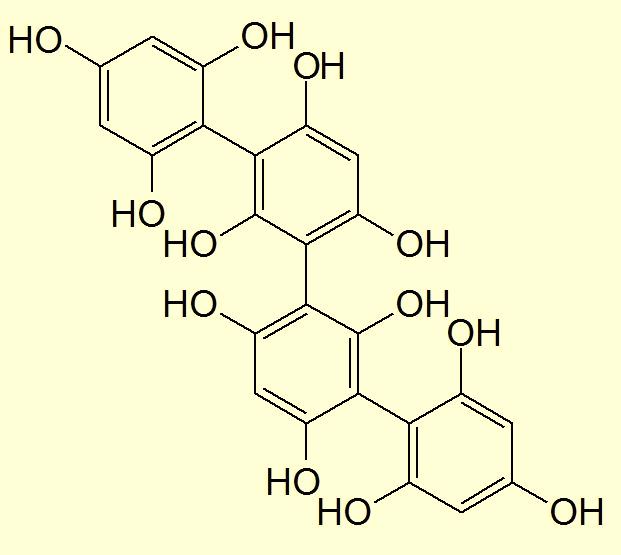
Tetrafucol A (Тетрафукол А) - пример танинов |
|
Известность и практическое значение танины получили благодаря способности связываться с биологическими полимерами: белками, полисахаридами, нуклеиновыми кислотами и др. Также танины могут связывать тяжелые металлы и некоторые биологические токсины (не только высокомолекулярные, но и с низкомолекулярные: например, алкалоиды).
С тяжелыми металлами танины образуют прочные комплексы, с биологическими полимерами и алкалоидами - нерастворимые осадки. Танины оказывают дубящее действие на шкуры животных, обладают антисептическими свойствами, а также - характерным вяжущим вкусом. Как и другие полифенолы, танины легко окисляются, поэтому они обладают антиокислительным (антиоксидантным) действием. Применяются в пищевой промышленности, кожевенной промышленности (дубление кож и меха), раньше использовались для крашения тканей и т.д. Благодаря способности связывать тяжелые металлы и биологические яды танины используются в медицине для детоксикации. Дополнительно танины применяются в медицине для лечения ожогов (вяжущие средства) и в качестве средств против диареи. Танины являются природной защитой растений от патогенных микроорганизмов, а также от поедания жвачными животными: благодаря танинам растения становятся для животных невкусными (хотя и остаются съедобными, просто травоядные употребляют растения с высоким содержанием танинов неохотно). Аналогами танинов, но с гораздо большей молекулярной массой, можно считать гумусовые вещества: гуминовые кислоты, фульвокислоты и т.п. Это еще более конденсированные продукты, чем танины. Гуминовые и фульвокислоты образуются при разложении растений. Они распространены, как в грунте, так и в природных водах и также могут прочно связывать переходные металлы ("тяжелые металлы") в комплексы. Большое преимущество танинов (особенно - для домашней лаборатории) - их доступность. Танины содержатся в коре, древесине, листьях, плодах (иногда семенах, корнях, клубнях) многих растений. Чай, кора и листья дуба, чернильные орешки, кора акации, кора каштана, кожура граната, косточки винограда и многие-многие другие виды растительного сырья могут послужить источником танинов. Для извлечения танинов из растений достаточно обработки горячей водой (можно и холодной, но процесс будет идти медленнее). Если речь идет о медицинском препарате, водную вытяжку последовательно обрабатывают разными несмешивающимися с водой органическими растворителями (хлороформ, этилацетат) для удаления сопутствующих танинам веществ. Как вариант, растворителями предварительно обрабатывают само сухое растительное сырье, а экстракцию танинов проводят этанолом. Примеры методик выделения танинов и родственных соединений - см. Лазурьевский Г. В., Терентьев И. В., Шамшурин А. А. Практические работы по химии природных соединений (1966) [ссылка] - C.248 и далее. Для домашних или лекционных опытов процедура очистки танинов необязательна. Достаточно получить отвар или настой растений (например, заварить чай) и использовать его для проведения характерных реакций. Какие именно реакции можно провести с танинами? Вопрос этот оказался не таким простым, как я думал. С одной стороны, танины - продукты известные с глубокой древности, своего значения они не утратили до сих пор. Следовательно, химия танинов должна быть всесторонне исследована. Так оно и есть. Но попытки найти обзоры и монографии вроде "реакции танинов" или "танины в аналитической химии" не увенчались успехом. Статьи по комплексообразованию танинов, например, с медью или железом (II), (III) - да, фрагменты в монографиях, посвященным аналитической химии или технологии металлов - да, танины с точки зрения фармацевтов - да, но не что-то более общее. Например, в монографии Музгин В.Н., Хамзина Л.Б., Золотавин В.Л., Безруков И.Я. - Аналитическая химия ванадия (1981), С.8 [ссылка] танины приведены в перечне веществ, которые осаждают ванадий - и все. В ГОСТе, который регламентирует анализ титановой губки, указано, что для отделения ниобия и тантала от титана и сопутствующих примесей используют двухразовое осаждение ниобия и тантала танином в соляной кислоте. В записи лекций нашел, что танины могут быть использованы для отделения урана и тория от сопутствующих металлов (каким именно образом - профессор не указывает, а просто вываливает на несчастных студентов длинный список веществ, даже не удосужившись уточнить: в каких комбинациях и для чего конкретно они используются) - [см. И.Н.Бекман - ТОРИЙ. Курс лекций [ссылка]]. Спросил у товарища: - Известно, что танины образуют комплексы с железом (III), а как с другими металлами? - Ты что хочешь связать танинами свои - Нет, конечно. Смерть от - Тогда - двухвалентное железо. - А точно танины образуют комплекс и с двухвалентным железом? - Я брал соли двухвалентного железа, - реагировали так же, как и соли трехвалентного. - Разумеется: реакция чувствительна, а там почти всегда есть примесь трехвалентного железа. - С восстановленным препаратом - тоже. - Возможно, но ты же на воздухе пробовал. Если двухвалентное железо не дает комплекса с каким-то лигандом, а трехвалентное - образует прочный комплекс, то добавление этого лиганда должно облегчить окисление двухвалентного железа в трехвалентное, поскольку оно будет связываться в прочный комплекс. (Позже, правда, в научной статье я нашел, что и двухвалентное железо дает комплексы с танинами). А другие металлы? - Ниобий и тантал, по-моему, осаждаются танинами. Германий - точно осаждается. Это способ выделять германий из надсмольных вод (коксохимических заводов). Интересный получился разговор, но ответ на свой вопрос я так и не получил. Обратился к фармацевтам, точнее - к тому, что они написали. В книге Ковалев В.Н. - Практикум по фармакогнозии (2003) [ссылка] качественные реакции на танины разделены на две группы: "осадочные" и "цветные". Первая группа делится на "общие осадочные реакции": осаждение танинов раствором желатина, солями алкалоидов и солями тяжелых металлов. А также - на "отличительные осадочные реакции": гидролизуемые танины осаждаются раствором ацетата свинца в уксусной кислоте, конденсированные - нет; зато конденсированные дубильные вещества осаждаются бромной водой или формальдегидом в присутствии концентрированной соляной кислоты при нагревании. "Цветные реакции" (не путать с "цветными революциями") - взаимодействие танинов с солями трехвалентного железа; с нитритом натрия и уксусной кислотой (появляется красно-фиолетовая окраска). С ванилином в кислой среде катехины (разновидность конденсированных танинов) дают красную окраску. Другими словами, можно провести реакции танинов с: хлоридом железа (III); с растворимыми белками (не обязательно с желатином); с нитритом натрия и кислотой (нитрита пока под рукой нет, но будем оптимистами!); с ванилином (отсутствует аналогично нитриту, но ванильный сахар продается везде); с солями (подручных) переходных металлов - с заранее неизвестным результатом; дополнительно - действие кислоты и щелочи на танины. |

Танин |

|

Галловая кислота |

|

|

|

|

Гумат натрия |

|
|
Фрукты и совок (лирическое отступление) / Fruits and soviet system (lyrical digression)
Что использовать в качестве источника танинов? Фото "готового" танина и галловой кислоты (см. выше) я сделал уже после того, как начал эксперименты. Коллега узнал, что я заинтересовался танинами и предложил свои реактивы. Но на момент начала экспериментов предстояло выбрать источник танина. К счастью, выбор довольно широкий - это не нитрат уранила и не хлорид европия. В прошлых опытах я брал чай, чернильные орешки, листья дерева сумах оленерогий (см. подборку: Опыты с растениями и насекомыми. Природные вещества / Experiments with Plants and Insects. Natural Products [ссылка]). Позже прочитал, что танинами богата кожура граната. А это - вариант... И название интересное... Возник соблазн написать большими буквами (CapsLock-On) что-то вроде: "гранат является фруктом; схожесть названия "гранат" с называнием соответствующего оружия является случайной и не может быть расценена как пропаганда терроризма" (по аналогии со словесными кривляньями, практикуемыми в одной "далекой и не очень солнечной стране" по поводу статуса "иностранный агент"). Или привести армейскую шутку: "Ты не бойся гранаты - она ручная!" (шутки-шутками, а часть людей боится бросать боевые гранаты - инстинкт самосохранения у них развит сильнее, чем у остальных). Но вместо этого стал вспоминать. С гранатами у меня связаны яркие детские воспоминания. Детство прошло в конце 70-х - начале 80-х в г Киев, Черкассы и в соседнем с Киевом райцентре. Раньше хорошо жилось! Мандарины или апельсины мы видели раза два в год. А, если их и продавали, то часто в комплекте с гнилыми яблоками ("набор фруктовый"): килограмм апельсин - два кило яблочной гнили. Многие выбрасывали яблока, не отходя от кассы (точнее - не отходя от прилавка). Лимоны - бывали чаще, но тоже считались роскошью. Бананы впервые в жизни я увидел примерно в 3 классе средней школы. Ананасы - классе так в 5 (правда, до этого пару раз пробовал консервированные ананасы - не понравились: на вкус - почти никакие). Могли ли мы знать, что через N-лет в Украине настанет период, когда бананы будут продаваться везде и стоить дешевле, чем яблоки!? Зато гранаты во времена моего детства вполне продавались. А люди их не очень-то и покупали. Одним не нравился кислый вкус, другим… доступность. Гонки за дефицитом превратились тогда в своеобразный спорт: если товар продавался свободно, - люди думали, что он плохой. Например, морская рыба тогда была дешевой и доступной, поэтому считалась "едой для бедных". А теперь рыба, и стоит недешево и непрестижной едой не считается… Впрочем, подобное было не только при совке, но и в других странах. Те же устрицы в Европе изначально были едой для малообеспеченных - как дешевый заменитель мяса, но их запасы стремительно стали истощаться, в результате устрицы превратились в дорогой деликатес, который подают в ресторанах. В детстве я очень любил гранаты, зато во взрослом возрасте - успел позабыть: с прилавков они не исчезли, просто стоили гораздо дороже, чем большинство фруктов. А недавно я увидел гранаты почти по цене цитрусовых - вот тогда и вспомнил про опыты с танинами. Купил - и сразу же понял, что я забыл, как чистить кожуру гранатов - чтобы не разбрызгать яркий сок. Вкус граната я тоже уже не помнил. Мораль: прошлое - как настоящее, в нем бывает и плохое, и хорошее. Большинство людей вбили себе в голову, что раньше было все хорошо, или наоборот - все плохо. |

|

|

|
|
Реакция танинов с хлоридом железа (III) / Reaction of tannins with iron (III) chloride
Реакция с катионом трехвалентного железа является характерной для веществ с фенольным гидроксилом, в частности - для танинов. Цвет комплекса может отличаться в зависимости от природы фенольного соединения. Танины дают черную или темно-фиолетовую окраску.Кожуру одного граната залил дистиллированной водой в стакане на 300 мл почти до верха, накрыл, оставил стоять на сутки при комнатной температуре. Получил коричневый настой. Зачем использовать дистиллированную воду? Если повезет, то можно обойтись и без нее. Однако, как показала практика, водопроводная вода может содержать много железа. Иногда реакцию между катионами железа и танинами можно наблюдать даже при попытке вымыть чашку с недопитым чаем (см. статью: Чайная колориметрия [ссылка]).  Железо в питьевой воде Итак, в стакан с настоем кожуры граната добавил несколько капель коричневого раствора хлорида железа (III) (близкого к насыщенному). Перемешал. Результат - интенсивная черная окраска. Сначала использовал неразведенный настой. Во втором опыте развел настой кожуры граната раз 5 дистиллированной водой, результат - тот же: когда капли раствора хлорида железа (III) опускаются на дно, образуются черные вихревые кольца, черные облака и нити, а после перемешивания - непрозрачный черный раствор. В следующих опытах стал разводить настой все сильнее. Под конец развел несколько миллилитров настоя примерно в 150 мл дистиллированной воды, потом - две капли настоя в таком же количестве воды. При добавлении хлорида железа (III) окраска комплекса все рвано была интенсивной. Лишь в последнем случае получился частично прозрачный серый раствор (на видео у самого разведенного раствора - фиолетовый оттенок, вживую он выглядел серым). |

Настой граната и раствор хлорида железа (III) |

Реакция танинов (настой кожуры граната) с хлоридом железа (III) - Показано несколько опытов, причем сверху вниз используется все более разбавленный настой |

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

К настою граната добавим раствор нитрата кобальта |

|

Окраска стала более интенсивной, но не радикально |

Теперь добавим концентрированный раствор аммиака - выпадет обильный коричневый осадок |

|

Через сутки. Сверху - коричневый раствор, потом - слой темного осадка, ниже - зеленый осадок |

|

К настою граната добавим раствор сульфата меди |

|

Раствор станет зеленовато-желтым |

Добавим концентрированный раствор аммиака |

Также выпадет объемный осадок, основная масса которого будет коричневой |

|

|

Через сутки. Сверху - синий раствор, потом - слой светлого голубого осадка, ниже - коричневый осадок |

|