Химия и Химики № 3 2017
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 3 2017 Журнал Химиков-Энтузиастов |
Эксперименты с золотом ч.4, 5 Experiments with gold В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Золото, серная кислота и гипохлорит натрия. Gold, sulfuric acid and sodium hypochlorite
В первой части статьи показано, что золото растворяется в смеси соляной кислоты и пергидроля (30% перекись водорода) [ссылка], причем позолота на фарфоре исчезла под действием этой смеси быстрее, чем под действием царской водки [ссылка]. Кроме царской водки или смеси соляной кислоты и перекиси водорода есть много других веществ и смесей, которые растворяют золото [K1]. С точки зрения доступности компонентов заслуживают внимания смеси сильной минеральной кислоты (соляной, серной, азотной и др.) и гипохлорита натрия. Принцип их действия такой же, как и в случае смеси соляной кислоты и перекиси водорода: в результате реакции между компонентами выделяется хлор, который и растворяет золото. Сильная минеральная кислота реагирует с гипохлоритом, вытесняя слабую хлорноватистую кислоту. Хлорноватистая кислота неустойчива, она существует только в растворе. Но даже в водном растворе она постепенно разлагается. При этом выделяется хлороводород (соляная кислота) и кислород в атомарном виде. Хлороводород окисляется хлорноватистой кислотой с образованием хлора. HClO = HCl + O HClO + HCl = Cl2 + H2O Кстати, в техническом растворе гипохлорита хлорид-ионы есть уже изначально - независимо от первой реакции, просто, чтобы хлорноватистая кислота (гипохлорит) окислила хлорид (соляную кислоту) нужна кислая среда - для этого и добавляют сильную минеральную кислоту. В качестве кислоты я выбрал разбавленную серную кислоту (для разнообразия: поскольку в первой части статьи использовалась соляная кислота; плюс раствор серной кислоты более доступен: он используется в качестве электролита для свинцовых аккумуляторов). Источником гипохлорита натрия служило моющее и чистящее средство "Белизна". В стаканчик поместил осколок фарфоровой чашки с позолотой, добавил 23 мл воды, затем - 2.5 мл концентрированной серной кислоты, перемешал. После этого добавил 1.5 мл "Белизны" (гипохлорит натрия). Позже - еще 0.5 мл "Белизны". "Белизну" добавлял "культурно": медленно, по каплям, стараясь, чтобы каждая капля попала в то место стакана, где находится позолота. В результате хлор выделялся именно в том месте, где находилось золото, а не по всему объему стакана. Это было нужно, чтобы не превращать кухню (где проводился эксперимент) в газовую камеру. Попадание капель гипохлорита в серную кислоту вызывало выделение газа, появился запах хлора (но умеренный, поскольку я добавлял гипохлорит медленно и в умеренных количествах). Слой позолоты довольно быстро стал растворяться, оставляя после себя белый фарфор. Новые капли гипохлорита добавлял в те места, где оставалась не растворившаяся позолота. В результате позолота в течение нескольких минут растворилась. Таким способом можно растворить золото, не имея в своем распоряжении соляной и азотной кислоты или перекиси водорода. |

Золото, серная кислота и гипохлорит натрия Gold, sulfuric acid and sodium hypochlorite |

|

|
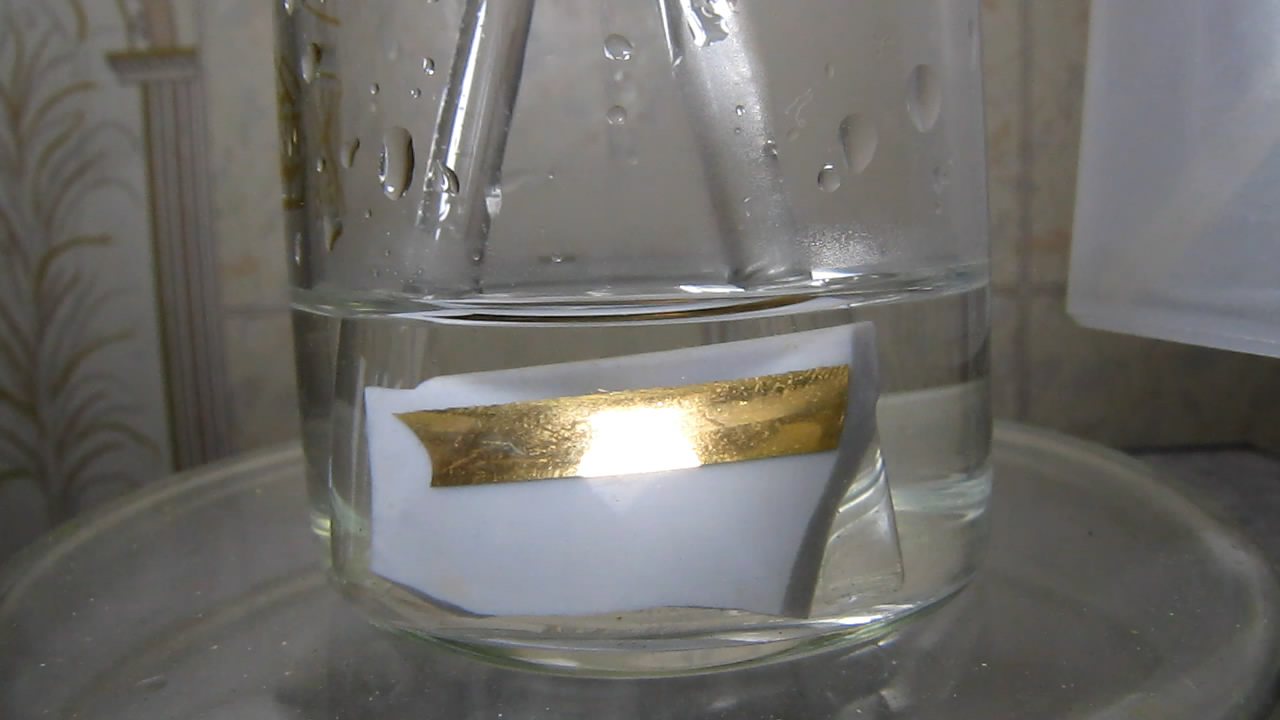
|

|

|

|

|

|

|

|

|

|

|

|

|
|
Большинство способов растворения золота, описанных в предыдущих частях статьи, основаны на растворении золота в хлорной воде (водный раствор хлора). Хлор образуется в результате окисления соляной кислоты (хлороводорода) каким-либо окислителем (перекись водорода, гипохлорит и др.). В случае "царской водки" окислителем служит концентрированная азотная кислота, а кроме хлора с золотом реагирует также хлористый нитроил NOCl. Однако, кроме хлорной воды золото растворяется в водных растворов других галогенов: брома и даже йода.
Недавно к последней части статьи прислали комментарий: "Золото эффективно растворяется в растворах трийодида (в обычной йодной настойке) за счет образования стабильного йодидного комплекса [AuJ2]-. Но дешевым такой способ не является". В свое время я еще в школе так растворил позолоту с осколка бокала. - Тогда даже не мог подумать, что золото растворяется в йоде (попробовал на всякий случай, а когда увидел результат - сильно удивился). Воспроизведем этот опыт. Источником йода послужила аптечная 5% йодная настойка. Она представляет собой раствор йода в смеси воды и спирта, куда дополнительно добавлен йодид калия. Дело в том, что йод плохо растворяется в воде, но хорошо - в спирте (и многих других неполярных или слабополярных органических растворителях). Йодид калия добавляют для увеличения растворимости йода, поскольку он образует с молекулярным йодом комплекс K[I3], или KI·I2. Я взял 3 кусочка фарфора с позолотой (в форме полоски). Далее приготовил раствор: 10 мл спирта, 3 мл воды и несколько капель аптечного раствора йода - до бурой окраски, но чтобы раствор остался прозрачным. Разумеется, можно использовать и просто 5%-ю йодную настойку, однако она непрозрачная: не будет видно, как золото реагирует с йодом под слоем раствора. В первые минуты визуальных изменений не было заметно. Признаки растворения позолоты появились через 10 мин, а через 15 мин произошло практически полное растворение. От золотой полоски остался только коричневый орнамент, который, как выяснилось, оказался не из золота. Повторю то, что уже было сказано: данный способ интересен с точки зрения чистой химии, но с точки зрения практики (если нужно растворить позолоту, а тем более - компактное золото) - есть гораздо более дешевые способы. |
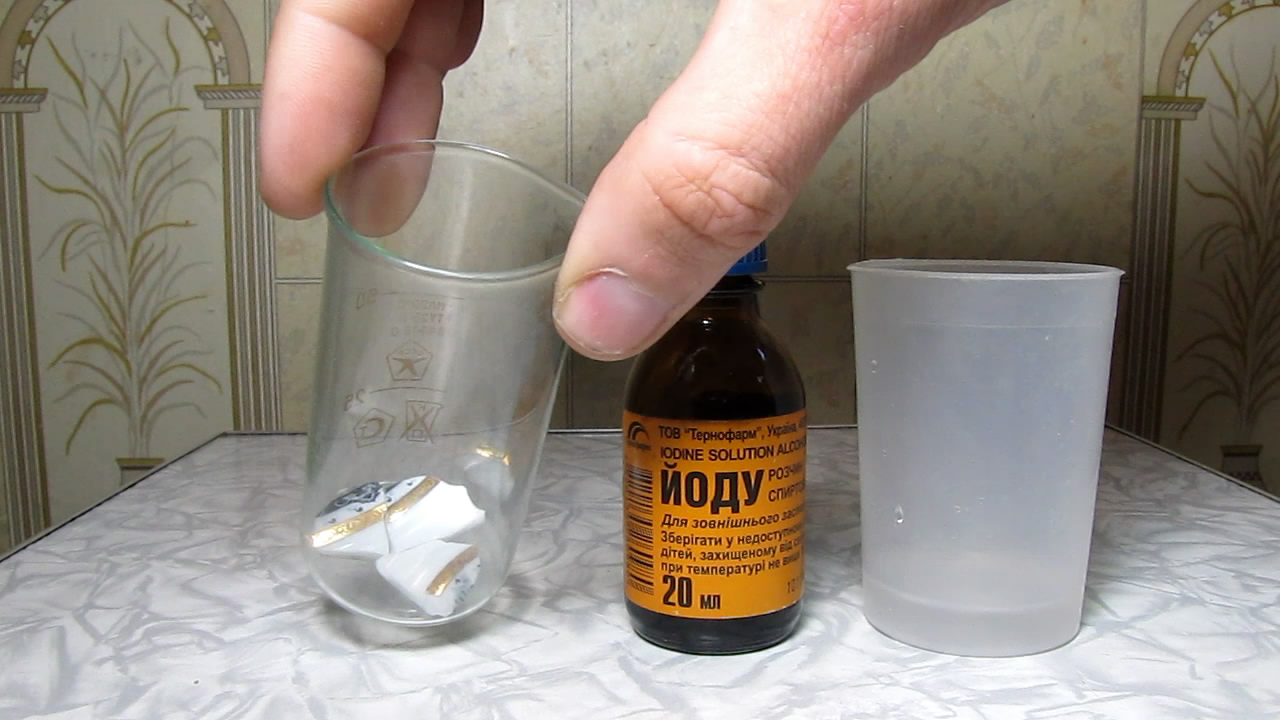
Йод и золото Iodine and gold |

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
|
Комментарии
К1
Золото эффективно растворяется в растворах трииодида (обычной иодной настойке) за счет образования стабильного иодидного комплекса [AuJ2]-. Но дешевым такой способ не является.
|