Но оставим дамскую моду в стороне, хотя нам и придется иметь дело с чулками. Итак, задача: растворить нейлон. Приведу статью про нейлон из Большой Советской энциклопедии.
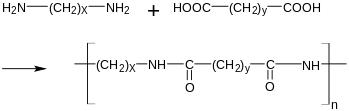
Полигексаметиленадипинамид, [-HN(CH2)6NHCO(CH2)4CO-]n, линейный алифатический полиамид, получаемый поликонденсацией в расплаве соли АГ [из гексаметилендиамина H2N(CH2)6NH2 и адипиновой кислоты HOOC(CH2)4COOH]. П. - роговидный кристаллический полимер белого цвета, без запаха, молекулярная масса 15 000 - 25 000, плотность 1.14 г/см3 (20 °С), степень кристалличности 40-60%, tпл 264 °C. П. - наиболее широко распространённый полиамид; характеризуется высокой прочностью (например, при растяжении 80 Мн/м2, или 800 кгс/см2, при изгибе 100 Мн/м2, или 1000 кгс/см2) и абразивостойкостью; превосходит др. алифатические полиамиды по термостойкости (разлагается выше 350 °C с выделением CO, CO2, NH3). Растворим в концентрированной серной, уксусной и муравьиной кислотах, фторированных спиртах и фенолах, устойчив к действию масел, растворов щелочей; сильно поглощает влагу (поглощение воды при насыщении 9-10%). П. перерабатывают методами, обычными для полиамидов (см. также Поликапроамид); применяют главным образом для изготовления волокон (см. Полиамидные волокна).
П. производят под названием: анид (СССР), найлон-6,6, зайтел-101, зайтел-106 (США), маранил, лурон, сутрон, брулон (Великобритания), перлон Т, игамид А, энтернамид (ФРГ).
В статье указаны следующие растворители для нейлона (точнее - полигексаметиленадипинамида, далее - просто "нейлон"): концентрированная серная кислота, уксусная кислота, муравьиная кислота, фторированные спирты и фенолы. Для начала решил попробовать муравьиную кислоту. Почему именно муравьиную? Если честно, я сначала провел опыт, а только потом прочел приведенную выше статью из БСЭ.
Я помнил, что нейлон хорошо растворим в муравьиной кислоте, кроме того, аналогичные эксперименты недавно провел коллега - ему был нужен раствор полиамидов (в частности - нейлона) для получения мембран. В качестве растворителя он использовал муравьиную кислоту и смеси на ее основе.
Источником нейлона послужили порванные женские чулки, в одном случае - телесного цвета, во втором - черные.
Налил в бюкс примерно 20 мл муравьиной кислоты (98-100%, ч.д.а.) и поместил в него кусок ткани чулка, помешал стеклянной палочкой. В жидкости ткань быстро "распалась" и растворилась, став похожей по виду на крахмальный клейстер. Повторил процедуру уже с бОльшим куском ткани - нейлон быстро растворился.
Взял еще больший кусок ткани - на этот раз черной, поместил в кислоту и помешал палочкой. Ткань начала растворяться, но процесс прошел не мгновенно: сначала нейлон распался на куски, перед растворением значительная часть ткани превратилась в липкую массу. По мере перемешивания липкая масса постепенно растворялась. Визуально это очень напоминало растворение целлюлозы (фильтровальной бумаги) в реактиве Швейцера [2]. Растворил еще один лоскут нейлона - еще бОльший.
Растворение было практически полным (правда, потом нашел на дне бюкса небольшой кусочек нерастворившейся ткани, но, видимо, дело в недостаточно тщательном перемешивании). Раствор нейлона в муравьиной кислоте был подвижным, хотя на вид и гораздо более вязким, чем исходная кислота. Цвет - темно-коричневый. Если будете повторять опыт, - по возможности возьмите бесцветный или светлый нейлон: темный краситель все "забивает".
Эксперимент с полученным раствором (выделение нейлона из раствора) описан в третьей части статьи, во второй части статьи описан аналогичный опыт с раствором нейлона в смеси муравьиной и монохлоруксусной кислот (получен коллегой без моего участия).
Техника безопасности дана во второй части статьи: с муравьиной кислотой лучше не шутить, а с раствором нейлона в муравьиной кислоте - тем более.
__________________________________________________
2 См. статью
Реактив Швейцера и растворение целлюлозы [ссылка]
|