
Магнетит

Магнетит

Вкрапления магнетита и других тяжелых минералов в кварц

Гематит

Маггемит

Добыча железной руды

Добыча железной руды

| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 8 2013 Журнал Химиков-Энтузиастов |
Магнетит - ферримагнитный оксид железа В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Кроме некоторых ферромагнитных металлов и сплавов свойством притягиваться к магниту обладает также ряд оксидов [1]. Пожалуй, самый известный из "магнитных" оксидов - магнетит Fe3O4 - смешанный оксид железа (II, III). Самый известный и самый доступный - он образуется при простом нагревании железа.
Другой оксид железа - Fe2O3 также образует магнитную модификацию - γ-Fe2O3, которая распространена в природе (минерал маггемит) и входит в состав залежей железных руд. Однако гораздо чаще встречается другая модификация оксида железа (III) - минерал гематит, α-Fe2O3, который ферримагнитными свойствами не обладает. Более того, в природных условиях маггемит неустойчив и постепенно переходит в гематит. При умеренном нагревании этот переход происходит быстро. Несмотря на то, что минерал гематит более распространен в природе, чем магнетит и маггемит, залежи железных руд часто обнаруживали именно благодаря магнитным свойствам двух последних минералов. Для этого не обязательно иметь сложные приборы - достаточно обычного компаса. Залежи магнитных руд вызывают заметное (а подчас - сильное) отклонение магнитной стрелки. Впервые я познакомился с магнетитом (если не считать созерцания школьных коллекций минералов) когда положил в печку - сверху горящего антрацита - консервную банку. На раскаленных до желтого цвета углях жесть прогорела насквозь, превратившись большей частью в темные блестящие чешуйки - это и был магнетит. Железо окислилось до оксида Fe3O4. Магнитные свойства последнего обнаружились, когда я поднес к нему железные ножницы. Позже я обратил внимание, что оксид кобальта Co3O4, который образовался при разложении нитрата кобальта, также притягивается магнитом (т.е. обладает ферримагнитными свойствами). Однако, в данном случае важны условия разложения, поскольку состав данного оксида и, по-видимому, - его магнитные свойства сильно зависят от температуры. Из формулы следует, что на один атом кобальта (II) приходится два атома кобальта (III). Другими словами Co3O4 = CoO·Co2O3. Но это не обязательно так: соединение может содержать, как больше, так и меньше кислорода по сравнению с приведенной формулой - в зависимости от условий. __________________________________________________ 1 Имеются в виду вещества, которые притягиваются к магниту со значительной силой, которую легко можно ощутить (например, - ферромагнетики). Кроме них есть много веществ, которые обладают парамагнитными свойствами: такие вещества притягиваются к магниту, но очень слабо, т.к. под действием поля в них возникает лишь слабая магнитная упорядоченность. Чтобы притяжение парамагнитных веществ к магниту стало заметным визуально, как правило, нужны сильные магниты или специальные условия эксперимента. Также много веществ обладает диамагнитными свойствами - отталкиваются от магнита. Под действием внешнего магнитного поля магнитные моменты атомов диамагнитных веществ ориентируются в направлении, противоположном направлению поля. Подробнее о магнитных свойствах веществ - см. статью Точка (температура) Кюри; раздел Магнитные свойства веществ (введение) [ссылка] |

Магнетит |

Магнетит |

Вкрапления магнетита и других тяжелых минералов в кварц |

Гематит |

Маггемит |

Добыча железной руды |

Добыча железной руды |

|
|
До сих пор были упомянуты только три магнитных оксида - γ-Fe2O3, Fe3O4 и Co3O4. Однако кроме данных оксидов существует целый класс аналогичных веществ, которые называются феррИмагнетики. Внешне - по их отношению к магниту такие вещества напоминают феррОмагнетики - такие как железо или неодимовый магнит. Ферримагнетики притягиваются к магниту, поскольку под действием магнитного поля у них также возникает магнитная упорядоченность.
Но внешняя схожесть не отражает физической сути процессов, которые происходят в веществе под действием магнитного поля. В ферромагнетиках магнитные моменты атомов ориентируются в направлении внешнего магнитного поля, причем эта упорядоченность может сохраняться и после снятия внешнего магнитного поля - возникает постоянный магнит (о магнитных свойствах веществ см. ссылку в примечании [1]). В отличие от ферромагнетиков, ферримагнетики состоят как бы из двух решеток (подрешеток), магнитные моменты одной из них ориентируются в направлении внешнего поля, другой - против внешнего поля. Это очень напоминает антиферромагнитные вещества, но есть и существенная разница: в ферримагнетиках магнитные моменты двух подрешеток не равны по величине, хотя и противоположны по направлению. В результате суммарный магнитный момент не равен нулю. 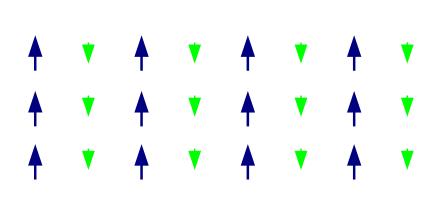
Магнитная упорядоченность в ферримагнетиках В более сложном случае подрешеток может быть не две, а несколько, но непременным является условие: их магнитные моменты направлены антипараллельно [2] и не равны по величине. Такое неравенство обусловлено тем, что разные подрешетки образованы разными атомами и в разном количестве (например, в магнетите - атомами Fe(II) и Fe(III) ). Ферримагнитными свойствами обладают некоторые сплавы металлов, но в основном "привилегию" на данное свойство имеют оксиды, наиболее известными среди которых являются ферриты (именно они и дали название этому типу магнетизма - ферримагнетизм). Ферриты можно рассматривать как смешенные оксиды железа (III) и других металлов. Например, ферриты шпинельного типа [3] имеют формулу MeFe2O4 [или MeO·Fe2O3], где Me = Ni2+, Co2+, Fe2+, Mn2+, Mg2+, Cu2+. Не трудно видеть, что если Me = Fe2+ - мы имеем магнетит. Подобно ферромагнитным металлам и сплавам ферриты обладают хорошими магнитными свойствами но, в отличие от металлов, ферриты имеют низкую электропроводность. Такое сочетание свойств незаменимо для работы с высокими частотами (более 100 кГц). Ферриты используют в качестве магнитных материалов в радиотехнике, электронике, автоматике и вычислительной технике (ферритовые поглотители электромагнитных волн, антенны, сердечники, элементы памяти, постоянные магниты и т.д.). __________________________________________________ 2 Магнитные моменты направлены антипараллельно - т.е. векторы магнитных моментов разных подрешеток параллельны, но направлены противоположно друг другу. 3 Шпинель - природный минерал, оксид магния и алюминия MgAl2O4. Вещества, которые имеют кристаллическую решетку, схожую с кристаллической решеткой шпинели, называют веществами шпинельного типа. |

Шпинель |
|
Вернемся к оксиду железа (II, III) и приступим к экспериментам. Недавно мне выпала еще одна возможность познакомиться с магнетитом. Я положил в муфель кольцо от взорвавшейся гидротермальной бомбы и полоску железа - они служили всего лишь в качестве опоры для электрической лампы, которую я намеревался нагреть. Сначала дал 800°С, потом - 1000°С.
Что случилось с лампой, я надеюсь в ближайшее время описать, железо же покрылось темным слоем магнетита. Магнетит легко счистился с металла - достаточно было простого постукивания. Теперь с помощью магнита от старого радиоприемника можно было продемонстрировать, что магнетит обладает ферримагнитными свойствами. Единственное, при работе с порошками металлов или чешуйками магнетита желательно завернуть магнит в кулек - чтобы потом не пришлось счищать прилипшие частички со всей поверхности магнита. |

Магнетит |

|

|

|

|

|

|

|

|

|

|

|

|

|