
"Замерзание" воды при комнатной температуре (кристаллизация сульфата натрия)

| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 3 2010 Журнал Химиков-Энтузиастов |
 |
"Замерзание" воды при комнатной температуре (кристаллизация сульфата натрия) |

|
|
''Freezing of Water'' at Room Temperature (the Crystallization of Solution of Sodium Sulfate) |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
В прошлом номере журнала мы рассказывали про опыт с пересыщенным раствором ацетата натрия [1] . В плотно закрытой колбе такой раствор может храниться очень долго. Например, раствор, который остался от прошлых опытов, стоит уже второй месяц - без каких-либо признаков кристаллизации. Но стоит открыть колбу и незаметно бросить туда кристаллик ацетата натрия, как произойдет моментальная кристаллизация. Внешне этот процесс очень напоминает замерзание воды. Существуют и другие вещества, с которыми можно провести похожий эксперимент.
ProAlexandr прислал видео и описание опыта по кристаллизации пересыщенного раствора сульфата натрия. Этот эксперимент настолько напоминает кристаллизацию ацетата натрия, что внешне их отличить довольно сложно. Перед тем, как перейти к описанию эксперимента, рассмотрим некоторые свойства сульфата натрия. При комнатной температуре сульфат натрия образует кристаллогидрат с десятью молекулами воды: Na2SO4·10H2O. В природе этот гидрат встречается в виде минерала мирабилита. Другое название декагидрата сульфата натрия - глауберова соль. При увеличении температуры растворимость сульфата натрия в воде быстро растет (см. рисунок). Но когда температура достигает 32.384°C, происходит резкое изменение: дальнейший нагрев приводит не к увеличению, а к уменьшению растворимости соли. Это объясняется тем, что в данной точке гидрат Na2SO4·10H2O переходит в безводную соль, процесс сопровождается плавлением сульфата натрия в собственной кристаллогидратной воде. Максимальная растворимость сульфата натрия составляет 49.7 г Na2SO4 в 100 г воды. Плавление Na2SO4·10H2O можно использовать для калибровки термометров. 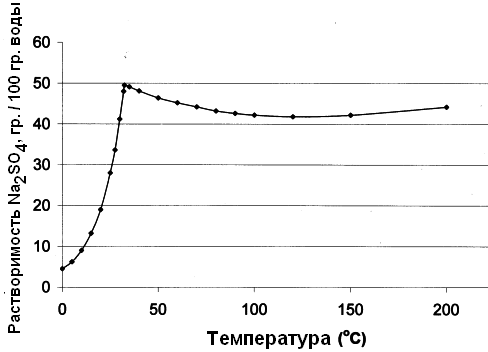
Зависимость растворимости сульфата натрия от температуры __________________________________________________ 1 См. статью "Замерзание" воды при комнатной температуре (кристаллизация ацетата натрия). Химия и Химики. № 2 (2010). [ссылка] |

Мирабилит - природный сульфат натрия Mirabilite (natural sodium sulphate) |

|

|

|

|

|
|
Таким образом, чтобы получить пересыщенный раствор сульфата натрия нужно растворить чуть больше 40 г Na2SO4 (безводной соли) в 100 г горячей воды. Нагревание раствора выше 32.384°C приводит к небольшому уменьшению растворимости соли, но имеет смысл нагреть воду значительно сильнее (вплоть до кипения), поскольку это значительно ускорит процесс растворения. Потом раствор охлаждают в закрытой колбе или пробирке и вносят затравку - кристаллик сульфата натрия. Происходит "моментальное замерзание" жидкости.
Сульфат натрия не является дефицитным веществом, но купить его можно только в магазинах реактивов. Можно ли приготовить сульфат натрия из доступных веществ? Для этого нужны два компонента: серная кислота и питьевая или кальцинированная сода. Разведенную серную кислоту можно купить в автомагазинах (электролит для кислотных аккумуляторов). Уравнение реакции имеет вид:
Для нейтрализации 98 г серной кислоты необходимо 168 г (2 x 84) питьевой соды. При этом образуется 142 г Na2SO4. Концентрация кислоты в электролите ориентировочно составляет 30-35%. Более точную концентрацию H2SO4 можно узнать, измерив, плотность раствора с помощью ареометра. Например, у нас есть 100 г 30% серной кислоты. Количество серной кислоты составляет: 100·0.3/98 = 0.306 моль, для ее нейтрализации необходимо: 2·84·0.306 = 51 г соды. При этом образуется 142·0.306 = 43.5 г сульфата натрия и 2·18·0.306 = 11 г воды. В исходном растворе было 100·(1-0.3)=70 г воды. Суммарное количество воды составляет 70 + 11 = 81 г Таким образом, в 81 г воды растворено 43.5 г сульфата натрия или 53 г Na2SO4 в 100 г воды. Как показали расчеты, при нейтрализации электролита питьевой содой должен образоваться пересыщенный раствор сульфата натрия, однако, ProAlexandr рекомендует такой раствор дополнительно упарить. О полноте нейтрализации серной кислоты можно судить по прекращению выделения углекислого газа при добавлении очередной порции соды. После некоторого упаривания и охлаждения раствор готов к проведению опытов. |

Кристаллизация пересыщенного раствора сульфата натрия ''Freezing of Water'' at Room Temperature (the Crystallization of Solution of Sodium Sulfate) |

|

|

|

|

|

|

|
 |

Добыча сульфата натрия, озеро Chaplin (Канада) |