
Получение иодистого азота (нитрида иода) NI3·NH3










| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 1 2013 Журнал Химиков-Энтузиастов |
Иодистый азот (нитрид иода) NI3·NH3 ч.1 В.Н. Витер |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Иодистый азот (нитрид иода) NI3·NH3 получил широкую известность благодаря неустойчивости и способности взрываться от легкого прикосновения или даже от того, что на него сядет муха. Собственно, и мухе прилетать необязательно: описаны случаи, когда иодистый азот взрывался просто от громкого звука. Взрывчатые свойства иодистый азот имеет только в сухом виде: мокрый иодистый азот не взрывается, но это не означает, что во влажном виде иодистый азот устойчив - он просто "тихо и мирно" разлагается, постепенно теряя свои замечательные свойства [k2].
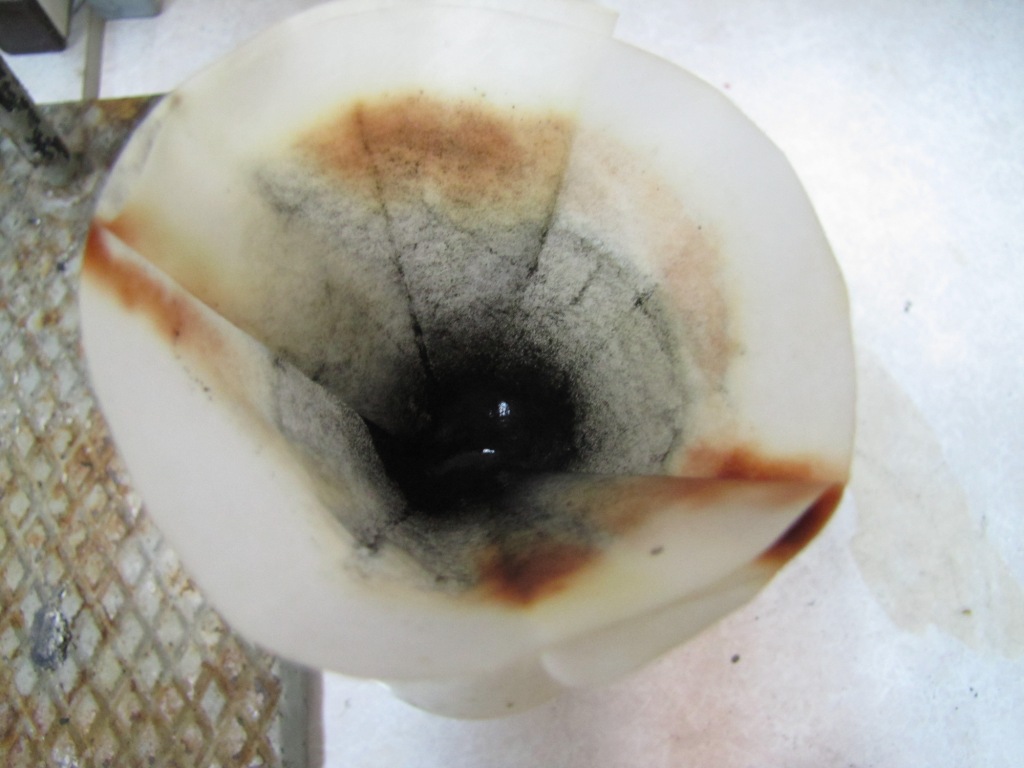
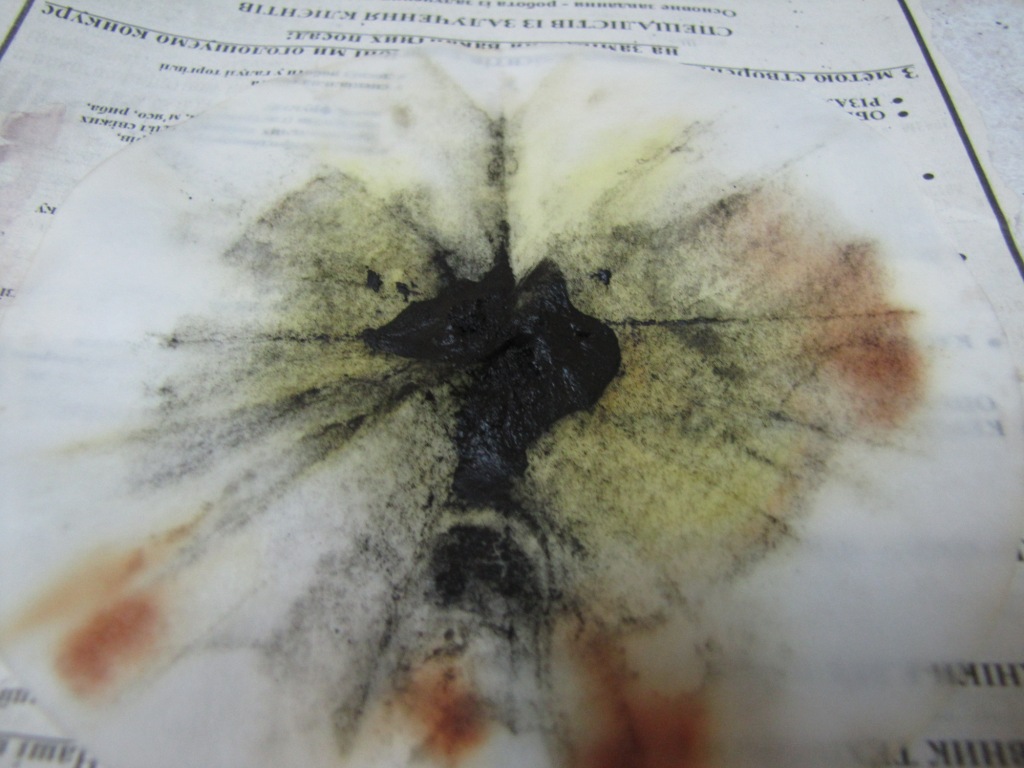
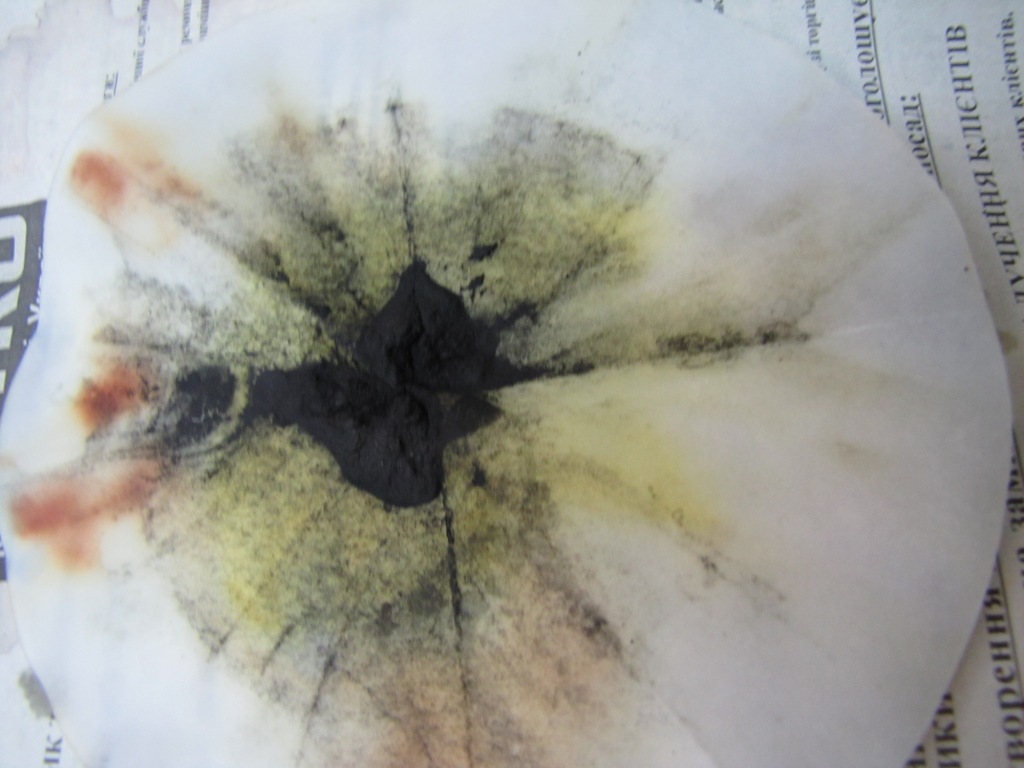
Другая причина известности и популярности иодистого азота - относительная доступность синтеза. Для этого необходимо иметь иод и аммиак. Иод лучше взять кристаллический, но если его нет - подойдет и аптечная иодная настойка. Единственное, из нее нужно для начала осадить иод [1]. Аммиак необходимо использовать концентрированный (25% раствор), но некоторые коллеги утверждают, что смогли приготовить иодистый азот исходя из 10% аптечного раствора аммиака [k1]. Ранее в журнале уже была статья по получению и взрыву иодистого азота [2], в ней рекомендовалось использовать не больше 0.5 г иода за один синтез. В этот раз мы решили несколько нарушить собственную рекомендацию и взяли 1.0 г кристаллического иода. Иод залили избытком аммиака и хорошо размешали, растирая крупинки иода стеклянной палочкой. Образовался серый осадок. Аммиак должен быть в избытке (о чем можно судить по запаху раствора), т.к. иодистый азот в кислой среде разлагается. Осадок отфильтровали на бумажном фильтре и хорошо промыли дистиллированной водой. Это важно, поскольку при получении иодистого азота одновременно образуется и иодид аммония, от которого нужно отмыть осадок. В процессе фильтрования и промывки наблюдалось отчетливое выделение иода - часть фильтровальной бумаги стала коричневой: видимо, иодистый азот заметно разлагается и в мокром виде. На всякий случай осадок промыли небольшой порцией концентрированного раствора аммиака - пятна иода исчезли. Для ускорения будущей сушки осадок напоследок промыли спиртом. После промывки фильтр с осадком оставили на ночь сушиться, положив на металлическое кольцо, закрепленное в штативе. К утру осадок высох, он представлял собой почти черный порошок, на бумаге снова образовались коричневые пятна иода. Осадок слегка потерли длинной проволочкой. Через пару секунд произошел громкий взрыв, образовалось фиолетовое облако паров иода, в фильтре образовалась большая дырка (сам фильтр подбросило). В прошлый раз, когда мы взрывали иодистый азот, осадок высох не полностью (часть его высохла, а часть - нет). В результате значительная часть вещества не взорвалась, а рассеялась по столу. Самое интересное началось уже после взрыва основной порции вещества: стоило провести по столу бумажкой, как многочисленные крупинки иодистого азота начинали "бахать". В этот раз все вышло по-другому: осадок был сухой, в результате практически весь иодистый азот взорвался - потом можно было сколько угодно проводить проволокой или рукой по стулу, на котором был закреплен штатив с осадком, - это не вызвало ни одного мини-взрыва. _____________________________________________________________ 1 Получение иода из аптечной иодной настойки описано в статье Иод из иодной настойки / Химия и Химики № 2 2011 - ссылка. Если вы планируете использовать полученный иод для синтеза иодистого азота, это значительно упрощает описанную в статье процедуру. Влажный осадок иода не нужно не только сушить в эксикаторе и сублимировать, но даже отжимать от воды - его сразу же используют для синтеза иодистого азота 2 См. статью: Получение и взрыв иодистого азота NI3·NH3 / Химия и Химики № 2 2010 ссылка |

Получение иодистого азота (нитрида иода) NI3·NH3 |

|

|

|

|

|

|

|

|

|

|

|

|

|

Взрыв иодистого азота (нитрида иода) NI3·NH3 |

|

|

|

|

|

|

|

|

|

|

|
|
Комментарии читателей
К1
Подтверждаю: я использовал для получения иодистого азота 10% аммиак - получалось. Из йодной настойки йод можно и не осаждать, но тогда "недотрога" получается в виде мелкого порошка (без кристалликов) и выход несколько ниже.
(Феерверкер) К2 Иодистый азот небезопасен и во влажном состоянии, и даже под слоем воды. В годы молодости автор комментария наблюдал взрывное разложение осадка иодистого азота в маточном растворе через несколько секунд после того, как в сосуд попал кристаллик бихромата аммония с загрязненного шпателя. Вполне вероятно, что соединения шестивалентного хрома катализируют разложение иодистого азота - юные экспериментаторы могут это проверить, но с осторожностью. |