Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Синтез перекиси ацетона: что не следует делать
Когда речь заходит о перекиси ацетона (и некоторых аналогичных веществах) обычно говорят: "Нельзя!", "Никогда этого не делайте!", "Вы обязательно останетесь без рук!" и т.п. Нетрудно догадаться, что такого рода запреты не только стимулируют интерес к данному веществу, но и могут служить причиной несчастных случаев.
Получать перекись ацетона будут независимо от запретов - и существует риск, что синтез будет фатальным. Почему? Да потому, что человеку просто говорят: "Нельзя!" и пугают сюжетами из желтой прессы.
Как правило, авторы псевдоморальных предостережений не объясняют: почему именно нельзя, чего следует опасаться, что именно не следует делать и что может случиться, если вы проигнорируете технику безопасности (ТБ).
В химии сформировался двойной стандарт морали: большинство химиков, которые умеют работать руками, делали и делают подобные эксперименты, но в лучшем случае они рассказывают о них в узком круге друзей. Химик без экспериментов - не химик.
Зато официальная версия: "Нельзя!". Более того: этим "Нельзя!" очень часто прикрываются люди, неспособные к работе руками (которая является основной для химика).
Если сравнить современные учебники или практикумы с более ранними изданиями, то это сравнение будет далеко не в пользу первых. В старых учебниках и практикумах все излагается четко, конкретно и в доступной форме. В новых книгах материал дается размыто и бессистемно: главного не дают, зато уделяют большое внимание второстепенным деталям. Почему? Да потому, что учебники нередко пишут "бумажные химики", неспособные к работе химика вообще, и к работе в лаборатории в частности.
Вернемся к перекиси ацетона и постараемся ответить на вопрос: "Что именно опасно?". Начнем с синтеза.
Получать перекись ацетона будут независимо от запретов - и существует риск, что синтез будет фатальным. Почему? Да потому, что человеку просто говорят: "Нельзя!" и пугают сюжетами из желтой прессы.
Как правило, авторы псевдоморальных предостережений не объясняют: почему именно нельзя, чего следует опасаться, что именно не следует делать и что может случиться, если вы проигнорируете технику безопасности (ТБ).
В химии сформировался двойной стандарт морали: большинство химиков, которые умеют работать руками, делали и делают подобные эксперименты, но в лучшем случае они рассказывают о них в узком круге друзей. Химик без экспериментов - не химик.
Зато официальная версия: "Нельзя!". Более того: этим "Нельзя!" очень часто прикрываются люди, неспособные к работе руками (которая является основной для химика).
Если сравнить современные учебники или практикумы с более ранними изданиями, то это сравнение будет далеко не в пользу первых. В старых учебниках и практикумах все излагается четко, конкретно и в доступной форме. В новых книгах материал дается размыто и бессистемно: главного не дают, зато уделяют большое внимание второстепенным деталям. Почему? Да потому, что учебники нередко пишут "бумажные химики", неспособные к работе химика вообще, и к работе в лаборатории в частности.
Вернемся к перекиси ацетона и постараемся ответить на вопрос: "Что именно опасно?". Начнем с синтеза.
Возможные опасности при синтезе перекиси ацетона.
Во-первых, ни в коем случае не следует брать большие количества исходных веществ - это более-менее понятно [ < см. методику в ч. 2 >].
Во-вторых, при получении перекиси ацетона из перекиси водорода, ацетона и соляной кислоты смесь необходимо хорошо охлаждать. Практически смесь ставят на ледяную баню, а в вещества перед смешиванием бросают кусочки снега или льда. Не забывайте также о хорошем перемешивании.
Зачем нужно охлаждение?
Если проводить синтез без охлаждения, может образоваться хлорацетон - вещество, обладающее сильным слезоточивым действием. При реакции перекиси водорода и соляной кислоты образуется хлор, который реагирует с ацетоном, давая хлорацетон.
В первых экспериментах автор пренебрег охлаждением, в результате сильно наплакался (в самом буквальном смысле).
Более того, раньше мне приходилось проводить взаимодействие ацетона и брома. Как известно, при этом образуется бромацетон и бромистый водород. Бромацетон - также известный лакриматор (вещество со слезоточивым действием). В колбочку с ацетоном я добавил несколько миллилитров брома. Произошло активное выделение газа, из колбы ударил фонтан тумана бромистого водорода, однако заплакать не пришлось. Слезоточивое действие бромацетона ощущалось, только если наклониться над колбой. Туман бромистоводородной кислоты досаждал больше.
В случае с хлорацетоном все было гораздо хуже - он более летучий.
Но есть еще одна причина, почему синтез перекиси ацетона следует проводить при хорошем охлаждении - в противном случае вещество разложится прямо в растворе. Ниже дано видео неудачных экспериментов, на котором видно, как образуется белый осадок перекиси ацетона, который сразу же разлагается с активным выделением газов. На дне собралась коричневатая жидкость, вероятно, это и был хлорацетон.
Во втором неудачном эксперименте я смешал ацетон и соляную кислоту, смесь охладил и аккуратно добавил к ней неохлажденную перекись водорода. Сначала все было нормально, но в момент, когда я поставил стаканчик со смесью в лоток с водой и снегом, началось бурное выделение газов: перекись ацетона разложилась.
В дальнейшем я тщательно охлаждал исходные вещества, а в перекись водорода добавлял снег [ < см. ч. 2 >].
Во время проведения опытов я не мог понять, какое слезоточивое вещество образуется, но потом Александр подсказал, что это хлорацетон. Чуть позже в книге Вейганд-Хильгетаг Методы эксперимента в органической химии ссылка. нашел методику синтеза хлорацетона. Как видите, исходными веществами служат ацетон и хлор.
Во-вторых, при получении перекиси ацетона из перекиси водорода, ацетона и соляной кислоты смесь необходимо хорошо охлаждать. Практически смесь ставят на ледяную баню, а в вещества перед смешиванием бросают кусочки снега или льда. Не забывайте также о хорошем перемешивании.
Зачем нужно охлаждение?
Если проводить синтез без охлаждения, может образоваться хлорацетон - вещество, обладающее сильным слезоточивым действием. При реакции перекиси водорода и соляной кислоты образуется хлор, который реагирует с ацетоном, давая хлорацетон.
В первых экспериментах автор пренебрег охлаждением, в результате сильно наплакался (в самом буквальном смысле).
Более того, раньше мне приходилось проводить взаимодействие ацетона и брома. Как известно, при этом образуется бромацетон и бромистый водород. Бромацетон - также известный лакриматор (вещество со слезоточивым действием). В колбочку с ацетоном я добавил несколько миллилитров брома. Произошло активное выделение газа, из колбы ударил фонтан тумана бромистого водорода, однако заплакать не пришлось. Слезоточивое действие бромацетона ощущалось, только если наклониться над колбой. Туман бромистоводородной кислоты досаждал больше.
В случае с хлорацетоном все было гораздо хуже - он более летучий.
Но есть еще одна причина, почему синтез перекиси ацетона следует проводить при хорошем охлаждении - в противном случае вещество разложится прямо в растворе. Ниже дано видео неудачных экспериментов, на котором видно, как образуется белый осадок перекиси ацетона, который сразу же разлагается с активным выделением газов. На дне собралась коричневатая жидкость, вероятно, это и был хлорацетон.
Во втором неудачном эксперименте я смешал ацетон и соляную кислоту, смесь охладил и аккуратно добавил к ней неохлажденную перекись водорода. Сначала все было нормально, но в момент, когда я поставил стаканчик со смесью в лоток с водой и снегом, началось бурное выделение газов: перекись ацетона разложилась.
В дальнейшем я тщательно охлаждал исходные вещества, а в перекись водорода добавлял снег [ < см. ч. 2 >].
Во время проведения опытов я не мог понять, какое слезоточивое вещество образуется, но потом Александр подсказал, что это хлорацетон. Чуть позже в книге Вейганд-Хильгетаг Методы эксперимента в органической химии ссылка. нашел методику синтеза хлорацетона. Как видите, исходными веществами служат ацетон и хлор.
Получение хлорацетона.
В колбу загружают 500 г ацетона и 125 г измельченного в порошок мрамора. Охлаждают проточной водой и пропускают в реакционную массу умеренный ток хлора, при этом добавляя по каплям 315 мл воды. Температура реакционной смеси должна быть не выше 30°С и не ниже 10°С. После растворения почти всего мрамора температуру повышают до 40°С и поддерживают ее в течение нескольких часов до окончания выделения CO2. Следят за тем, чтобы в смеси все время оставался мрамор, в случае надобности его добавляют в небольшом количестве. По окончании реакции отделяют в делительной воронке образовавшийся верхний слой и подвергают его фракционной перегонке, собирая продукт с температурой кипения 118-120°С.
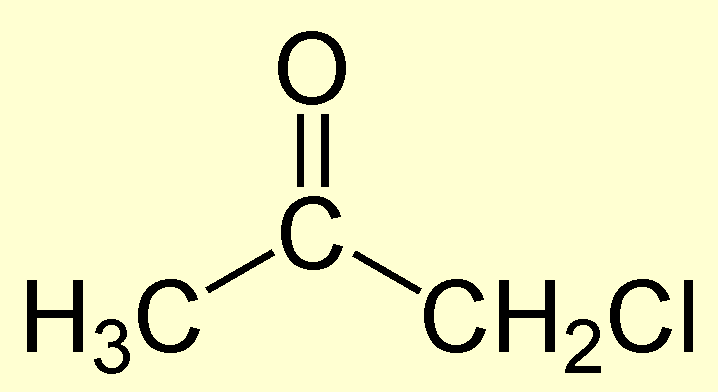
Хлорацетон 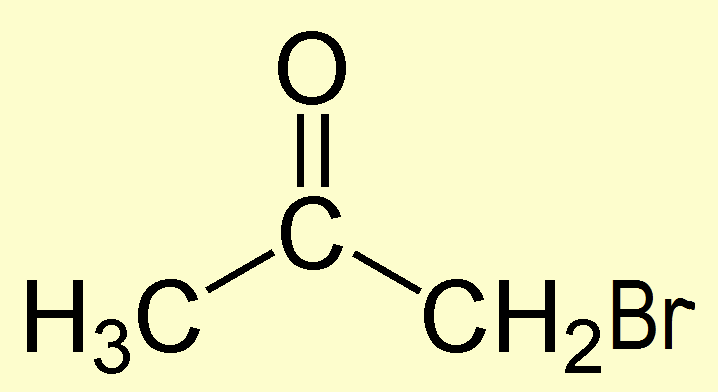
Бромацетон |
Во второй части статьи описана методика получения перекиси ацетона с использованием соляной кислоты, но вместо соляной подойдут и другие кислоты, например, разбавленная серная или даже лимонная. Есть, правда, указания, что перекись ацетона, полученная с использованием серной кислоты, менее стабильна (поскольку кроме триперекиси ацетона она содержит также диперекись). Насколько это соответствует действительности, я не знаю (сравнительных экспериментов не проводил).
В следующем подразделе (4-2) мы рассмотрим опасности, которые подстерегают экспериментатора при обращении с полученной перекисью ацетона.