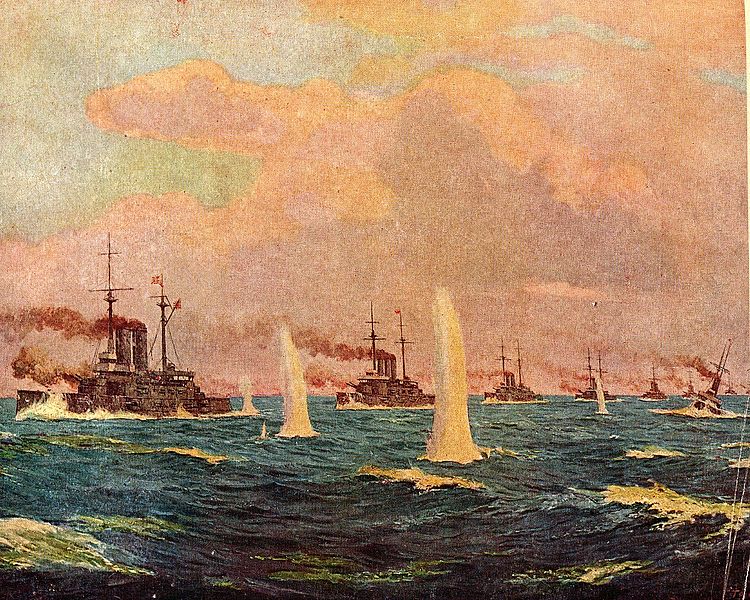
Цусимское сражение

Крейсер Олег после Цусимской битвы

Взрыв английского линейного крейсера Queen Mary (Ютландский бой)
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 4 2013 Журнал Химиков-Энтузиастов |
Пикриновая кислота (2,4,6-тринитрофенол) ч.1 Козьма Прутков |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Вступление
Пикриновая кислота - одно из первых взрывчатых веществ, которое получило массовое применение. Многие века практически единственным взрывчатым веществом оставался черный (дымный) порох. Наряду с преимуществами он имел и массу недостатков, в частности, недостаточную бризантность [1]. Только в девятнадцатом веке массовое применение получил нитроглицерин и взрывчатые вещества на его основе - динамиты.
Нитроглицерин и динамиты значительно превосходили черный порох по силе взрыва, но были опасны в обращении, несмотря на это они активно применялись в горной промышленности, при прокладке дорог и т.п. С использованием в военном деле было сложнее: нитроглицерин и динамиты можно было использовать лишь для снаряжения мин и других "стационарных боеприпасов". При попытке начинить динамитом снаряды, они часто взрывались еще в стволе пушки. Позже военные стали использовать другой эфир азотной кислоты - нитроцеллюлозу (пироксилин). Начиненные пироксилином снаряды были более безопасны в обращении, но имели массу недостатков (в частности, пироксилин нужно было увлажнять). На смену нитроцеллюлозе пришла пикриновая кислота: она обладала высокой бризантностью и была сравнительно безопасна при условии надлежащего обращения. Приведем фрагмент из книги А. Штетбахер Пороха и взрывчатые вещества (1936) [ссылка]: Вследствие высокой плотности заряжания и скорости детонации пикриновая кислота принадлежит к сильнейшим военным взрывчатым веществам; до [первой] мировой войны она оставалась наиболее бризантным материалом для снаряжения снарядов. 27 мая 1905 года в районе острова Цусима (в проливе между Кореей и Японией) состоялось сражение между флотами России и Японии. Русский флот потерпел сокрушительное поражение, основной причиной которого были безграмотные действия командования. Однако не последнюю роль сыграло и то, что снаряды русских кораблей были оснащены пироксилином (который к тому же слишком сильно увлажнили), а японские снаряды были начинены пикриновой кислотой (японцы называли пикриновую кислоту "шимозе"). К сожалению, термин "надлежащее обращение" предусматривает знание свойств вещества. Пикриновая кислота является сильной кислотой и легко образует соли с металлами, что учитывалось далеко не всегда. Дело в том, что многие из солей пикриновой кислоты чувствительны к ударам. Поскольку в девятнадцатом (да и в двадцатом) веке корпуса большей части боеприпасов были сделаны из металла, "незапланированное" образование пикратов стало причиной большого числа несчетных случаев. В частности от неожиданного взрыва погиб офицер артиллерии С.В. Панпушко и два его помощника. Панпушко был одним из первых, кто занимался разработкой боеприпасов с пикриновой кислотой в России. На смену пикриновой кислоте пришел тринитротолуол (ТНТ, тротил). По взрывчатым свойствам он уступал пикриновой кислоте, но отличался куда большей стабильностью (в частности, "просто так" он не образует соли с металлами). Это означало не только большую безопасность в обращении, но и более высокие боевые характеристики снарядов, что в полной мере проявилось во время Ютландского морского сражения между флотами Великобритании и Германии. Формально сражение окончилось вничью, реально - британцы смогли вытеснить немцев с морских просторов: после Ютландского боя крупные силы немецкого флота больше никогда не выходили в море. Однако потери британцев были намного выше. Благодаря использованию снарядов с тротилом немцы смогли нанести большой урон британскому флоту, который значительно их превосходил (в частности, затонуло три новых британских линейных крейсера). Если бы немецкие снаряды были начинены не тротилом, а пикриновой кислотой - потери англичан были бы гораздо меньше. _________________________________________________________ 1 Бризантность - способность взрывчатого вещества разрушать окружающие тела. |
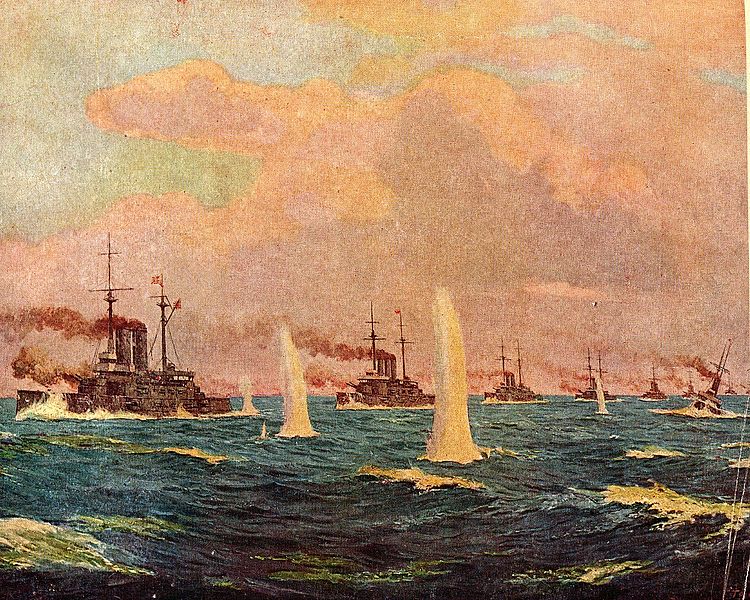
Цусимское сражение |

Крейсер Олег после Цусимской битвы |

Взрыв английского линейного крейсера Queen Mary (Ютландский бой) |
|
При словах "пикриновая кислота" многие вспоминают взрывчатку, однако у данного вещества много других применений. Задолго до того, как стало известно, что пикриновая кислота является взрывчатым веществом, ее использовали для крашения шерсти и шелка. Более того, даже после того, когда были открыты взрывчатые свойства пикратов металлов, многие считали, что сама кислота взрывчатыми свойствами не обладает. В том, что пикриновая кислота - хороший краситель, убедились многие люди, которые с ней работали. Их легко можно узнать - по желтым рукам и лицам.
Сегодня пикриновая кислота не применяется для крашения текстиля, но продолжает активно использоваться в гистологии - для окрашивания биологических препаратов с целью изучения их структуры под микроскопом. Стандартным методом в гистологии является окраска препаратов по Ван Гизон. В данном методе используется смесь кислого фуксина и пикриновой кислоты. В результате разные элементы ткани приобретают контрастную окраску, благодаря которой они становятся хорошо различимыми под микроскопом. Пикриновая кислота применяется в аналитической химии (реактив на алкалоиды), также она является промежуточным продуктом в органическом синтезе (в частности - при получении красителей). Соли пикриновой кислоты - пикраты могут быть использованы в пиротехнике, например, они входят в некоторые свистящие составы. |
Образец ткани, окрашенный по Ван Гизону |
Пикриновая кислота (2,4,6-тринитрофенол) ч.2 Козьма Прутков |
|
Получение пикриновой кислоты
В литературе описано много разнообразных способов получения пикриновой кислоты: от осторожного нитрования раствора фенола в парафиновом масле, до окислительного нитрования бензола в азотной кислоте в присутствии катализатора - соли ртути.
Однако многообразие методов еще не означает, что всеми этими методами можно и нужно пользоваться на практике. Решил использовать один из классических способов - сульфирование фенола с последующим нитрованием образовавшейся смеси сульфофеноловых кислот. Методика синтеза приведена в книге А.А. Солонина Лабораторное приготовление взрывчатых веществ. Пособие для практических занятий в лаборатории (1925) [ссылка]: К 10 гр. фенола приливают осторожно 45 гр. концентрированной серной кислоты; смешение производят в сосуде с притертой пробкой и после прилития серной кислоты взбалтывают несколько раз смесь и затем дают ей стоять до тех пор, пока проба смеси, разбавленная водой, не дает осадка фенола, так как фенол растворяется труднее сульфофеноловой кислоты; в колбу наливают 75гр. азотной кислоты (уд. в. 1,4) и начинают из капельной воронки понемногу капать сульфеноловую смесь и по временам взбалтывают колбу; при этом нитровании выделяются красно-бурые пары окислов азота, которые отводятся при помощи трубки в отверстие тяги. Затем смесь нагревают в продолжение 1-2 часов на водяной бане, пока еще заметно действие азотной кислоты. Жидкость теряет свой первоначальный темный цвет и окрашивается в желтый. Если, как это иногда бывает (обыкновенно, если ошибочно взято мало азотной кислоты), отделяется темно-желтое масло, состоящее, главным образом, из динитрофенола, то для окончательного превращения динитрофенола в пикриновую кислоту надо упарить на песочной бане смесь до 2/3 объема и вновь заменить дымящейся азотной кислотой убыль жидкости. Жидкость опять нагревают на водяной бане до тех пор, пока проба смеси, будучи разбавлена холодной водой, не выделит желтых кристаллов, растворяющихся в чистой кипящей воде без мути и следов масла. Наконец, через еще горячую смесь, продувают воздух; для этой цели опускают стеклянную трубку в смесь и, соединивши эту трубку с каучуковым шаром или мехом, продувают воздух до тех пор, пока не перестанут выделяться красно-бурые пары окислов азота. Смесь из колбы выливается в избыток холодной воды, которую через некоторое время, когда пикриновая кислота осядет, при помощи сифона сливают и заменяют свежей. При помощи фарфоровой воронки и водяного насоса фильтруют пикриновую кислоту и, растворивши при нагревании в небольшом количестве воды (20ч. воды на 1ч. кислоты), оставляют пикриновую кислоту выкристаллизовываться. Выкристаллизовавшуюся пикриновую кислоту фильтруют опять при помощи фарфоровой воронки и водяного насоса и сушат на часовом стекле или в фарфоровой чашке при температуре 35°С до постоянного веса. Охлаждают в эксикаторе и затем взвешивают. Температура плавления пикриновой кислоты должна быть близка к 121°С. Хорошая пикриновая кислота при нагревании в течении трех часов при 100°С не должна изменяться в цвете и не должна становиться тестообразной. Следовательно, первым этапом синтеза является сульфирование фенола концентрированной серной кислотой. В методике указано количество фенола в 10 г, но я уменьшил количества веществ вдвое: для многих опытов вполне хватит того количества пикриновой кислоты, которое получается из 5 г фенола. В распоряжении имелся только старый фенол (1986 года изготовления). Для большинства реактивов срок хранения не критичен, однако фенол легко окисляется на воздухе и теряет свои свойства. Так, автор видел банку фенола меньшей давности (1990 года), все содержимое которой превратилось в ярко-красную вязкую жидкость, в то время как чистый фенол - бесцветные кристаллы. Тем не менее, открыв банку, автор немало удивился - фенол только в верхнем слое порозовел (что указывало на окисление), а дальше он представлял собой бесцветные кристаллы. Таким образом, фенол оказался пригодным для синтеза. |
Фенол (карболовая кислота) |
|
В маленькую колбу отвесил 5 г фенола, после чего прилил 30 г концентрированной серной кислоты. Жидкость немного потемнела. Колбу поставил на электрическую плитку. Вскоре, фенол расплавился и собрался в виде бесцветной жидкости над темным слоем серной кислоты. Еще через 10 минут фенол полностью растворился в кислоте. Колбу охладил, сульфофеноловую смесь перелил в капельную воронку.
|
|
В коническую колбу налил 50 мл азотной кислоты (в методике указано 75, при уменьшении объема вдвое следовало бы использовать 37.5 мл, но кислота была плотностью 1.38, вместо указанных в методике 1.4). Из капельной воронки начал довольно медленно, с перемешиванием прикапывать смесь сульфокислот.
|
|
Вскоре начали выделяться нитрозные газы, установку пришлось вынести на улицу.
|
|
После добавления всего раствора колбу вначале поставил на плитку, а после нагрева примерно до 100°С - на водяную баню.
|
|
Еще при предварительном нагреве на плитке раствор стал мутным - начали образовываться кристаллы пикриновой кислоты.
Примерно через 30 минут выделение оксидов азота прекратилось. Раствор вылил в химический стакан с 150 мл холодной воды. Мелкие кристаллы пикриновой кислоты выглядели весьма красиво на солнечном свету. |
|
Взвесь кристаллов отфильтровал через отрезок ткани, после чего поместил в стакан с кипящей водой, растворил и охладил, проведя таким образом перекристаллизацию пикриновой кислоты.
Выпадающие при охлаждении игольчатые кристаллы выглядят чрезвычайно красиво, напоминая известный опыт "золотой дождь" (кристаллизация иодида свинца [2]). _________________________________________________________ 2 См. статью Золотой дождь - осаждение иодида свинца PbI2 [ссылка]. |
|
После полного охлаждения раствора кристаллы отфильтровал на бумажном фильтре, отжал, накрыв кружком фильтровальной бумаги, и высушил на улице на солнечном свету. Это было ошибкой - сильный ветер, который был в тот день, занес в чашку с кислотой несколько песчинок. Не смертельно, но неприятно.
|
Пикриновая кислота |
|
Общий выход получился немногим больше 8 г, это составляет около 160 % от массы исходного фенола, что довольно неплохо, учитывая потери при перекристаллизации.
Любопытно, что раствор пикриновой кислоты окрашен в ярко-желтый цвет, такие же пятна она оставляет на руках при попадании раствора, в то время как по литературным данным идеально чистая пикриновая кислота представляет собой бесцветные кристаллы [3]: Абсолютно чистая пикриновая кислота (так же как и γ-изомер) бесцветна и только на воздухе, вероятно от действия следов аммиака, образующего с нею интенсивно желтый пикрат аммония, окрашивается в желтый цвет. Возможно, что причину окрашивания следует искать в частичном превращении первоначальной бесцветной бензоидной формы в желтую хиноидную форму, тем более что пикрат аммония, употреблявшийся американцами как до мировой войны, так и во время нее, существует в двух хромоизомерных формах. [K1] _________________________________________________________ 3 См. книгу А. Штетбахер Пороха и взрывчатые вещества (1936) [ссылка]. |
|
Комментарии
К1
Жёлтый цвет пикриновой кислоте придаёт её анионная форма. Влаги воздуха, а тем более влаги после перекристаллизации из воды достаточно для образования ничтожного количества крайне яркого иона, в итоге кислота выглядит светло-жёлтой. В отсутствие следов воды пикриновая кислота не имеет окраски, например, её раствор в сухом бензоле бесцветен.
|