Химия и Химики № 7 2016
Журнал Химиков-Энтузиастов
| Оглавление | Видео опыты по химии | Видео опыты по физике | На главную страницу |
|
Химия и Химики № 7 2016 Журнал Химиков-Энтузиастов |
Металлический цезий ч.3, 4 Metallic caesium (cesium) Добрый Химик, Злой химик |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Разложение азида цезия
Цезий - самый тяжелый и самый активный щелочной металл (если не считать франций). Одновременно цезий - самый легкоплавкий металл (не считая франция и токсичной ртути). Разумеется, перспектива получить цезий в домашних условиях выглядит весьма привлекательно. В данном номере журнала уже была статья, в которой описано получение металлического цезия из фторида [1]. Восстановителем служил металлический литий, причем вместо лития для этой цели прекрасно подойдут кальций, магний и даже алюминий. Недостатком данного способа является необходимость использовать муфельную печь (или другой нагревательный прибор, способный нагреть металлический реактор до температуры порядка 800-1000°С), а также - необходимость использовать поток аргона (инертный газ) и вакуум. Кроме того, нужно изготовить металлический реактор. Все это можно сделать дома (особенно, если для лабораторных целей есть отдельный сарай или гараж), но затраты труда и времени будут ощутимыми.
Caesium azide decomposition А нельзя ли получить металлический цезий как-нибудь проще? Хотя бы, чтобы увидеть небольшое количество металла, перед тем, как он окислится. Небольшие количества натрия и калия можно получить разложением соответствующих азидов. В свою очередь азиды можно синтезировать с помощью реакции между гидразином N2H4 и эфирами азотистой кислоты HNO2 - органическими нитритами в присутствии гидроксидов соответствующих металлов - натрия или калия (эфиры азотистой кислоты могут быть с различными спиртами, например, с н-бутанолом). Азиды других металлов можно получить по реакциям обмена. Получение и разложение азида калия мы недавно описывали [2]. Азид калия разлагается сравнительно спокойно, причем образующийся металл собирается в одну каплю. Таким способом удобно получать небольшие количества калия, а затем сразу же использовать их для простых экспериментов. Цезий близок по свойствам к металлическому калию, поэтому я ожидал, что небольшие количества металлического цезия удастся получить разложением азида. Свойства и превращения азидов щелочных металлов хорошо описаны в книге Л.И. Багал Химия и технология инициирующих взрывчатых веществ (1975), С. 158-161 [ссылка], в частности, в этой книге приводится таблица с данными о выходах щелочного металла при разложении соответствующего азида: 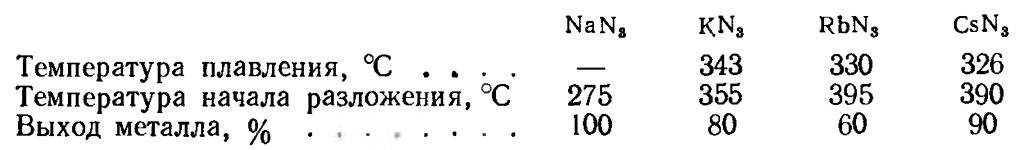 Из чего получить азид цезия? Был у меня раствор, приготовленный для пламенного абсорбционного фотометра, он содержал: хлорида лантана - 100 г/л и хлорида цезия - 8 г/л. Возник вопрос: каким простым способом отделить цезий от лантана? Обычно лантаноиды осаждают в виде оксалатов (осадителем служит щавелевая кислота или ее соли). Чтобы не вносить лишних катионов, осадил лантан щавелевой кислотой, профильтровал. Осталась "мелочь" - перевести хлорид цезия в карбонат. Согласно методике, приведенной в монографии Г. Брауер (ред.) Руководство по препаративной неорганической химии, С.464 [ссылка] чистые карбонаты щелочных металлов от натрия до цезия получают из хлоридов следующим образом. Сначала хлориды переводят в нитраты путем обработки избытком азотной кислоты. После удаления хлора полученные нитраты обрабатывают четырехкратным избытком кристаллической щавелевой кислоты в платиновых чашках и, наконец, превращают их в чистые карбонаты путем прокаливания.  Из карбоната цезия обменной реакцией с азидом бария получил немного азида цезия - примерно 2.2 г. Высушил его над серной кислотой. __________________________________________________ 1 О простом способе получения металлического цезия / Simple method of metallic caesium preparation [ссылка] 2 Азид калия (получение и разложение) / Potassium azide (preparation and decomposition) [ссылка] |

Азид цезия и азид калия. Азид цезия имеет желтоватый оттенок. Азид калия чисто белого цвета Caesium azide and potassium azide |
|
Пробовал разложить азид цезия в кварцевых цилиндриках (в таких цилиндрах я разлагал азиды калия и бария [2]). При нагревании азид цезия вначале плавится, появляются пузырьки, соль желтеет. Потом происходит резкое разложение азида с выбросом продуктов реакции (примерно, как в случае азида калия). В результате на стенках цилиндра получается красновато-желтый налет цезия, быстро исчезающий. В отличие от калия, цезий не собирался в капли. Плохо также, что реакция идет более бурно, чем в случае азида калия. Калий можно получить в пробирке разложением азида, пусть и небольшой кусочек. Этого калия хватает на несколько реакций с водой. А вот цезий "просто так" не получается.
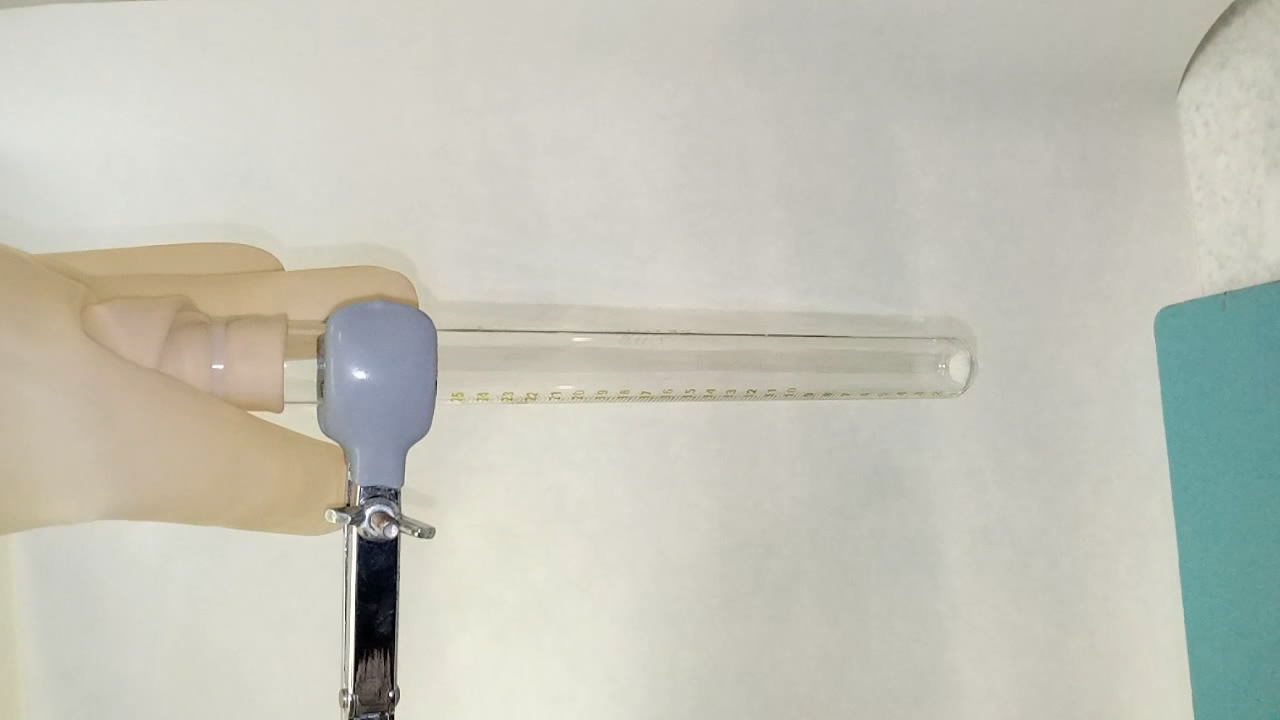
Решил еще несколько раз провести разложение азида цезия с целью все-таки получить металлический цезий. Разлагал примерно 0.5 г азида цезия в пробирке, заранее продув аргоном и нацепив сверху резиновую перчатку, наполовину наполненную аргоном (использовать воздушный шарик вместо перчатки не рекомендую: его может разорвать при разложении). Вначале вещество плавится и желтеет, затем большая часть пробирки мгновенно, с хлопком покрывается зеркалом из цезия. Золотистым и довольно красивым. Но далее зеркала дело не идет. В этом отличие цезия от калия: разложение азида калия идет спокойнее, калий собирается в крупные капли, которые затем сливаются в одну каплю. Была мысль соскрести цезий со стенок пробирки. Внутрь пробирки с помощью шприца налил "осч" гексан (чтобы не нарушить инертную атмосферу, перчатку проколол шприцом). Слой цезия быстро потускнел и начал исчезать. Если просто срезать резиновую перчатку и пустить в систему воздух, цезиевое зеркало на стенках пробирки исчезает за считанные секунды. Вывод напрашивается неутешительный: вряд ли можно получить простым способом существенные количества цезия путем разложения азида. А как же литературные данные, согласно которым при разложении азида цезия выход металла даже выше, чем при разложении азида калия? Лабораторные методики получения металлического цезия разложением азида цезия предусматривают разложение азида в высоком вакууме со строгим соблюдением температурного режима, причем реакция длится очень долго - несколько дней. Никто не утверждает, что "цезий из азида получить нельзя", но на коленках это вряд ли реально. Ниже приведено видео разложения азида цезия, которое я снял "ради самого процесса" - к тому времени уже не было надежды получить металлический цезий разложением азида. |
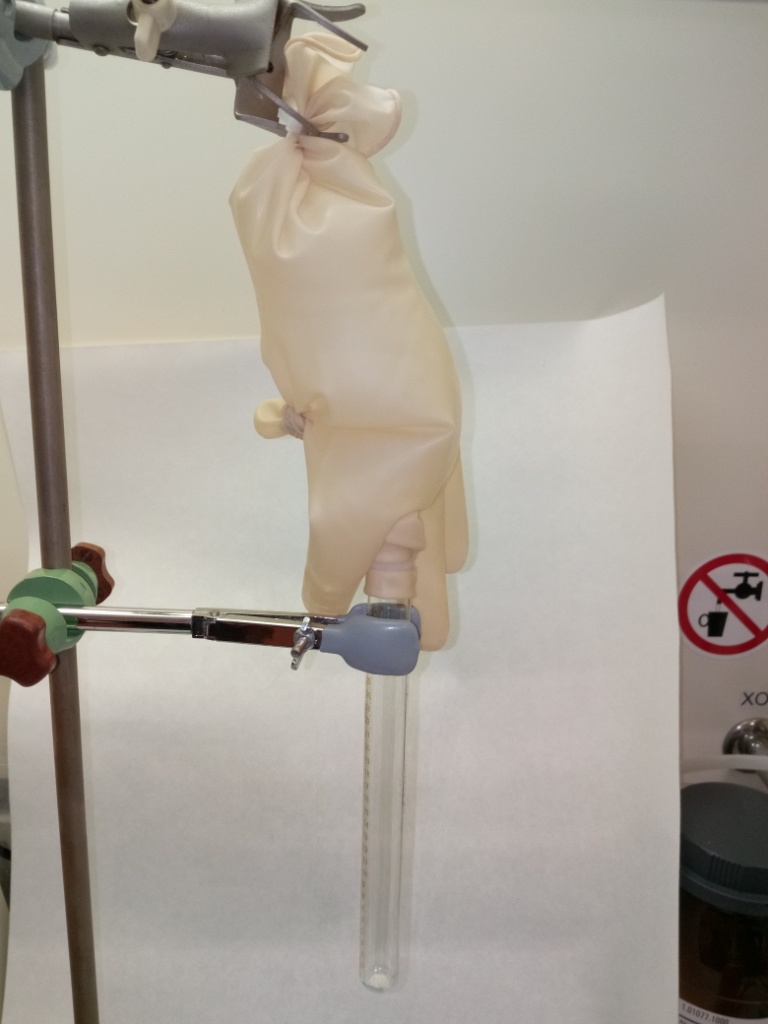
Разложение азида цезия Caesium azide decomposition |
|

|

|

|

|

|

|
|
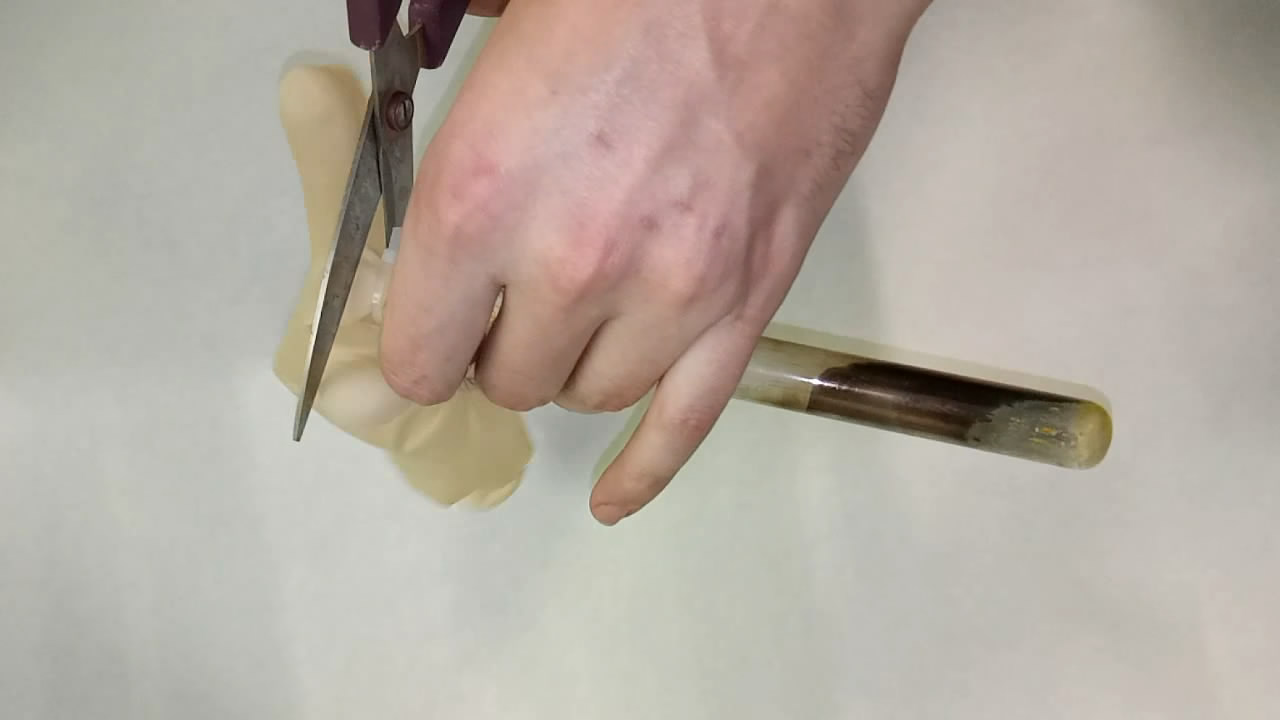
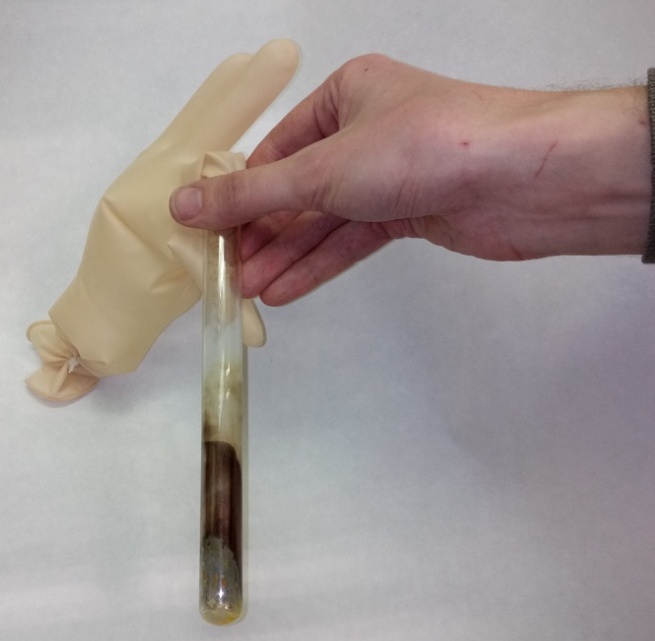
Если пустить в пробирку воздух, цезиевое зеркало быстро исчезает |

|

|

|

|

|

Разложение азида натрия (на воздухе) Sodium azide decomposition (in air) |

|

|

|

|

|

|

|

|

|
|
<Химические вулканы и Фараоновы змеи ч.2> <Химические вулканы ч.1> < Опыты со щелочными металлами > < Опыты со щелочными металлами 1 > [Эксперименты с ацетиленом] [Эксперименты с ацетиленом, метаном, пропаном и бутаном] [Эксперименты с ацетиленом, метаном, пропаном и бутаном 2] <Эксперименты с пропан-бутановой смесью 1> <Эксперименты с пропан-бутановой смесью 2> <Эксперименты с фосфором ч.1> <Эксперименты с фосфором ч.2> <Эксперименты с водородом 1> <Эксперименты с водородом 2> <Эксперименты с водородом 3> <Хлористый азот (трихлорид азота). Иодистый азот (нитрид иода)> <Перекись ацетона, ГМТД, органические перекиси> <Черный порох> <Кумулятивный эффект (№5 2011)> <Нитроглицерин, Этиленгликольдинитрат, Нитроэфиры, Нитропроизводные> <Огонь от капли воды (№1 2012)> <Огонь на ладони (Холодный огонь)> <Ртуть, Амальгамы, Соединения Ртути> <Щелочные металлы (Обсудить на форуме)> [Отправить Комментарий / Сообщение об ошибке] |