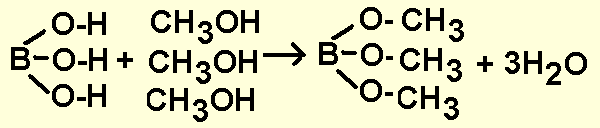Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Вступление
Подобно другим неорганическим и органическим кислотам борная кислота H3BO3 образует эфиры со спиртами. Наиболее известным из эфиров борной кислоты является триэтилборат B(OC2H5)3 и триметилборат B(OCH3)3 (эфиры борной кислоты с этиловым C2H5OH и метиловым CH3OH спиртом соответственно, другое название - борноэтиловый и борнометиловый эфир).
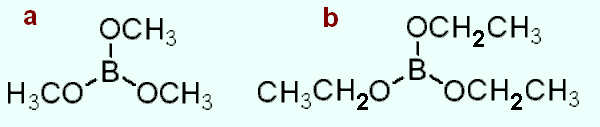
Строение молекул триметилбората (a) и триэтилбората (b)
Во-первых, эти вещества горят зеленым пламенем. Учитывая, что метиловый и этиловый эфиры борной кислоты легко образуются, их используют для демонстрационных экспериментов.
Во-вторых, среди "широкой публики" и даже среди химиков бытует убеждение, что триэтилборат горит холодным пламенем. Например, приходилось встречать утверждения:
"пламя триэтилбората имеет температуру 40 °С";
"пламя триэтилбората настолько холодное, что не поджигает бумагу, в нем можно свободно держать руку".
Довольно показательной в этом отношении является статья в Википедии о холодном пламени. Приведем дословную цитату: