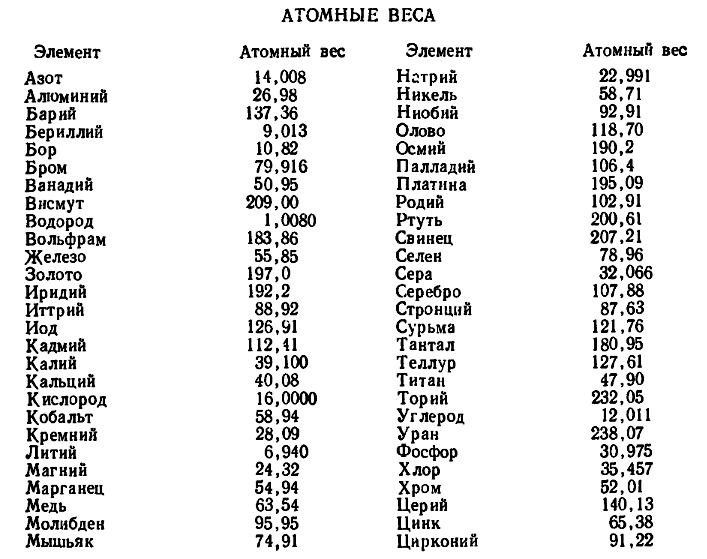
Пятьдесят четыре известных во времена Берцелиуса элемента, атомные веса которых вычислены исходя из атомного веса кислорода (16.0000) (из книги «Поиски элементов»).
| Оглавление | Видео опыты по химии | На главную страницу |
|
Химия и Химики № 2 2012 |
Краткая история химии. Развитие идей и представлений в химии Айзек Азимов |
|
Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Глава 8. Периодическая таблица
В истории развития органической и неорганической химии XIX столетия наблюдается любопытная параллель. В первые десятилетия число вновь открытых органических соединений, а также элементов увеличивалось ошеломляюще быстро. В третьей четверти столетия органические соединения были в определенной степени систематизированы благодаря введению структурных формул. До некоторой степени упорядочены были и элементы; отчасти этому способствовали итоги Международного химического конгресса, который состоялся в начале сентября 1860 г. в г. Карлсруэ.
Однако начнем с беспорядка, царившего в начале столетия. Античные ученые, как известно, описали десять элементов, средневековые алхимики - четыре. В XVIII столетии были открыты такие газообразные элементы, как азот, водород, кислород и хлор, и такие металлы, как кобальт, платина, никель, марганец, вольфрам, молибден, уран, титан и хром. В первом десятилетии XIX в. к этому списку добавилось не менее четырнадцати новых элементов. Так, только Дэви выделил с помощью электролиза ни мало, ни много шесть элементов, Гей-Люссак и Тенар выделили бор, Уолластон - палладий и родий, Берцелиус открыл церий. Английский химик Смитсон Теннант (1761-1815), у которого Уолластон работал в качестве ассистента, открыл осмий и иридий. Другой английский химик Чарльз Хэтчетт (ок. 1765-1847) выделил колумбий (теперь официально называемый ниобием), а шведский химик Андерс Густаф Экеберг (1767-1813) открыл тантал. Последующие десятилетия были не столь богаты открытиями, но тем не менее число элементов продолжало расти. Так, Берцелиус открыл еще четыре элемента: селен, кремний, цирконий и торий. Луи Никола Воклен в 1797 г. открыл бериллий. К 1830 г. было открыто пятьдесят пять различных элементов. В теории алхимиков фигурировало всего лишь четыре элемента, и такое резкое увеличение списка элементов, которые, вдобавок, сильно отличались по свойствам, озадачило химиков. Почему элементов столько? Сколько их еще осталось открыть? Десять? Сто? Тысячу? Бесконечное число? Заманчиво было попытаться как-то упорядочить список уже известных элементов. Может быть, при этом удастся выявить число еще неоткрытых элементов и обнаружить какую-то закономерность в изменении свойств уже открытых? Первым, кому удалось уловить некоторые проблески порядка, был немецкий химик Иоганн Вольфганг Дёберейнер (1780-1849). В 1829 г., изучая свойства брома - элемента, открытого тремя годами ранее французским химиком Антуаном Жеромом Баларом (1802-1876), Дёберейнер установил, что бром по своим свойствам занимает промежуточное положение между хлором и йодом. [Йод был открыт другим французским химиком Бернаром Куртуа (1777-1838) в 1811 г.] В ряду хлор - бром - йод наблюдалось не только постепенное изменение цвета и реакционной способности, но и постепенное изменение атомного веса. Случайное совпадение? Дёберейнер продолжил поиски и нашел еще две группы из трех элементов (он назвал их триадами), у которых также наблюдалось постепенное изменение свойств. Этими группами были кальций, стронций, барий и сера, селен, теллур. В обеих группах атомный вес среднего элемента примерно равен среднему атомных весов двух других элементов. Опять совпадение? Дёберейнер пытался найти другие такие триады, но безуспешно. Поскольку разбить пятьдесят шесть известных элементов на триады не удалось, химики пришли к выводу, что триады Дёберейнера - явление случайное. Более того, соответствие в изменении атомных весов и химических свойств элементов в триадах Дёберейнера не произвело никакого впечатления на химиков. В первой половине XIX в. химики вообще недооценивали значение атомных весов. Атомные веса было удобно использовать при проведении разного рода расчетов, но ориентироваться на них, например, при составлении списка элементов представлялось нерезонным. Существовали сомнения относительно целесообразности использования атомных весов в проведении расчетов. Некоторые химики не проводили четкого различия между атомным весом и молекулярным весом; некоторые путали понятия «атомный вес» и «эквивалентный вес». Так, например, эквивалентный вес кислорода равен 8 , атомный вес - 16, молекулярный вес - 32. При проведении расчетов удобнее всего пользоваться эквивалентным весом, который равен 8, почему же в таком случае для определения места кислорода в списке элементов следует использовать число 16? Эта путаница с эквивалентным, атомным и молекулярным весами не только мешала решить вопрос о списке элементов, но и вообще отрицательно сказалась на развитии химии. Разногласия по поводу относительных атомных весов, приписываемых различным атомам, привели к разногласиям и в отношении числа атомов отдельных элементов, входящих в данную молекулу. Кекуле вскоре после опубликования своих предложений относительно структурных формул ясно понял, что его идея повиснет в воздухе, если химики не смогут прийти к согласию в вопросе об эмпирических формулах. Поэтому он предложил для обсуждения этого вопроса созвать конференцию ведущих химиков Европы. В результате в 1860 г. в г. Карлсруэ в Германии впервые в истории состоялась международная научная встреча химиков, получившая название «Первый международный химический конгресс». На конгрессе присутствовало 140 делегатов, и среди них итальянский химик Станислао Канниццаро (1826-1910) [2]. Двумя годами ранее Канниццаро случайно обнаружил работу своего соотечественника Авогадро. Изучив эту работу, Канниццаро увидел, как с помощью гипотезы Авогадро можно разграничить понятия «атомный вес» и «молекулярный вес» для основных газообразных элементов и что, используя это различие, можно внести ясность в вопрос об атомных весах элементов вообще. Кроме того, он увидел, насколько важно четко отличать атомный вес от эквивалентного веса. На конгрессе Канниццаро произнес яркую речь по этому вопросу, а затем распространил брошюру, в которой детально излагал свою точку зрения. Ему удалось убедить химиков в своей правоте, хотя произошло это не сразу и потребовало больших усилий. С этого времени в вопрос об атомных весах была внесена ясность и было по достоинству оценено значение таблицы атомных весов, составленной Берцелиусом. Применительно к органической химии это означало, что теперь можно уже было договориться об эмпирических формулах соединений и продолжить изучение строения молекул, уточняя расположение атомов сначала плоскостное, а затем и пространственное. В неорганической же химии теперь был принят рациональный порядок расположения элементов - в порядке увеличения их атомных весов. Как только такой список был составлен, химики смогли посмотреть на него под новым углом зрения. |

Пятьдесят четыре известных во времена Берцелиуса элемента, атомные веса которых вычислены исходя из атомного веса кислорода (16.0000) (из книги «Поиски элементов»). |
|
В 1864 г. английский химик Джон Александер Рейна Ньюлендс (1837-1898) расположил известные элементы в порядке возрастания атомных весов. Составив такой список элементов, он обнаружил, что в полученном ряду можно выявить определенную закономерность в изменении свойств элементов. Когда Ньюлендс расположил элементы вертикальными столбцами по семь элементов в столбце, то выяснилось, что сходные элементы, как правило, попадают в одни и те же горизонтальные ряды. Так, калий располагается вслед за очень похожим на него натрием, селен располагается в одном ряду с похожей на него серой, кальций - рядом с похожим на него магнием и т. д. Действительно, в соответствующем ряду можно было найти каждую из трех триад Дёберейнера.
Ньюлендс назвал открытую им закономерность законом октав, так как каждый восьмой элемент обладал свойствами, сходными с первым, девятый - со вторым и т. д.
(В музыкальной октаве семь нот, восьмая нота начинает новую октаву.) К сожалению, помимо рядов, содержащих сходные элементы, в таблице были ряды с совершенно непохожими элементами. Поэтому другие химики сочли такое совпадение случайным и отнеслись к открытию Ньюлендса как к не заслуживающему внимания факту. Ньюлендсу не удалось даже опубликовать свою работу. Двумя годами раньше французский геолог Александр Эмиль Бегюйе де Шанкуртуа (1820-1886) также расположил элементы в порядке возрастания атомных весов и отметил их на так называемом «винтовом» графике. И в этом случае наблюдалась та же тенденция: сходные элементы попадали в вертикальные столбцы. Публикуя свое сообщение, Шанкуртуа не сопроводил его построенным им графиком, и его работа также осталась незамеченной. |

«Закон октав» Ньюлендса (1864 г.). |
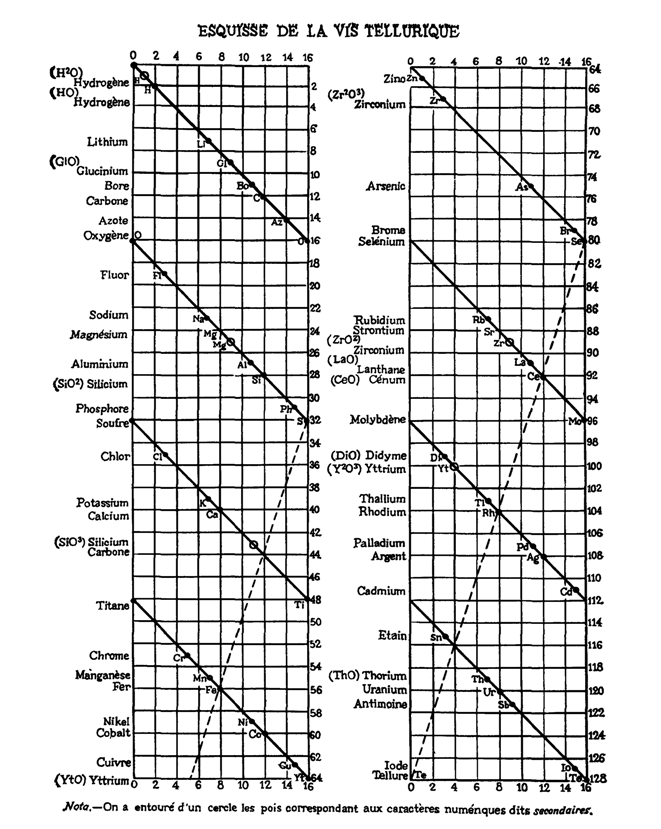
«Винтовой график» Бегуйе де Шанкуртуа (1862 г.) Расположив элементы в порядке возрастания их атомных весов, ученый соединил линиями элементы с похожими свойствами. |
|
Более удачливым оказался немецкий химик Юлиус Лотар Мейер (1830-1895). Мейер рассматривал объемы, занимаемые весовыми количествами элемента, численно равными их атомным весам. При этом выяснилось, что в каждом таком весовом количестве любого элемента содержится одно и то же число атомов. Это означало, что отношение рассматриваемых объемов различных атомов равнялось отношению объемов отдельных атомов этих элементов [3]. Поэтому указанная характеристика элемента получила название атомный объем.
Графически зависимость атомных объемов элементов от их атомных весов выражается в виде ряда волн, поднимающихся острыми пиками в точках, соответствующих щелочным металлам (натрию, калию, рубидию и цезию). Каждый спуск и подъем к пику соответствует периоду в таблице элементов. В каждом периоде значения некоторых физических характеристик, помимо атомного объема, также закономерно сначала уменьшаются, а затем возрастают. Водород - элемент с наименьшим атомным весом - стоял в списке элементов первым. В то время принято было считать, что первый период включает лишь один элемент. (В современных таблицах первый период включает два элемента - водород и гелий.) Второй и третий периоды графика Мейера включали каждый по семь элементов, эти периоды дублировали октавы Ньюлендса. Однако в следующих двух периодах число элементов превышало семь. Таким образом Мейер показал, в чем ошибка Ньюлендса. Закон октав не мог строго выполняться для всего списка элементов, последние периоды должны были быть длиннее первых. Мейер опубликовал свою работу в 1870 г. Годом раньше русский химик Дмитрий Иванович Менделеев (1834-1907) установил порядок изменения длины периодов элементов и наглядно продемонстрировал значение своего открытия [4]. Менделеев выполнял свою диссертационную работу в Германии, в Гейдельберге, как раз во время Международного химического конгресса в Карлсруэ. Он присутствовал на конгрессе и слышал речь Канниццаро, в которой тот четко изложил свою точку зрения на проблему атомного веса. Вернувшись в Россию, Менделеев приступил к изучению списка элементов и обратил внимание на периодичность изменения валентности у элементов, расположенных в порядке возрастания атомных весов: валентность водорода 1, лития 1, бериллия 2, бора 3, углерода 4, магния 2, азота 3, серы 2, фтора 1, натрия 1, алюминия 3, кремния 4, фосфора 3, кислорода 2, хлора 1 и т. д. Основываясь на увеличении и уменьшении валентности, Менделеев разбил элементы на периоды; первый период включает только один водород, затем следуют два периода по семь элементов каждый, затем периоды, содержащие более семи элементов. Менделеев воспользовался этими данными не только для того, чтобы построить график, как это сделали Мейер и Бегюйе де Шанкуртуа, но и для того, чтобы построить таблицу, подобную таблице Ньюлендса. Такая периодическая таблица элементов была яснее и нагляднее, чем график, и, кроме того, Менделеев сумел избежать ошибки Ньюлендса, настаивавшего на равенстве периодов. Свою таблицу Менделеев опубликовал в 1869 г., т. е. раньше, чем была издана основная работа Мейера. Однако честь открытия Периодической системы элементов принадлежит Менделееву [5] не из-за приоритета публикации, действительная причина состоит в том, как Менделеев построил свою таблицу. Для того чтобы выполнялось требование, согласно которому в столбцах должны находиться элементы с одинаковой валентностью, Менделеев в одном или двух случаях был вынужден поместить элемент с несколько большим весом перед элементом с несколько меньшим весом. Так, теллур (атомный вес 127.6, валентность 2) пришлось поместить перед йодом (атомный вес 126.9, валентность 1), чтобы теллур попал в один столбец с элементами, валентность которых равна 2, а йод попал в один столбец с элементами, валентность которых равна 1 [6]. Поскольку этого оказалось недостаточно, Менделеев счел также необходимым оставить в своей таблице пустые места (пробелы). Причем наличие таких пробелов он объяснил не несовершенством таблицы, а тем, что соответствующие элементы пока еще не открыты. В усовершенствованном варианте таблицы (1871 г.) существовало много пробелов, в частности не заполнены были клетки, отвечающие аналогам бора, алюминия и кремния. Менделеев был настолько уверен в своей правоте, что пришел к заключению о существовании соответствующих этим клеткам элементов и подробно описал их свойства. Он назвал их экабор, экаалюминий и экакремний («эка» на санскрите означает «одно и то же»). Таким образом Менделеев развил идею Дёберейнера о промежуточном значении атомного веса среднего элемента в триаде; однако никто из предшественников Менделеева не рискнул предугадывать существование и свойства неоткрытых элементов. Тем не менее часть химиков была настроена скептически, и, возможно, их недоверие еще долго не удалось бы преодолеть, если бы смелые предсказания Менделеева не подтвердились столь блестяще. Это стало возможно прежде всего благодаря применению нового физического прибора - спектроскопа. |
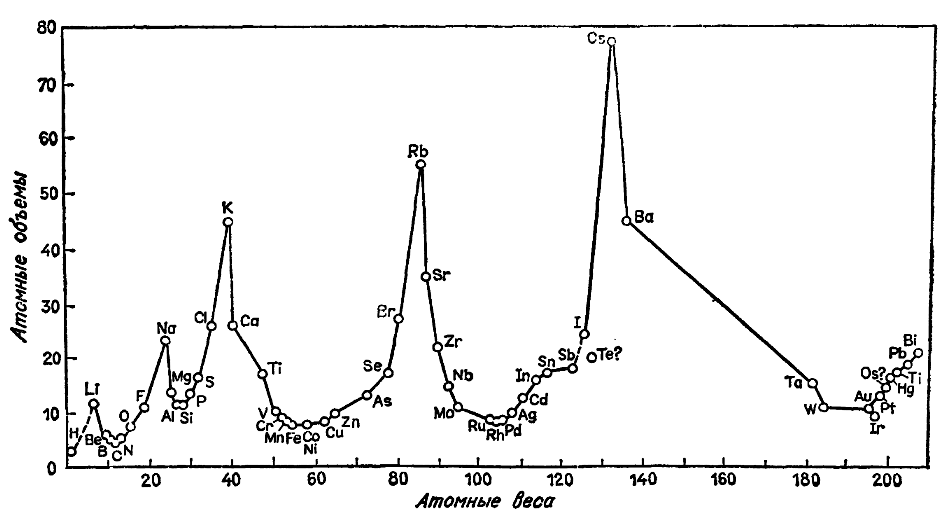
График Мейера (кривая атомных объемов элементов). |

Страница из статьи Менделеева, опубликованной в 1869 г. в «Журнале русского химического общества». В этой статье Менделеев впервые подробно изложил основы периодической системы элементов. |
|
В 1814 г. немецкий оптик Йозеф фон Фраунгофер (1787-1826) испытывал превосходные призмы собственного изготовления. Пропуская луч света сначала через щель, а затем через трехгранные стеклянные призмы, Фраунгофер получил солнечный спектр, пересекаемый рядом темных линий. Он насчитал около шестисот таких линий и тщательно зафиксировал их положение в спектре.
В конце 50-х годов XIX в. немецкий физик Густав Роберт Кирхгоф (1824-1887), работавший с немецким химиком Робертом Вильгельмом Бунзеном (1811-1899), показал, что эти линии содержат поразительную информацию. В качестве источника света эти ученые пользовались изобретенной Бунзеном горелкой - той самой бунзеновской горелкой, которая известна каждому начинающему химику. Сгорающая в горелке смесь газа и воздуха дает почти бесцветное пламя с достаточно высокой температурой. Когда Кирхгоф помещал в пламя горелки крупицы различных химических веществ, оно окрашивалось в разные цвета. Свет от такого пламени, пропущенный через призму, давал не сплошную полосу, а отдельные яркие линии. Кирхгоф показал, что для каждого элемента, разогретого в пламени горелки, характерен свой спектр. Таким образом, снимая спектр излучения химического элемента, Кирхгоф как бы снимал «отпечатки пальцев» такого элемента. Получив такую информацию, можно было решить и обратную задачу: опознать элемент, входящий в состав неизвестного вещества. Прибор, используемый для определения элементов описанным способом, получил название спектроскопа. Сегодня мы уже знаем, что излучение света атомами обусловлено определенными явлениями, связанными с их структурой. В атомах каждого элемента эти явления протекают по-своему. Следовательно, каждый элемент испускает набор излучений только определенных длин волн. При облучении светом элементов в парообразном состоянии наблюдается обратная картина: свет определенных длин волн не излучается, а поглощается. Более того, поскольку как поглощение, так и излучение света обусловлено одними и теми же процессами, протекающими в противоположных направлениях, то пары поглощают излучение с точно теми же длинами волн, какие наблюдаются в других условиях при испускании излучения. Представлялось весьма вероятным, что темные линии в спектре Солнца обусловлены тем, что испускаемый раскаленной солнечной поверхностью свет поглощают газы более холодной солнечной атмосферы. Пары веществ (химических элементов), находящиеся в атмосфере Солнца, также поглощают свет определенных длин волн, и по положению возникающих темных линий в спектре можно судить, какие элементы находятся в атмосфере Солнца. Именно спектроскоп позволил доказать, что Солнце (а также звезды и межзвездный газ) состоит из элементов, полностью идентичных земным. Этот вывод окончательно разбил утверждение Аристотеля, считавшего, что небесные тела состоят из веществ, отличающихся по своей природе от веществ, составляющих Землю. С изобретением спектроскопа химики получили новый эффективный способ обнаружения элементов. Так, например, если в спектре раскаленного минерала содержатся линии, не принадлежащие известным элементам, то есть основания предполагать, что этот минерал содержит неизвестный элемент. Бунзен и Кирхгоф сами продемонстрировали эффективность этого метода. В 1860 г., исследуя образец минерала, они обнаружили в его спектре линии, которые не принадлежали ни одному из известных элементов. Начав поиски нового элемента, они установили, что это щелочной металл, близкий по своим свойствам натрию и калию. Бунзен и Кирхгоф назвали открытый ими металл цезием (от латинского caesius - сине-серый), так как в спектре этого металла самой яркой была именно синяя линия. В 1861 г. эти ученые открыли еще один щелочной металл, который также назвали по цвету его спектральной линии рубидием (от латинского rubidus - темно-красный). Новый прибор начали использовать и другие химики. Одним из них был французский химик Поль Эмиль Лекок де Буабодран (1838-1912), который в течение пятнадцати лет изучал минералы своих родных Пиренеев. В 1875 г., исследуя спектр цинковой руды, он нашел новый элемент, который назвал галлием (Галлия - древнеримское название Франции). Спустя некоторое время Лекок де Буабодран получил такое количество этого элемента, что смог изучить его свойства. Ознакомившись с сообщением ученого, Менделеев сразу же указал, что новый элемент - это его экаалюминий. Дальнейшие исследования полностью подтвердили справедливость такого утверждения: свойства галлия оказались идентичны описанным Менделеевым свойствам экаалюминия. Два других элемента из числа предсказанных Менделеевым были открыты старыми методами. В 1879 г. шведский химик Ларе Фредерик Нильсон (1840-1899) открыл новый элемент и назвал его скандием (в честь Скандинавии). Один из коллег Нильсона, шведский химик Пер Теодор Клеве (1840-1905), сразу же указал на сходство свойств скандия и описанного Менделеевым экабора. Наконец, в 1886 г. немецкий химик Клеменс Александр Винклер (1838-1904), анализируя серебряную руду, установил, что на долю содержащихся в ней известных элементов приходится только 93% ее веса. Пытаясь отыскать недостающие 7%, Винклер открыл новый элемент, названный им германием (в честь Германии). Оказалось, что этот элемент идентичен экакремнию Менделеева. Таким образом, в течение пятнадцати лет были открыты все три элемента, предсказанные Менделеевым, причем свойства всех трех элементов на удивление точно соответствовали свойствам, описанным Менделеевым. После этого в ценности и полезности периодической таблицы уже не могло быть никаких сомнений. |
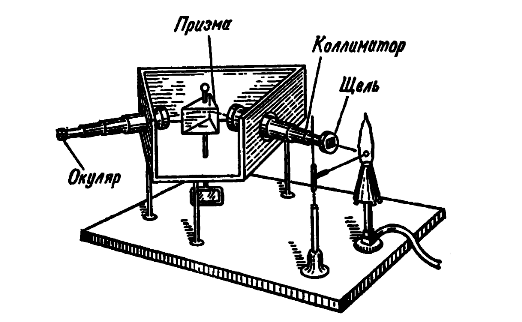
Схема спектроскопа. Сравнивая спектры излучений раскаленных металлов, ученые смогли открыть новые элементы. |
|
Однако таблице Менделеева предстояла еще одна серьезная проверка - в ней должно было найтись место для других вновь открытых элементов.
Например, еще в 1794 г. финский химик Юхан Гадолин (1760-1852) предположил, что в минерале, полученном из Иттербийского карьера, расположенного вблизи Стокгольма, содержится новый оксид металла (или земля). Поскольку эта новая земля значительно отличалась от уже известных земель, например кремнезема, извести и магнезии, то ее отнесли к редким землям. Гадолин назвал открытый им оксид иттрия по названию карьера; спустя 50 лет из этого оксида был выделен в относительно чистом виде новый элемент - иттрий. Примерно в середине XIX столетия химики начали интенсивно изучать состав редкоземельных минералов. Проведенные исследования показали, что эти минералы содержат целую группу новых элементов - редкоземельных элементов. Шведский химик Карл Густав Мосандер (1797-1858) открыл, например, в конце 30-х - начале 40-х годов XIX в. четыре редкоземельных элемента: лантан, эрбий, тербий и дидим. На самом деле их было пять, поскольку спустя сорок лет в 1885 г. австрийский химик Карл Ауэр фон Вельсбах (1858-1929) обнаружил, что дидим представляет собой смесь двух элементов, которые он назвал празеодимом и неодимом. Лекок де Буабодран также открыл два редкоземельных элемента: самарий в 1879 г. и диспрозий в 1886 г. Сразу два редкоземельных элемента - гольмий и тулий описал в 1879 г. П. Т. Клеве, а в 1907 г. французский химик Жорж Урбэн (1872-1938) сообщил о новом четырнадцатом редкоземельном элементе - лютеции (Лютеция - древнее название Парижа). Редкоземельные элементы обладают очень сходными химическими свойствами, их валентность равна трем. По-видимому, все эти элементы необходимо было поместить в один столбец периодической таблицы. Однако ни один из столбцов не был таким длинным, чтобы вместить четырнадцать элементов. Далее, поскольку атомные веса всех редкоземельных элементов очень близки, их следовало поместить в один горизонтальный ряд, другими словами, в один период. В принципе их можно было поместить в шестой период, если предположить, что он длиннее, чем четвертый и пятый, которые в свою очередь длиннее, чем второй и третий периоды. Однако объяснить причины сходства свойств редкоземельных элементов в то время не удалось (это было сделано лишь в 20-х годах XX в.). Другая группа вновь открытых элементов, о существовании которой во времена Менделеева химики и не подозревали, не вызвала таких затруднений; элементы этой группы прекрасно вписались в периодическую таблицу. В 80-х годах XIX в. английский физик Джон Уильям Стратт, лорд Рэлей (1842-1919), с большой точностью определил атомные веса кислорода, водорода и азота. При этом он установил, что атомный вес азота меняется в зависимости от источника газа. Так, атомный вес азота, полученного перегонкой жидкого воздуха, немного больше, чем у азота, полученного химическим путем. Шотландский химик Уильям Рамзай (1852-1916) заинтересовался этой проблемой и вспомнил об эксперименте Кавендиша, который еще в 1785 г. пытался связать азот воздуха с кислородом; в свое время эта работа не привлекла внимания химиков. Кавендиш установил тогда, что последний пузырек газа нельзя было заставить соединиться с кислородом ни при каких условиях. Логично было предположить, что этот последний пузырек газа мог быть и не азотом. Возможно, получаемый из воздуха азот содержит в качестве примеси другой газ, плотность которого выше, и именно поэтому полученный из воздуха азот кажется немного тяжелее, чем есть на самом деле. В 1894 г. Рамзай повторил эксперимент Кавендиша, выделил оставшийся пузырек газа и провел его анализ новым методом, во времена Кавендиша еще неизвестным. Рамзай нагрел этот газ, изучил его спектр. В результате выяснилось, что оставшийся пузырек представляет собой новый газ, плотность которого несколько выше, чем у азота. Содержание его в атмосфере равно примерно 1% (по объему). Он химически инертен, не реагирует ни с одним другим элементом. По этой причине газ получил название аргон (от греческого αρυος - инертный). Атомный вес аргона, как выяснилось, чуть меньше 40. Это означало, что аргон должен располагаться в периодической таблице где-то возле таких элементов, как сера (атомный вес 32), хлор (атомный вес 35.5), калий (атомный вес 39) и кальций (атомный вес чуть больше 40). Исходя только из атомного веса аргона, его следовало поместить между калием и кальцием. Однако, согласно установленному Менделеевым принципу, валентность играет более важную роль, чем атомный вес. Поскольку аргон не взаимодействует ни с одним элементом, то, следовательно, валентность его равна нулю. Куда в таком случае поместить аргон? Валентность серы равна 2, хлора 1, калия 1 и кальция 2. Таким образом, в этой области периодической таблицы валентность меняется в следующей последовательности: 2, 1, 1, 2. Нуль в такой последовательности должен располагаться между двумя единицами; 2, 1, 0, 1, 2. Следовательно, место аргона между хлором и калием. Однако, если принять периодическую таблицу как руководство, аргон не может существовать один. Он должен быть одним из представителей семейства инертных газов - элементов с нулевой валентностью. Столбец, занимаемый этими газами, должен располагаться между столбцами, занятыми галогенами (хлором, бромом и т. д.) и щелочными металлами (натрием, калием и т. д.); валентность и тех, и других равна единице. Рамзай начал поиски. В 1895 г. он узнал, что в США из уранового минерала получены пробы газа - предположительно азота. Рамзай повторил эту работу и установил, что в спектре этого газа содержатся линии, которых нет ни в спектре азота, ни в спектре аргона, зато такие же линии наблюдал в солнечном спектре во время солнечного затмения 1868 г. французский астроном Пьер Жюль Сезар Жанссен (1824-1907). В то время английский астроном Джозеф Норман Локьер (1836-1920) приписал эти линии новому элементу, который он назвал гелием (от греческого ηλιος - Солнце). В свое время химики почти не обратили внимания на это сообщение: новый элемент был открыт на Солнце, да еще довольно новым, не вполне завоевавшим доверие методом. Однако работа Рамзая показала, что тот же самый элемент существует и на Земле. Рамзай сохранил за элементом название, данное ему Локьером. Так был открыт гелий - самый легкий из инертных газов, который стоит вслед за водородом - элементом с наименьшим атомным весом. В 1898 г., осторожно нагревая жидкий воздух в поиске инертных газов, которые, как предполагал Рамзай, будут испаряться первыми, он обнаружил три новых газа. Рамзай назвал их неон (новый), криптон (скрытый) и ксенон (чуждый). Сначала считалось, что инертные газы могут представлять интерес только как объект научного исследования и никакого практического применения они не найдут. Однако в своих исследованиях, начатых им в 1910 г., французский химик Жорж Клод (1870-1960) показал, что электрический ток, пропускаемый через некоторые газы, подобные неону, вызывает мягкое окрашенное свечение. Практическое применение этого свойства хорошо известно: таким газом можно заполнять трубки, изогнутые в виде букв, слов, фигур и т. п., и уже в 40-х годах нашего столетия улицы больших городов заливал неоновый свет [7]. |
|
____________________
[1] См.: Фигуровский Н. А. Открытие элементов и происхождение их названий. - М.: Наука, 1970, 207 с. [2] На конгрессе присутствовали русские ученые А. П. Бородин, Н. Н. Зинин, Т. Лесинский, Д. И. Менделеев, Я. Натансон, Л. Н. Шишков. О С. Канниццаро см.: Быков Г. В., Крицман В. А. Станислао Канниццаро. Очерк жизни и деятельности. - М.: Наука, 1972, 215 с. [3] Указанное соотношение выполняется лишь приблизительно, поскольку атомы различных элементов не всегда заполняют одинаковые части занимаемого веществом пространства. [4] См.: Кедров Б. М. День одного великого открытия. - М.: Соцэкгиз, 1958, 560 с.; Кедров Б. М. Философский анализ первых трудов Д. И. Менделеева о периодическом законе (1869-1871). - М.: Изд-во АН СССР, 1959, 294 с.; Фигуровский Н. А. Дмитрий Иванович Менделеев. - М.: Изд-во АН СССР, 1961, 315 с. [5] В данном случае Менделеев интуитивно принял правильное решение, однако объяснить, почему элементы следует располагать именно таким образом, удалось лишь спустя около полувека. [6] Открытие Д. И. Менделеевым периодического закона датируется 17 февраля (1 марта) 1869 г., когда им была составлена таблица, озаглавленная "Опыт системы элементов, основанной на их атомном весе и химическом сходстве". В 1864 г. Л. Мейер предложил таблицу для нескольких групп элементов, в которой он показывал соотношение их атомных масс, но никаких теоретических выводов не делал. Менделеев же развил свои представления, придав уже к 1871 г. своей периодической системе современный вид. [7] По материалам этой главы см. также: Макареня А. А. Д. И. Менделеев и физико-химические науки. Опыт научной биографии Д. И. Менделеева. - М.: Атомиздат, 1972; Трифонов Д. Н. Структура и границы периодической системы. - М.: Атомиздат, 1969; Б. М. Кедров, Д. Н. Трифонов. Закон периодичности и химические элементы. Открытия и хронология. - М.: Наука, 1969, 194 с.; Соловьев Ю. И., Петров Л. П. Вильям Рамзай. 1852-1916. - М.: Наука, 1971, 239 с. |
| < Содержание >
< Глава 1 >
< Глава 2 >
< Глава 3 >
< Глава 4 >
< Глава 5 >
< Глава 6 >
< Глава 7 > < Глава 8 > < Глава 9 > < Глава 10 > < Глава 11 > < Глава 12 > < Глава 13 > < Глава 14 > |