Обнаружив ошибку на странице, выделите ее и нажмите Ctrl + Enter
Горение фосфора под водой
Данный опыт если и не принадлежит к числу самых красивых, то, по крайней мере, один из самых необычных. Для начала приведем описание эксперимента из книги Рипан Р. Четяну И. Руководство к практическим работам по неорганической химии ссылка.
Горение белого фосфора под водой (окисление белого фосфора двуокисью хлора до его воспламенения)
В рюмку или стакан Берцелиуса емкостью 200-300 мл насыпают около 10 г хлората калия KClO3, наливают 140-200 мл воды и бросают 3-4 кусочка фосфора величиной с пшеничное зерно.
При помощи длинной воронки или пипетки наливают на бертолетову соль с фосфором концентрированную серную кислоту.
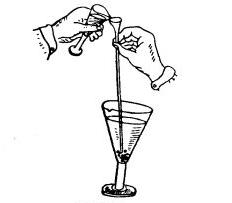
Выделяющийся при взаимодействии хлората калия и концентрированной серной кислоты двуокись хлора окисляет фосфор (в жидкости появляются яркие искры).
Плавлению и загоранию белого фосфора способствует тепло, выделяющееся при введении в воду концентрированной серной кислоты и в результате реакции между хлоратом и серной кислотой.
Разлагающаяся с небольшими взрывами двуокись хлора обуславливает потрескивание в рюмке, при этом происходят следующие реакции:
3KClO3 + 2H2SO4 + 3H2O + 2P = KClO4 + 2KHSO4 + 2H3PO4 + 2HCl
Между двуокисью хлора и фосфором протекает следующая реакция:
2ClO2 + 2P + 4H2O = 2H3PO4 + 2HCl
В приведенной выше методике из практикума Рипана и Четяну рекомендуется взять 10 г бертолетовой соли. К сожалению, у нас такого количества хлората калия не было, поэтому пришлось рекомендованное количество хлората поделить на 10.
Опыт провели в большой пробирке. На дно насыпали чуть больше 1 г хлората калия, налили примерно 10 мл воды, на бертолетову соль поместили кусочек желтого фосфора размером с пшеничное зерно и добавили пипеткой концентрированную серную кислоту.
Были слышны звуки, похожие на вскипание капелек воды, которые попали в горячее масло, от осадка хлората калия начали выделяться пузырьки газа, раствор стал желтовато-зеленым. Отчетливо был слышен запах хлора (так пахнет и диоксид хлора). Фосфор расплавился и превратился в желтую капельку. Возле капли начались желтые вспышки, по всему объему раствора появились желтые искры, раздавался треск. Капелька подпрыгивала и разделялась на более мелкие.
Скоро стало очевидно, что в пробирке не хватает трех вещей: бертолетовой соли, фосфора и серной кислоты. Горение фосфора под водой шло, но оно было не особо активным и слишком растянутым во времени. Другими словами, не следовало уменьшать рекомендованные количества веществ.
Делать нечего: в пробирку пришлось добавлять новые порции хлората калия и кусочки белого фосфора. Пару раз также добавили серную кислоту. В результате горение активизировалось: по всему объему жидкости плавали шарики фосфора, время от времени вспыхивая. Некоторые шарики всплывали на поверхность, где сгорали ярким желтым пламенем, образуя белый дым.
В темноте опыт выглядел красивее, но снимать его было труднее.


































































